Clear Sky Science · tr
Nanoparçacık temelli fototerapi sistemleri: moleküler mekanizmalar ve klinik uygulamalar
Işık: Nazik Bir Tıbbi Araç
Çoğumuz ışığı görmemizi sağlayan, cildimizi ısıtan veya güneş panellerini çalıştıran bir şey olarak düşünürüz. Bu derleme makale daha şaşırtıcı bir rolü inceliyor: dikkatle ayarlanmış ışığın, küçük mühendislikle üretilmiş parçacıklarla birlikte kullanılarak hastalıkları içeriden teşhis etmek ve tedavi etmek. Yazarlar, «nanoparçacık temelli fototerapi»nin zararını kanser hücrelerine odaklayabileceğini, kalp ve eklemlerdeki iltihabı yatıştırabileceğini ve hatta Alzheimer gibi durumlarda beyin içindeki toksik proteinleri temizlemeye yardımcı olabileceğini; tüm bunları yaparken çoğu sağlıklı dokuyu koruyabildiğini anlatıyorlar.
Küçük Parçacıklar Işığı Nasıl İlaca Dönüştürür
Bu yaklaşımın merkezinde, insan kılcalının genişliğinden binlerce kez daha küçük olan nanoparçacıklar bulunur; bu yapılar ilaç taşıyabilir, ışığı emebilir ve bu ışığı ya ısıya ya da kısa ömürlü kimyasal patlamalara dönüştürebilir. İki ana strateji öne çıkar. Fotodinamik terapide, nanoparçacığın yüzeyinde veya içinde bulunan ışıkla aktive olan moleküller, yakındaki hücre bileşenlerine zarar veren yüksek enerjili oksijen formları (reaktif oksijen türleri) üretir. Fototermal terapide ise altın veya siyah fosfor gibi diğer parçacıklar, yakın-infrared ışığı ısıya çevirerek tümör hücrelerini kısa süreliğine içeriden ‘‘pişirir’’. Işık hedeflenebildiği ve parçacıklar esas olarak hastalıklı dokularda birikecek biçimde tasarlanabildiği için, doktorlar geleneksel kemoterapi ve radyasyonun sahip olmadığı mekânsal hassasiyete ulaşır. 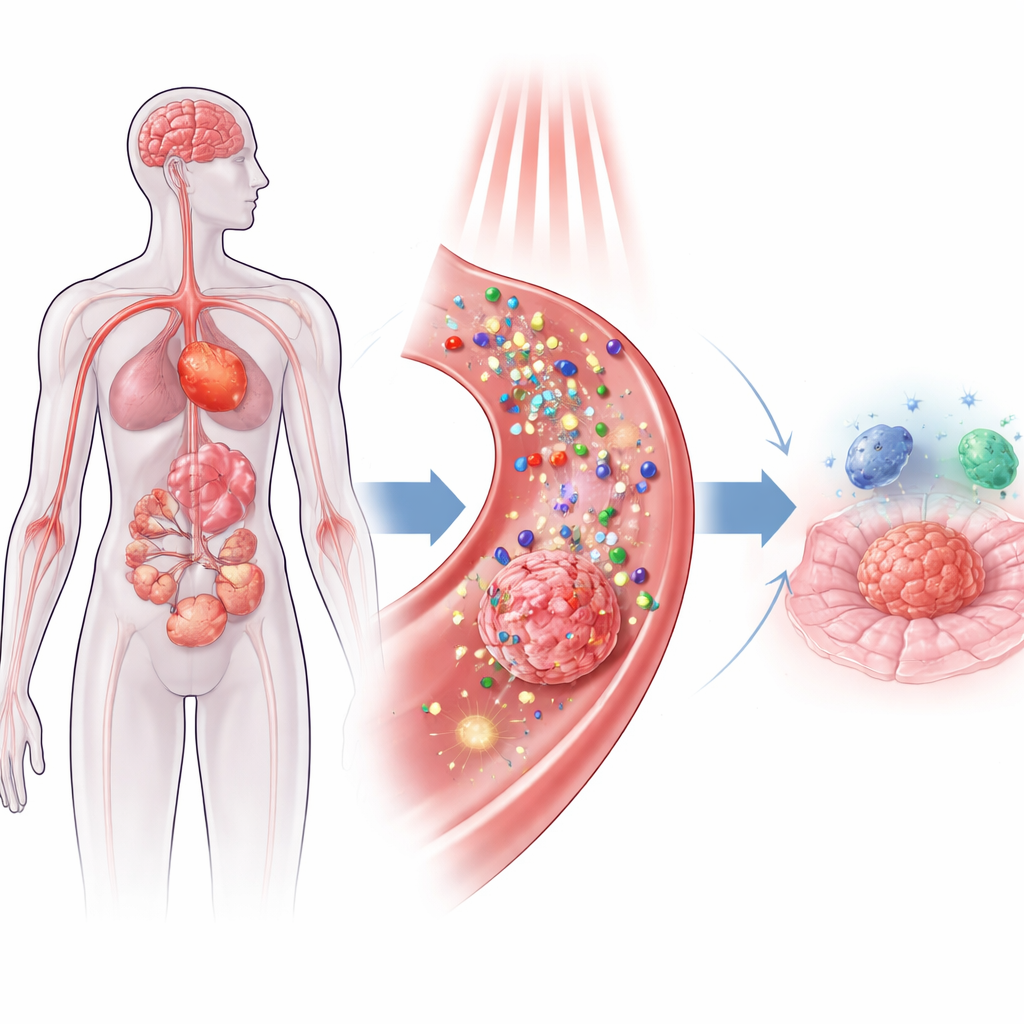
Daha Akıllı Taşıyıcılar ve Verme Yolları İnşa Etmek
Sadece vücuda ışık tutmak yeterli değildir; zorluk doğru parçacıkları doğru yere ulaştırmak ve onların etkili olacak kadar uzun süre orada kalmasını sağlamaktır. İnceleme, lipid veziküller (lipozomlar) gibi yumuşak taşıyıcılar, katı yağ parçacıkları ve polimer bazlı küreler veya miseller ile silika, metal, karbon veya metal-organik çerçeveler gibi sert iskeletlerden oluşan bir teslimat araçları kutusunu listeliyor. Yüzeyleri dolaşım süresini uzatmak için gizlenme polimerleriyle, bağışıklık savunmalarından kaçmak için doğal hücre zarlarıyla veya kanser ya da iltihaplı hücrelerdeki belirteçleri tanıyan “adres etiketleri” ile kaplanabilir. Bazı tasarımlar ‘‘akıllı’’dır: kan dolaşımında inert kalır, ancak tümör içindeki asidite, enzimler veya redoks koşullarına yanıt olarak boyut, yük veya şekil değiştirir ve içeriklerini yalnızca gerektiği yerde serbest bırakır.
Işık Hücrelere Çarptığında İçinde Neler Olur
Işık açıldığında, moleküler bir dizi olay başlar. Yazarlar, ışıkla uyarılan parçacıkların zarlar, DNA ve mitokondri ve lizozomlar gibi hayati yapılar üzerinde saldırılar düzenleyen oksidan patlamaları nasıl ürettiğini açıklar. Bu, hücreleri düzenli bir kendi kendine yok oluşa (apoptoz) itebilir veya hasar şiddetliyse, daha kaotik bir ölüme yol açabilir. Hücreler ayrıca otofaji adı verilen içsel bir geri dönüşüm sürecini artırabilir; bu süreç hafif streste hayatta kalmalarına yardımcı olabilir veya bunları bunalmış haldeyken daha hızlı yok olmaya sürükleyebilir. Kritik olarak, ölen tümör hücreleri bağışıklık sistemini harekete geçiren ‘‘tehlike’’ sinyalleri yayabilir: yüzeylerinde belirli proteinleri ortaya çıkarabilir, dendritik hücreleri çeken faktörler salabilir ve tümörle ilişkili bağışıklık hücrelerini baskılayıcı halden tümörle savaşan bir duruma dönüştürebilir. Aslında, lokal bir ışık tedavisi kişiye özel bir kanser aşısı gibi de işlev görebilir. 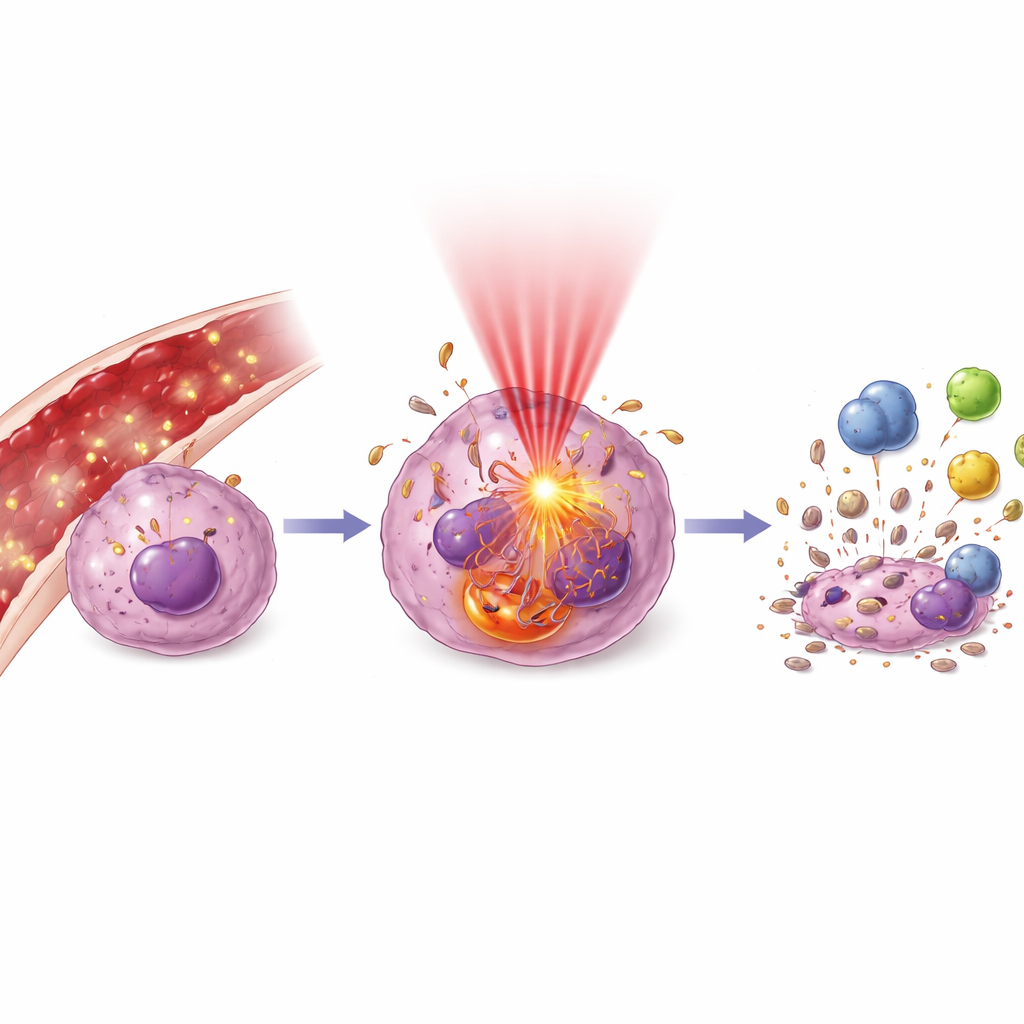
Kansere Ek olarak: Kalp, Beyin ve Otoimmün Hedefler
Kanser en gelişmiş alan olsa da, aynı ilkeler kronik durumlara uyarlanıyor. Kardiyovasküler hastalıkta, ışık bazlı yaklaşımlar hücreleri öldürmeyi hedeflemez; bunun yerine oksidatif stresi azaltmak, damar iç yüzeyini stabilize etmek ve tehlikeli plakları küçültmek veya sertleştirmeye yardımcı olmak amaçlanır. Beyinde, nöronlar çok hassas olduğundan, genellikle fotobiyomodülasyon olarak adlandırılan daha nazik ışık rejimleri mitokondriyal enerji üretimini artırmayı, toksik protein kümelerini azaltmayı ve mikroglia ile astrosit kaynaklı iltihabı azaltmayı hedefler. İnceleme ayrıca metabolik ve otoimmün hastalıklarda yürütülen erken çalışmaları vurguluyor; burada dikkatle dozlanmış ışık ve nanoparçacıklar bağışıklık hücrelerini dokuya zarar veren saldırgan davranıştan uzaklaştırıp daha düzenleyici, yatıştırıcı rollere doğru yönlendirebilir ve aynı zamanda insülin hassasiyetini ve yağ dokusu sinyalizasyonunu ılımlı bir şekilde iyileştirebilir.
Laboratuvardan Klinğe: Umutlar ve Engeller
On yıllarca süren araştırmalara rağmen, yalnızca birkaç ışıkla aktive olan ilaç tam onay almıştır; bunların çoğu göz hastalıkları ve bazı tümörler içindir. Yazarlar, nanoteknolojinin daha derin ışık nüfuzuna, daha iyi hedeflemeye ve tedaviyi gerçek zamanlı izlemek için yerleşik görüntülemeye olanak vererek bir sonraki dalgayı açmaya başladığını savunuyor. Yine de büyük engeller sürüyor: nanoparçacık üretiminin tutarlı kaliteyle ölçeklendirilmesi, uzun vadeli güvenlik ve vücuttan temizlenmenin kanıtlanması, derin organlara ışığın etkili şekilde iletilmesi ve sıkı düzenleyici gerekliliklerin karşılanması. İnceleme, malzeme bilimi, optik, biyoloji ve yapay zeka rehberliğindeki tasarımı birleştirerek nanoparçacık temelli fototerapinin niş uygulamalardan daha geniş, invaziv olmayan bir hassas tıbbın dayanağı haline gelmeye hazırlandığı sonucuna varıyor.
Atıf: Chauhan, D.S., Prasad, R., Dhanka, M. et al. Nanoparticles-based phototherapy systems: molecular mechanisms and clinical applications. Sig Transduct Target Ther 11, 95 (2026). https://doi.org/10.1038/s41392-025-02536-w
Anahtar kelimeler: nanoparçacık fototerapi, fototermal tedavi, fotodinamik tedavi, kanser nanoterapisi, fotobiyomodülasyon