Clear Sky Science · tr
IFFO1, LaminA/C-PGC1α ekseni aracılığıyla mitokondri bölünmesi ve yağ asidi sentezini koordine ederek meme kanserini engeller
Bu araştırma neden önemli
Meme kanseri, bazı tümörlerin büyümeye, yayılmaya ve mevcut tedavileri alt etmeye devam etmesi nedeniyle kadınlarda kanser kaynaklı ölümlerin önde gelen nedenlerinden biri olmaya devam ediyor. Bu çalışma, tümör büyümesinin iki temel motorunu—hücrenin enerji fabrikaları olan mitokondrileri ve yağ üretme ile depolama yeteneğini—dizginleyen, daha önce yeterince önem verilmeyen IFFO1 adlı hücresel bir “fren”i ortaya koyuyor. Bu frenin anlaşılması, farklı meme kanseri alt tiplerinde işe yarayabilecek yeni terapötik yaklaşımlar için taze bir açı sunuyor.
Meme hücrelerinin içindeki gizli bir koruyucu
Araştırmacılar, 30 kadın hastadan alınan örnekleri ve büyük halka açık kanser veritabanlarını inceleyerek çalışmaya başladılar. IFFO1 proteininin düzeylerinin tümör dokusunda çevre normal meme dokusuna göre sürekli olarak daha düşük olduğunu buldular. Kanser evresi ilerledikçe IFFO1 miktarı azaldı ve tümörlerinde daha yüksek IFFO1 bulunan hastaların yaşam süresi eğilimle daha uzundu. Kültürdeki meme kanseri hücrelerinde hücrelerin ekstra IFFO1 üretmeye zorlanması, onların büyüme, bölünme ve göç etme yeteneklerini keskin şekilde azalttı—tümörlerin genişlemesi ve yayılması için gerekli davranışlar. IFFO1 ayrıca kanser hücrelerinin ayrılmasına ve diğer dokulara saldırmasına yardımcı olan epitel–mezenkimal geçiş (EMT) olarak bilinen hücresel programı da bastırdı.
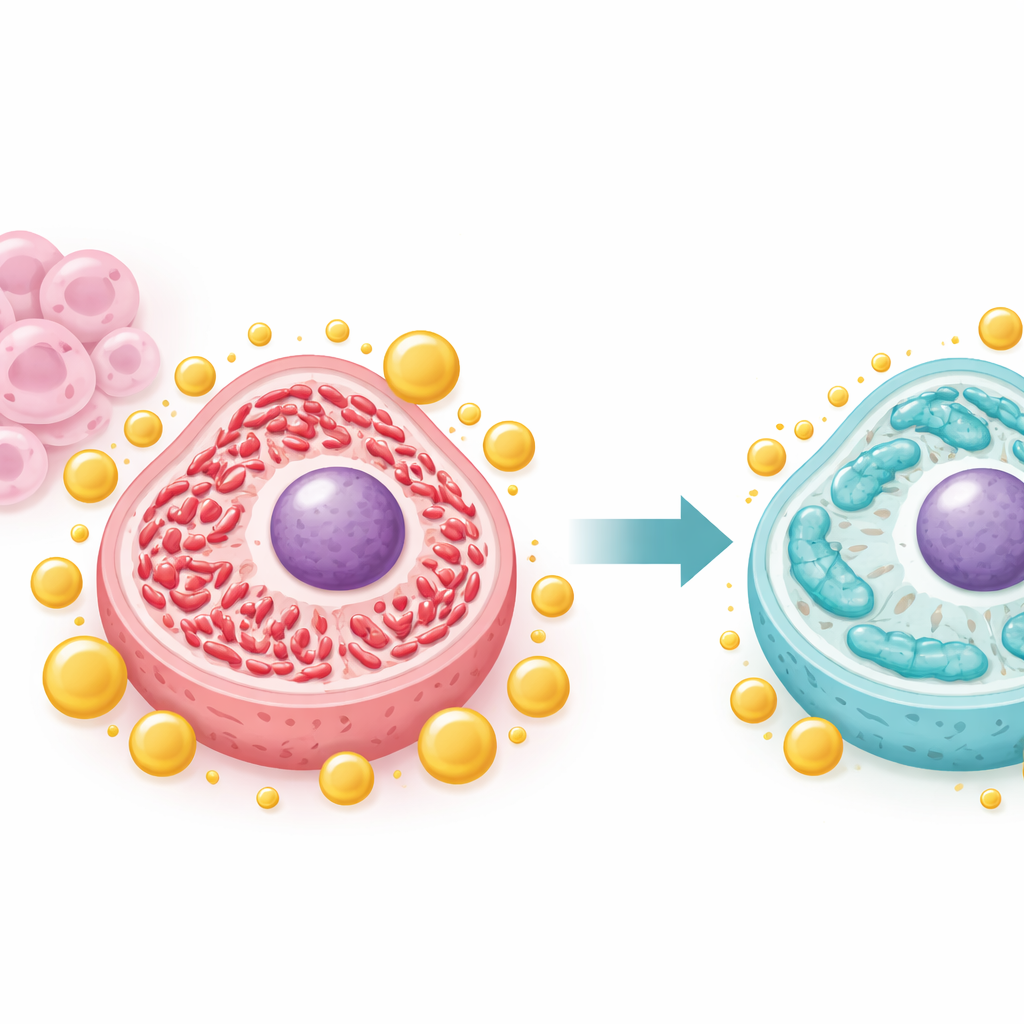
Aşırı aktif enerji fabrikalarını yatıştırmak
Kanser hücreleri sıkça hızlı büyümeyi desteklemek için mitokondrilerini yeniden şekillendirir. Ekip, IFFO1’in bu dengeyi yüksek oranda parçalanmış “bölünme” durumundan, genellikle daha sağlıklı ve daha stabil mitokondrilerle ilişkilendirilen daha uzamış “füzyon” durumuna kaydırdığını gösterdi. IFFO1 bol olduğunda Drp1 ve Fis1 gibi temel bölünme proteinleri azalırken füzyon proteinleri arttı. Mikroskopi, mitokondrilerin daha uzun ve daha az parçalanmış hale geldiğini; mitokondri DNA’sı ve enerji çıktısının agresif hücrelerde görülen anormal yüksek düzeylerden düştüğünü ortaya koydu. Bu değişiklikler, IFFO1’in mitokondrilerin kontrolsüz tümör büyümesini destekleyen hiperaktif bir konfigürasyona girmesini engellediğini düşündürüyor.
Yağ tedarik hattını kesmek
Hızlı büyüyen tümörler sadece enerjiye ihtiyaç duymaz; aynı zamanda yeni zarlar ve sinyal molekülleri oluşturmak için düzenli bir yağ tedarikine ihtiyaç duyarlar. Çalışma, IFFO1’in bu metabolik hızlandırıcıyı da bastırdığını buldu. Fazladan IFFO1’e sahip hücrelerde FASN, SREBP‑1, SCD1 ve diğerleri dahil olmak üzere temel yağ yapım proteinleri azaldı. Enzimatik testler yağ sentezleyen aktivitenin düştüğünü doğruladı ve kimyasal analizler serbest yağ asitleri, trigliseritler ve kolesterolde azalma gösterdi. Yağ depolarını vurgulayan görüntüleme boyaları, kanser hücreleri içinde daha az lipid damlası ve daha az nötr yağ olduğunu ortaya koydu. Buna karşılık, bölünme proteini Drp1’i artırmak ters etki yaptı ve yağ üretimini yükseltti; Drp1’i susturmak ise üretimi azalttı—bu durum, mitokondri şekli ile kanserde yağ tedariki arasında doğrudan bir bağlantıyı destekliyor.
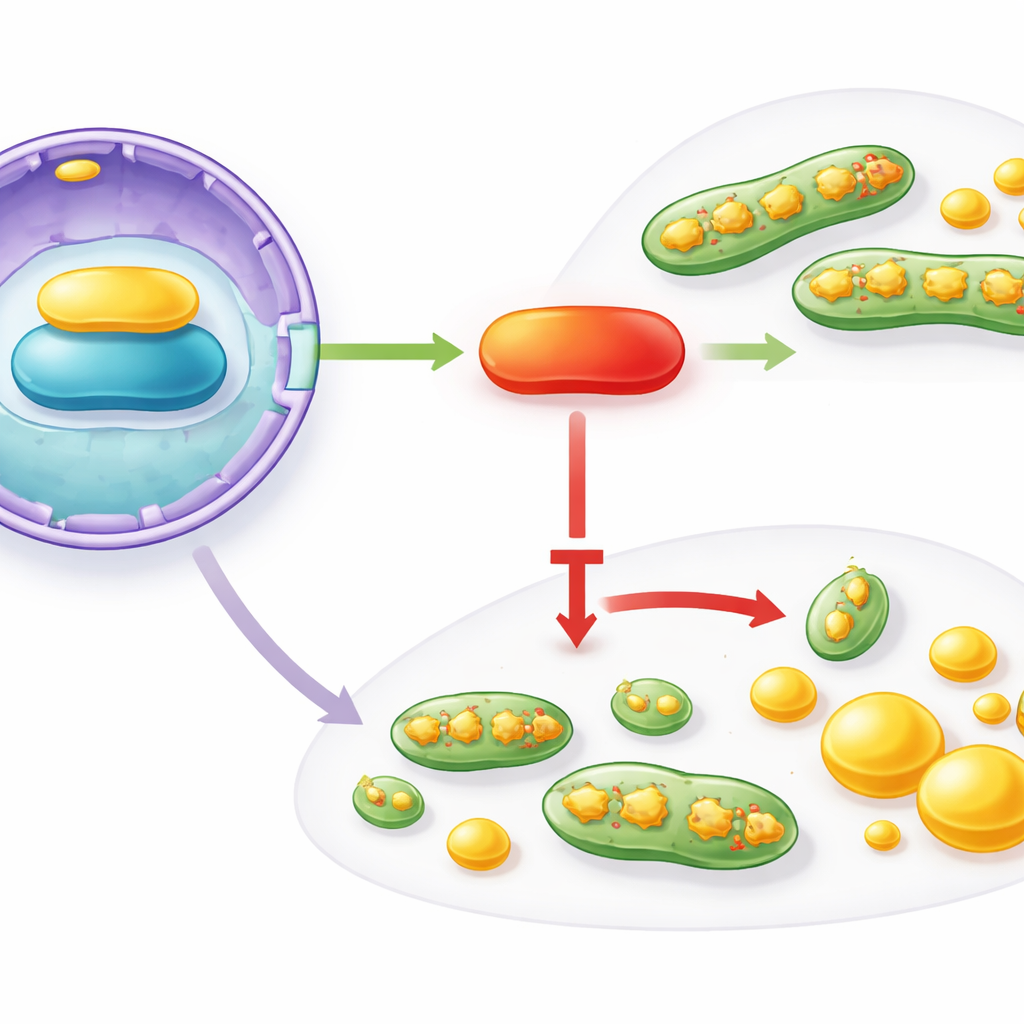
Çekirdekten mitokondriye bir sinyal zinciri
IFFO1 bu geniş değişiklikleri nasıl organize ediyor? Yazarlar, hücre çekirdeğinde başlayıp mitokondri ve yağ yapım makinelerine kadar ulaşan bir etkileşim zincirini izlediler. IFFO1, nükleer zarfın yapısal bir proteini olan Lamin A/C ile fiziksel olarak bağlanıyor ve onun düzeylerini artırıyor. Lamin A/C ise mitokondri sağlığı ve metabolizmayı denetleyen ana düzenleyici PGC1α’nın aktivitesini destekliyor. Meme kanseri dokularında ve hücrelerinde Lamin A/C ile PGC1α’nın her ikisinin de IFFO1 kaybını yansıtacak şekilde azaldığı bulundu. Bilim insanları yapay olarak IFFO1’i artırdıklarında Lamin A/C ve PGC1α yükseldi, mitokondri bölünmesi azaldı ve yağ sentezi zayıfladı. Lamin A/C’yi baskılama bu faydaları ortadan kaldırdı, ancak PGC1α’yı geri getirmek bunları yeniden sağladı; bu da tümör-promote eden mitokondri ve lipid değişikliklerini sınırlayan fonksiyonel bir IFFO1 → Lamin A/C → PGC1α eksenini işaretliyor.
Frene canlı hayvanlarda bakmak
Bu hücresel etkilerin gerçek tümörlere yansıyıp yansımadığını görmek için ekip, ekstra IFFO1 içeren veya içermeyen insan meme kanseri hücrelerini farelere nakletti. IFFO1 artırılmış tümörler daha yavaş büyüdü, deneysel son noktada daha az ağırlığa sahipti ve yağ birikimi belirtileri daha azdı. Kan dolaşımına enjekte edilerek akciğer metastazı oluşturma modelinde ise IFFO1 fazla üreten hücreler belirgin şekilde daha az akciğer tümör nodülü oluşturdu. Bu farelerden alınan doku analizleri hücre kültürü bulgularını yansıtıyordu: daha yüksek Lamin A/C ve PGC1α, daha az mitokondri bölünmesi ve daha düşük yağ sentezi.
Gelecekteki tedaviler için ne anlama geliyor
Bir arada ele alındığında, bu çalışma IFFO1’i hücrenin yapısal iskeleti, enerji fabrikaları ve yağ yapım makinesini birbirine bağlayan çok katmanlı bir tümör baskılayıcı olarak sunuyor. Lamin A/C’yi stabilize ederek ve PGC1α’yı yükselterek IFFO1, mitokondrilerin aşırı parçalanmasını önlüyor ve kanser hücrelerinin dayandığı yağların aşırı üretimini kesiyor. Uzman olmayanlar için ana mesaj, bu proteinin meme kanseri büyümesini ve yayılmasını besleyen hem enerji hem de yapı taşları üzerinde içsel bir fren görevi gördüğüdür. IFFO1 düzeylerini yükselten veya Lamin A/C–PGC1α yoluna etkilerini taklit eden ilaçlar bir gün özellikle agresif veya tedaviye dirençli meme kanseri formları için yeni seçenekler sunabilir.
Atıf: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
Anahtar kelimeler: meme kanseri, mitokondri dinamiği, yağ asidi sentezi, tümör metabolizması, PGC1α yolu