Clear Sky Science · tr
Onkojenik nükleotid sentezinin kontrolü
Kanser Hücreleri Neden Yapıtaşlarını Önemser?
Kanser sıklıkla bölünmeyi durduramayan hücreler olarak tanımlanır. Ancak kendilerini kopyalayabilmek için bu hücrelerin DNA ve RNA’yı oluşturan ve birçok hücresel süreci de besleyen küçük yapıtaşları olan nükleotidlere sürekli erişimi olmalıdır. Bu derleme, kansere yol açan genlerin nükleotid üretimini sürdürmek için hücre kimyasını nasıl yeniden düzenlediğini, tümörlerin bu molekülleri edinmenin farklı yolları arasında nasıl geçiş yaptığını ve doktorların bu hileleri eski ve yeni ilaçlarla nasıl kullanabileceğini açıklar.
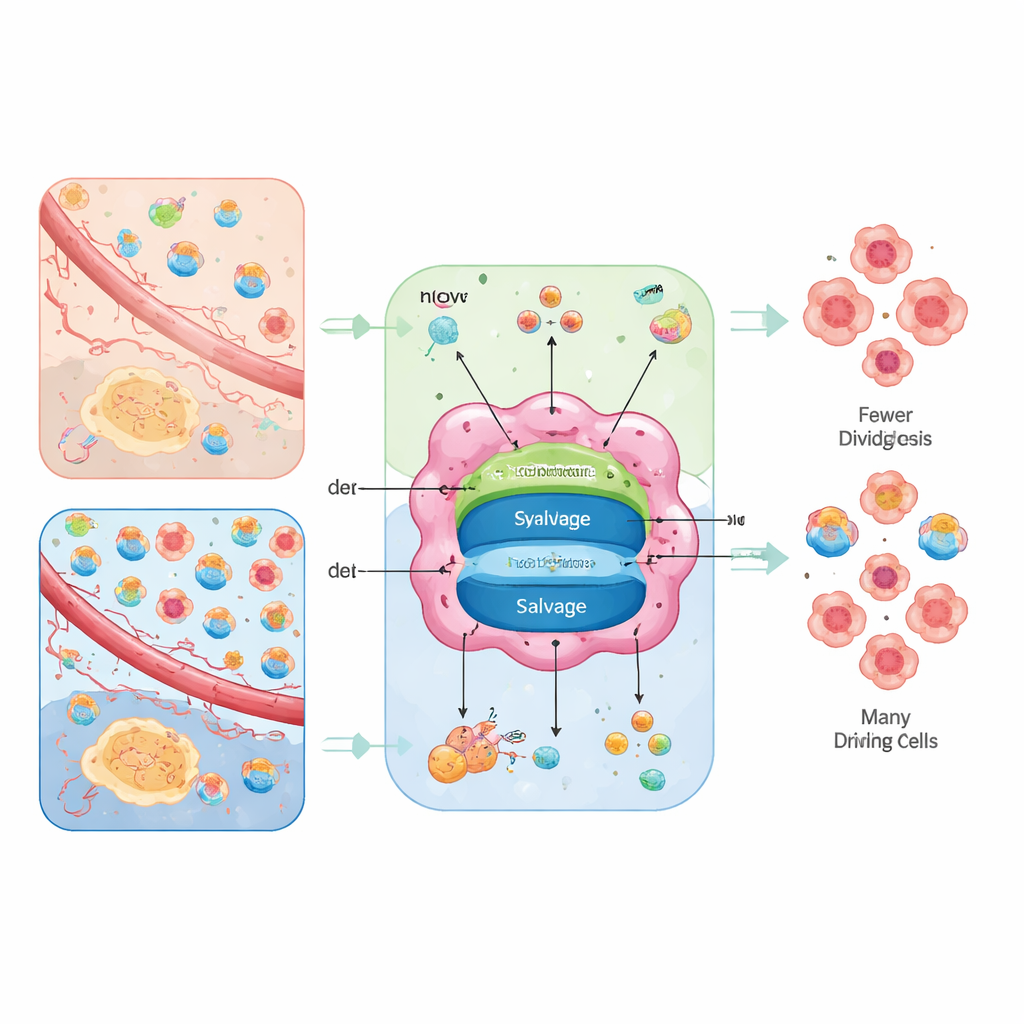
Aynı Yapıtaşlarına Giden İki Yol
Hücreler nükleotidleri sıfırdan yapabilir veya geri dönüştürebilir. "Sıfırdan" yol, de novo sentez olarak adlandırılır; glukoz, amino asitler, karbondioksit ve bikarbonat gibi temel besinlerden halkaları enerji yoğun, çok aşamalı reaksiyonlarla bir araya getirir. Geri dönüşüm yolu, salvage, dışarıdan veya hücresel atıklardan gelen yıkılmış bazları ve nükleozidleri alıp çok daha düşük enerji maliyetiyle tekrar kullanılabilir nükleotidlere dönüştürür. Tümörler her iki seçeneği de kullanır, ancak bunlar arasındaki denge onların iç güç kaynağına ve çevre dokunun sağladıklarına bağlıdır.
Tümör Ortamı Seçimi Nasıl Yönlendirir
Yazarlar nükleotid arzını "ortamın şekillendirdiği yönlendirme" problemi olarak çerçeveler. Amino asitlerin bulunduğu ama serbest nükleozidlerin kıt olduğu kötü beslenen bölgelerde kanser hücreleri büyük ölçüde de novo yolara dayanır ve bu adımları engelleyen ilaçlara karşı hassas hale gelir. Kan akımının yeterli olduğu, bol nükleozidin sağlandığı veya mitokondrilerin zayıf olduğu bölgelerde tümörler daha çok salvage'e güvenebilir ve bunun yerine nükleozid alımını engelleyen taşıyıcı bloklayıcılarına duyarlı olur. Her iki seçenek de açıksa tümörler metabolik esneklik gösterir ve tekil ilaçlardan kaçabilir; her iki yol kapandığında hücreler DNA replikasyonunda durur, hasar birikir ve ölebilir ya da daha olgun, daha az agresif bir duruma geçebilirler.
Nükleotid Arzını Besleyen Gizli Destek Hatları
Nükleotid fabrikalarını çalışır durumda tutmak birkaç destek devresi gerektirir. Pentoz fosfat yolu şeker iskeletini ve redüksiyon gücünü sağlar; glutamin ve mitokondrideki enerji üreten çevrim azot ve aspartatı temin eder; serin, glisin ve folat kimyası halkaları tamamlayan tek karbon birimlerini bağışlar; bikarbonat ise gerekli karbonları getirir. PI3K–AKT–mTORC1, RAS–MAPK ve MYC gibi kanser sürücüleri bu yolları birlikte yükseltir, kilit enzimleri artırır ve hatta kararsız ara ürünleri verimli şekilde yönlendiren çok-enzim kümeleri oluşturur. Buna karşılık LKB1–AMPK ve p53 gibi stres sensörleri normalde enerji veya DNA bütünlüğü tehlikede olduğunda frene basarak nükleotid çıktısını azaltır—birçok tümörün devre dışı bıraktığı frenler.
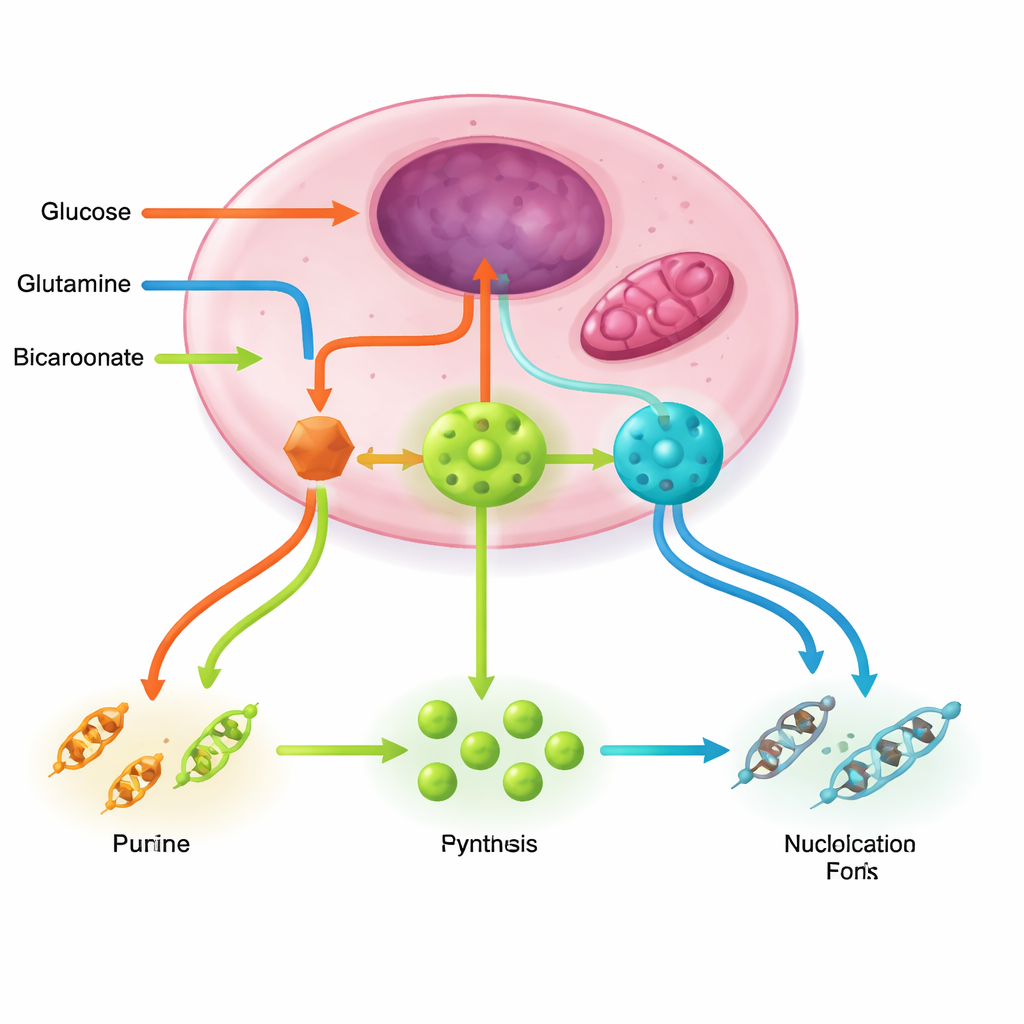
Eski Kemoterapi, Yeni Metabolik Mantık
Hızlı büyüyen hücreler nükleotidlere çok bağımlı olduğu için en erken kemoterapilerden bazıları bu zayıflığı hedef aldı. Metotreksat, 5‑florourasil, sitarabin, gemsitabin ve çeşitli pürin analogları gibi klasik ilaçlar ya folat kullanımını engeller, belirli enzimleri inhibitörler ya da hatalı yapıtaşları olarak davranıp DNA ve RNA’yı zehirler. Derleme bu ilaçları yönlendirme modeli merceğinden yeniden ele alır ve yan etkiler ile direncin neden yaygın olduğunu açıklar: kanser dışı dokular da nükleotidlere ihtiyaç duyar ve tümörler genellikle bir düğüm bloke edildiğinde akışı salvage veya paralel yollar üzerinden yeniden yönlendirebilir.
Yeni Nesil Stratejiler ve Açık Sorular
Daha yeni yaklaşımlar ağın en kanser-yanlı parçalarına saldırarak daha seçici olmayı amaçlıyor. MTHFD2 gibi mitokondrial tek karbon enzimlerine, DHODH gibi pirimidin enzimlerine ve IMPDH ile PAICS gibi pürin enzimlerine karşı deneysel ilaçlar geliştirilmekte, sıklıkla salvage taşıyıcılarını da bloke eden kombinasyonlarla birlikte. Yazarlar hangi tümörlerin de novo ya da salvage'e daha çok dayandığını belirlemek ve hastaları yol-hedefli tedavilerle eşleştirmek için taşıyıcı düzeyleri, kan damar yoğunluğu, mitokondriyal dayanıklılık ve belirli metabolik enzimlerin ekspresyonu gibi pratik belirteçler önerir. İleriye bakıldığında, gerçek tümörlerin içinde bu yolların zaman ve mekan içinde nasıl değiştiği, çevreleyen immün ve stromal hücrelerin nükleotid kullanılabilirliğini nasıl şekillendirdiği ve replikasyon stresinden yararlanırken normal dokuları aşırı zorlamayan tolere edilebilir ilaç programlarının nasıl tasarlanacağı gibi temel soruları vurgularlar. Birlikte, bu çalışma nükleotid metabolizmasını anlamanın ve hedeflemenin hücre bölünmesinin temel bir gereksinimini kansere karşı güçlü, kişiselleştirilmiş bir kaldıraç haline getirebileceğini savunur.
Atıf: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
Anahtar kelimeler: nükleotid metabolizması, kanser metabolizması, de novo sentez, salvage yolları, metabolik tedaviler