Clear Sky Science · tr
Yeni bir K6-K14 keratin füzyonunun indüklediği sitoskeleton yeniden düzenlenmesi, cGAS-STING seçilimi yoluyla kanser kök hücre özelliklerini ve hücresel plastisiteyi artırıyor
Şekil Değiştiren Kanser Hücreleri Çevrelerini Nasıl Kandırır
Kanser hücreleri yalnızca kontrolsüz büyümez; hayatta kalmak, saklanmak ve yayılmak için kendi iç “iskeletlerini” (sitoskeletonlarını) büküp şekillendirmeyi öğrenirler. Bu çalışma, baş ve boyun kanseri hücreleri içinde ortaya çıkan belirli bir yapısal kusurun çekirdekleri zedeleyip yerleşik bir tehlike alarmını tetikleyerek hücreleri uykuya soktuğunu ve nihayetinde daha agresif, invazif, kök hücre benzeri hücreler olarak geri dönmelerine nasıl yardımcı olduğunu gösteriyor. Bu mekanik yolun kanser evrimine katkısını anlamak, nüks ve metastazı engellemenin yeni yollarını açabilir.
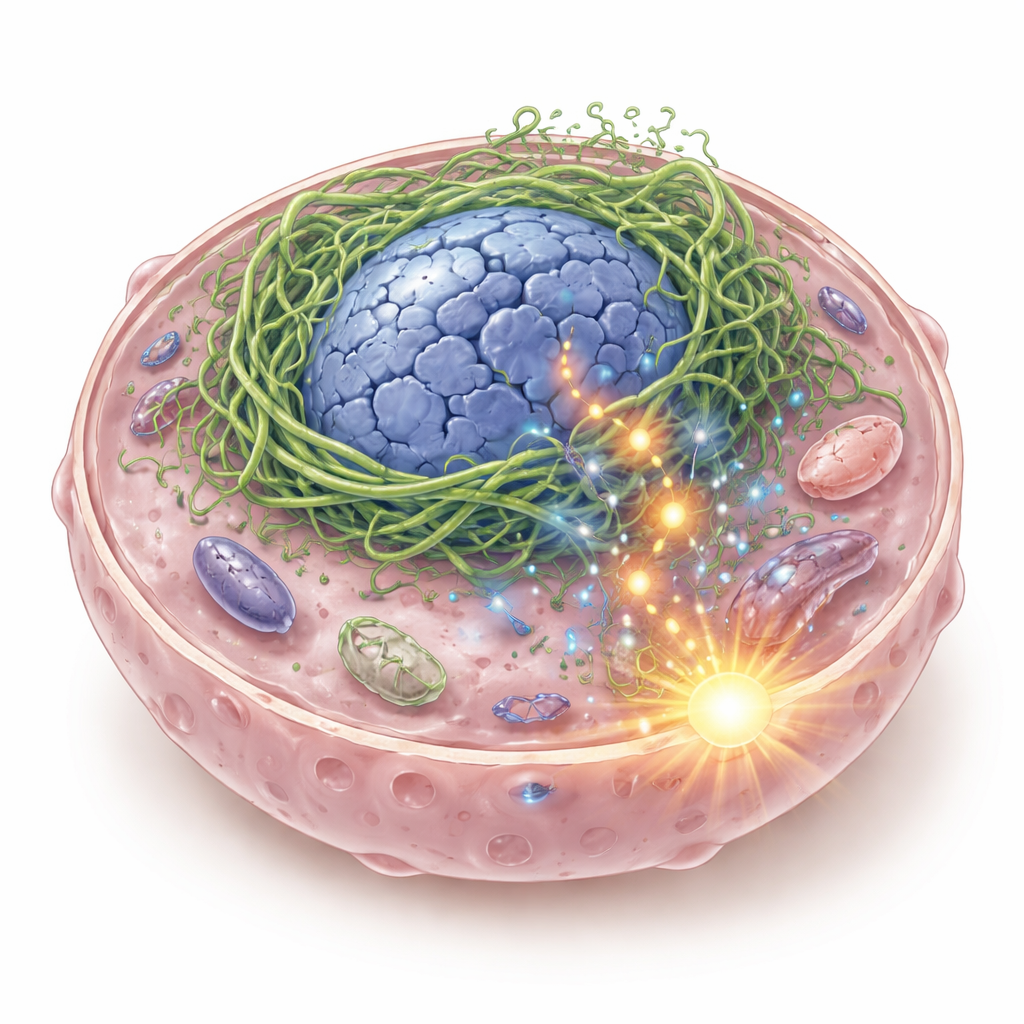
Tehlikeli Sonuçları Olan Kırık Bir İç İskelet
Her hücrenin içinde hücreyi ve çekirdeğini şekillendiren ve fiziksel güçleri algılamasına yardımcı olan protein filamentlerinden oluşan esnek bir iskelet vardır. Yazarlar, ağız ve boğazın döşeyen epitel dokularda yaygın olan bir iskelet proteinleri ailesi olan keratinlere odaklandı. Bazı baş ve boyun skuamöz hücreli kanserlerinde, iki keratin geninin birleşmesiyle oluşan K6-K14/V5 adlı hibrit bir keratin keşfettiler. Bu füzyon proteini kanser hücrelerinde aktif hale geldiğinde düzgün bir destek ağı oluşturmaz; bunun yerine çekirdeğin etrafında sıkı kümeler yaparak onu içi boş, şekli bozulmuş yapılara dönüştürür ve DNA kırılmalarına yol açar. DNA parçaları hücre sıvısına sızar ve burada normalde viral DNA varlığında alarm veren cGAS–STING adlı bir bağışıklık algılama sistemi tarafından tespit edilir.
Hücre Ölümü Baskısından Gizli Hayatta Kalmaya
Bu çekirdek hasarının hemen etkisi kanser hücreleri için zararlıdır: büyümeleri yavaşlar ve birçoğu ölür. Ancak bir kısmı dayanmayı başarır. Bu hayatta kalanlar fiziksel çevrelerinden güçlü şekilde etkilenir. Standart düz plastik yüzeylerde zamanla kaybolurken, gerçek doku dokusuna daha yakın olan yumuşak kolajen jel içinde büyütüldüklerinde varlıklarını sürdürür ve 3D-V5 olarak adlandırılan yeni bir popülasyon olarak yeniden ortaya çıkarlar. Gen aktivite analizleri, bu hücrelerin devam eden DNA hasarı alarmına yanıt olarak özellikle hatalı mitokondrileri geri dönüştüren, hasarlı parçaları temizleyen otofaji adlı kendini temizleme programını açtıklarını gösterir. Bu yanıt, ortadan kaldırılmak yerine stresi atlatmalarını sağlayan düşük aktiviteli uykuda bir duruma girmelerine yardımcı olur.
Uyuyan Hücreler Yeniden Kabuk Değiştirir ve Hareket Etmeye Hazırlanır
Uyurken, bu hayatta kalan hücreler sessizce iç programlarını yeniden yazar. Keratin proteinlerinin karışımını değiştirir ve bazı epitel özelliklerini korurken esneklik ve hareket kabiliyeti kazanan kısmi bir epitel–mezenkimal geçiş (pEMT) durumunu benimserler. Küreler oluşturma ve yeni hücre kümeleri tohumlama konusunda çok daha yetenekli hale gelirler; bu, kanser kök hücre özelliklerinin bir göstergesidir. Zamanla mekanik özellikleri geri kazanır: çekirdeklerini yeniden sertleştirir, güçlü aktin liflerini yeniden inşa eder ve çevre matrisi inceleyen ve kavrayan uzun çıkıntılar geliştirirler. Ayrıca ekstraselüler ağı parçalayarak ilerleme yolları açan matriks metalloproteinazlar (MMP'ler) adlı enzimleri artırırlar.
Destekleyici Bir Niş Oluşturmak İçin Komşu Hücrelerle Konuşmak
Bu yeniden programlanmış kanser hücreleri tek başına hareket etmez. Ekip, 3D-V5 hücrelerinin çevrelerine bol miktarda ekstraselüler vezikül adı verilen küçük paketler saldığını gözlemledi. Bu veziküller yakınlardaki oral fibroblastlara—bağ doku hücreleri—ulaştığında, fibroblastlar kendi gen aktivitelerini değiştirir ve tümör büyümesini destekleyen kanser ilişkili fibroblastlara benzeyen bir duruma geçerler. Değiş tokuş edilen sinyallerin çoğu, hücre proliferasyonu, plastisite ve direnç sürüklemesiyle bilinen büyüme faktörleri ve reseptörlerinden oluşan FGF–FGFR ekseni etrafında döner. Hem kültürde hem de fare tümörlerinde FGFR aktivitesini engellemek bu büyüme avantajını azalttı. Hayvanlarda, 3D-V5 hücrelerinden oluşan tümörler kötü farklılaşmış, daha invazif, kök hücre belirteçleri açısından zengin ve enjekte edildikleri bölgenin ötesine yayılmaya daha yatkındı.
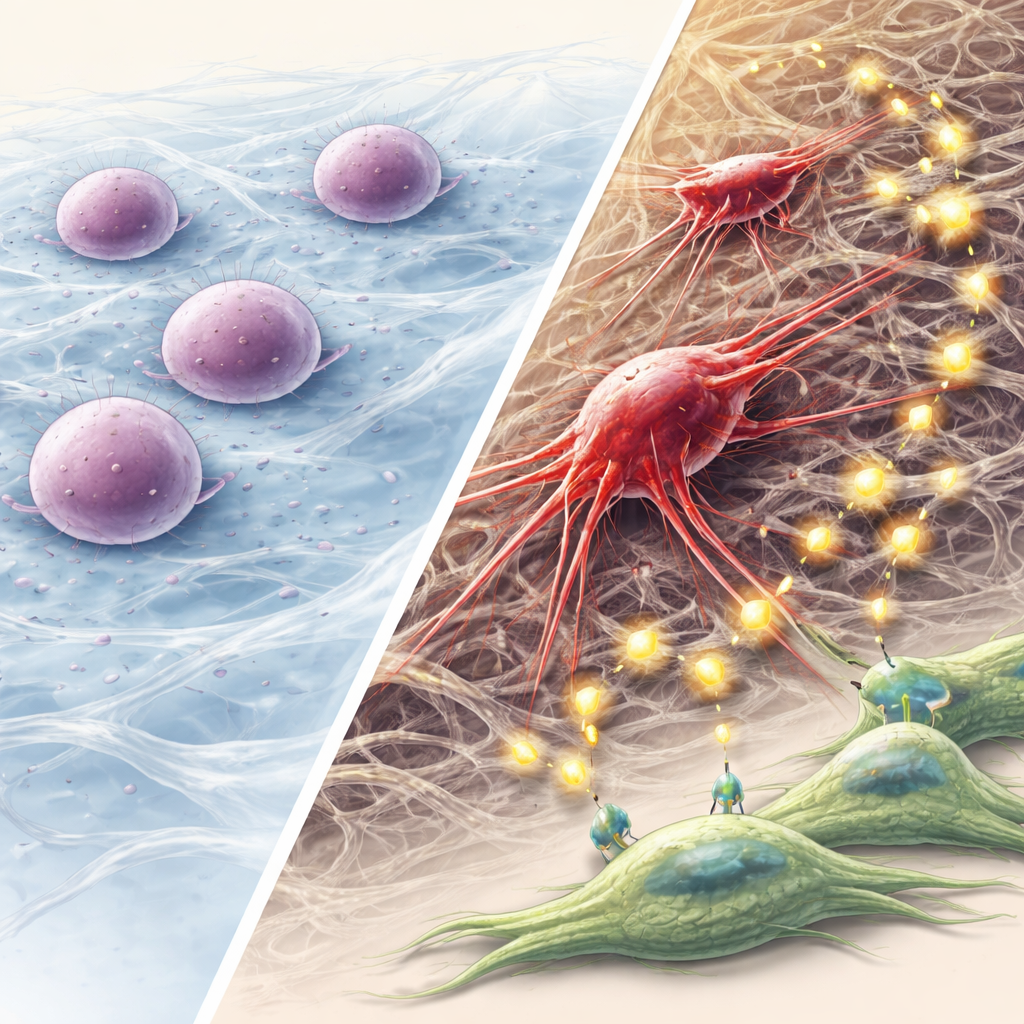
Agresif Kanser İçin Bu Mekanik Yol Neden Önemli
Bu çalışma adım adım bir model öneriyor: bir keratin füzyonu hücrenin iç iskeletini bozuyor, çekirdeği eziyor ve bir DNA hasarı alarmını tetikliyor; otofaji sonra birkaç hücrenin ölmek yerine uykuda kalmasına izin veriyor; zamanla bu hayatta kalanlar iskeletlerini yeniden düzenleyip kök hücreye benzeyen ve invazif özellikler kazanıyor ve veziküller ile FGF sinyali aracılığıyla çevrelerini yeniden şekillendiriyor. Uzman olmayanlar için ana mesaj, hücre içindeki fiziksel kuvvetler ve yapısal proteinlerin kanser evriminde genler ve kimyasallar kadar önemli olabileceğidir. Özellikle keratin füzyonları olan baş ve boyun kanserlerinde bu mekanik stres–otofaji–FGF yolunu hedeflemek, uykuda olan tümör hücrelerinin yeniden uyanmasını ve yayılmasını önlemek için yeni stratejiler sağlayabilir.
Atıf: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
Anahtar kelimeler: kanser kök hücre özellikleri, hücre sitoskeletonu, tümör uykuda kalma, baş ve boyun kanseri, mekanotransdüksiyon