Clear Sky Science · tr
TRIM21 aracılı HILPDA degradasyonu, PD‑L1 palmitoilasyonunu sınırlayarak meme kanserinde anti‑PD‑1 immünoterapi direncini aşar
Neden bazı kanser immünoterapileri etkisini kaybeder
Bağışıklık sistemini serbest bırakan ilaçlar, örneğin anti–PD‑1 tedavileri, agresif meme kanseri türleri de dahil olmak üzere birçok kanserin tedavisini dönüştürdü. Yine de birçok tümör ya hiç yanıt vermez ya da zamanla kaçış yolları geliştirir. Bu çalışma, üçlü negatif meme kanserinde böyle bir kaçış yolunu inceliyor ve tümör yağ metabolizmasının yeniden yönlendirilmesi ile yeniden kullanılmakta olan fenretinid adlı bir ilacın, standart immünoterapi işe yaramadığında bağışıklığın tekrar devreye girmesini nasıl sağlayabileceğini gösteriyor. 
Tümörleri koruyan gizli bir yardımcı
Araştırmacılar, hücrelerin stres altında yağları nasıl yönettiğiyle daha önce ilişkilendirilmiş az bilinen bir protein olan HILPDA’ya odaklandı. Anti‑PD‑1 tedavisine duyarlı kalan fare meme tümörlerini dirençli hale gelmiş tümörlerle karşılaştırarak, HILPDA düzeylerinin dirençli kanserlerde çok daha yüksek olduğunu buldular. Büyük hasta veri tabanları ve meme kanseri olan kadınlardan alınan tümör örneklerinin analizleri, HILPDA’nın normal meme dokusuna kıyasla tümörlerde, özellikle üçlü negatif hastalıkta, daha bol olduğunu ve tümörlerinde daha fazla HILPDA ifadesi olan hastaların genel olarak daha kötü çıktılara sahip olma eğiliminde olduğunu doğruladı. PD‑1 bloklayan ilaçlardan fayda görmeyen kişilerin tümörlerinde de daha fazla HILPDA vardı; bu da bu proteini doğrudan tedavi başarısızlığıyla ilişkilendiriyor.
Tümörler bağışıklık ortamını bize karşı nasıl çevirir
HILPDA’nın tümör içinde gerçekte ne yaptığını görmek için ekip, meme kanseri hücrelerini ya proteini aşırı üretecek ya da hiç üretemeyecek şekilde mühendislikledi ve ardından bunları insan bağışıklık hücreleriyle veya farelerde büyüttü. HILPDA yüksek olduğunda, tümörler düzenleyici T hücreleri, miyeloid kaynaklı baskılayıcı hücreler ve M2‑benzeri makrofajlar gibi saldırıyı azaltan ve kanserlerin gizlenmesine yardımcı olan bağışıklık hücre türlerini daha çok çekti. Aynı zamanda öldürücü CD8 T hücreleri ve doğal öldürücü hücrelerin sayısı ve etkinliği düştü ve toksik molekül salımı ile inflamatuar sinyal üretme yetenekleri zayıfladı. HILPDA susturulduğunda bu tablo tersine döndü: tümörlerde baskılayıcı hücreler azaldı, daha aktif öldürücü hücreler arttı, tümör büyümesi yavaşladı ve metastazlar azaldı. Kritik olarak, düşük HILPDA’lı tümörleri olan hayvanlara anti‑PD‑1 tedavisi uygulandığında tümörler daha çok küçüldü ve fareler daha uzun yaşadı; bu da HILPDA’nın immünoterapinin etkinliğini kontrol ettiğini gösteriyor.
Yağ üretimi, moleküler zırh ve bağışıklıktan kaçış
Daha derine indiklerinde, bilim insanları HILPDA’nın tümör metabolizmasını nasıl yeniden şekillendirerek bağışıklık savunmalarını güçlendirdiğini ortaya çıkardı. Kanser hücrelerinin içinde HILPDA, bir şaperon proteini olan HSP90’a bağlanarak yağ üretimini yönlendiren bir transkripsiyon faktörü KLF5’i stabilize ediyor. Bu üçlü, özellikle palmitat olmak üzere yağ asidi sentezini artırıyor ve tümör hücrelerini lipid damlacıklarıyla dolduruyor. Bu yağlardan biri daha sonra PD‑L1’e ekleniyor; PD‑L1 tümör yüzeyinde bulunan ve bağışıklık hücrelerine "saldırmayın" sinyali gönderen kontrol noktası proteinidir. Ekip, PD‑L1’e özgü bir noktaya palmitat eklemenin moleküler bir tutkal gibi davrandığını; PD‑L1’in hücre zarında kararlı durmasına yardımcı olduğunu ve yıkımının önlendiğini gösterdi. Bu tek bağlanma bölgesinin mutasyona uğratılması, HILPDA bol olsa bile PD‑L1’in kararlılığını elinden alıyor ve kanser hücrelerini koruma yeteneğini zayıflatıyor. Başka bir deyişle, HILPDA kaynaklı yağ üretimi, PD‑L1 üzerinde tümörün bağışıklık kalkanını inceden sağlam çeliğe çeviren kimyasal bir ince ayarı besliyor.
Bastırılabilecek yerleşik fren
Her hızlandırıcının bir freni vardır ve burada fren TRIM21 adlı başka bir proteindir. Yazarlar TRIM21’in HILPDA’yı tanıdığını ve onu hücrenin imha mekanizmasına gönderen moleküler "etiketlerle" işaretlediğini keşfettiler. Hastalardaki meme tümörlerinde, HILPDA yüksek olduğunda TRIM21 düzeyleri genellikle düşük eğilim gösteriyordu ve düşük TRIM21 kötü sonuçlarla ilişkilendirildi; bu durum, bu doğal frenleme sisteminin kanserde sıklıkla zayıfladığını düşündürüyor. Ekip ardından TRIM21’i güçlendirebilecek ilaçları aradı ve insanlarda zaten denenmiş bir retinoid olan fenretinidi tespit etti. Üçlü negatif meme kanserinin hücre ve hayvan modellerinde fenretinid, TRIM21 aktivitesini artırdı, HILPDA’nın yıkımını hızlandırdı, yağ sentezini ve PD‑L1’in koruyucu modifikasyonunu azalttı ve tümör büyümesi ile yayılmasını yavaşlattı. En çarpıcı olanı, fenretinid ile anti‑PD‑1 tedavisinin birleştirilmesinin tümörleri bağışıklık saldırısına karşı daha savunmasız hale getirmesi; tümör mikroçevresinde öldürücü T ve doğal öldürücü hücreleri artırırken baskılayıcı hücreleri azalttığı görüldü. 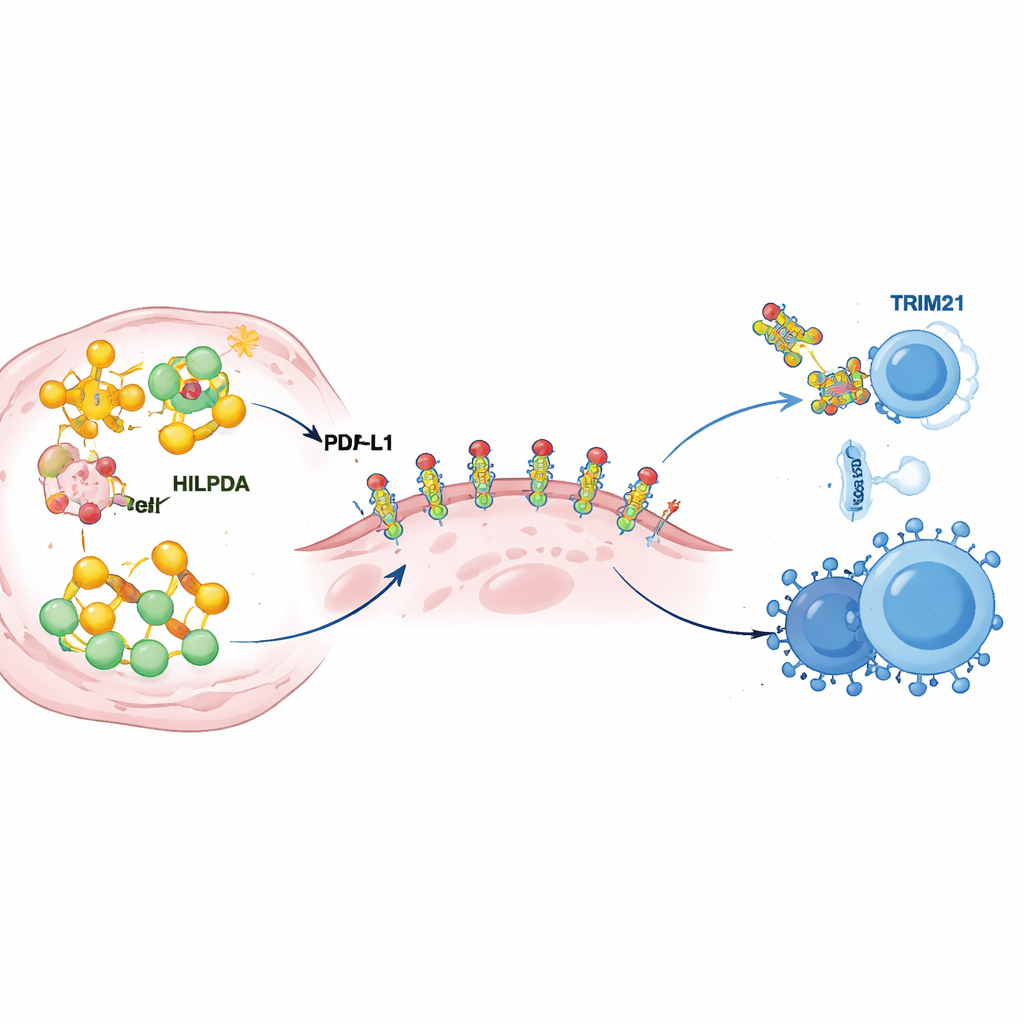
Gelecekteki kanser bakımına etkisi
Bu çalışma, stres altındaki meme kanseri hücrelerinin HILPDA’yı artırıp yağ üretimini hızlandırdığı ve yüzeylerindeki PD‑L1’i kimyasal olarak güçlendirerek PD‑1’i bloke eden ilaçlara rağmen bağışıklık hücrelerini baskılamaya devam etmelerini sağlayan bir olay zincirini ortaya koyuyor. TRIM21, HILPDA’yı parçalayabilen içsel bir güvenlik mekanizması görevi görüyor, ancak tümörlerde genellikle çok zayıf kalıyor. Fenretinidin bu güvenlik mekanizmasını yeniden etkinleştirebildiğinin bulunması, metabolik bir ilacı mevcut immünoterapi ile birleştirerek direncin üstesinden gelmeye yönelik pratik bir yol öneriyor. Klinik deneylerle doğrulanırsa TRIM21–HILPDA–PD‑L1 eksenini hedef almak, tedavisi zor üçlü negatif meme kanseri olan hastalara immün temelli tedavilerden fayda sağlama konusunda ikinci bir şans verebilir.
Atıf: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
Anahtar kelimeler: üçlü negatif meme kanseri, immünoterapi direnci, PD‑L1 palmitoilasyonu, tümör yağ metabolizması, fenretinid