Clear Sky Science · tr
Cereblon (CRBN), 6-fosfoglukonat dehidrogenaz (6PGD) enzimini olumsuz düzenleyerek prostat kanseri metastazını engeller
Bu araştırma neden önemli
Prostat kanseri prostat dışına diğer organlara yayıldığında tedavisi çok daha zorlaşır ve sıklıkla ölümcüldür. Bu çalışma, az bilinen bir hücresel “kalite kontrol” proteini olan cereblon’un (CRBN), agresif davranışı besleyen bir metabolik enzimi yok ederek prostat kanserinin yayılmasını nasıl engellediğini ortaya koyuyor. Bu doğal fren sistemini anlamak, özellikle tedavisi zor hastalık biçimlerinde metastazı yavaşlatma veya durdurma yolları için yeni yaklaşımlar öneriyor.
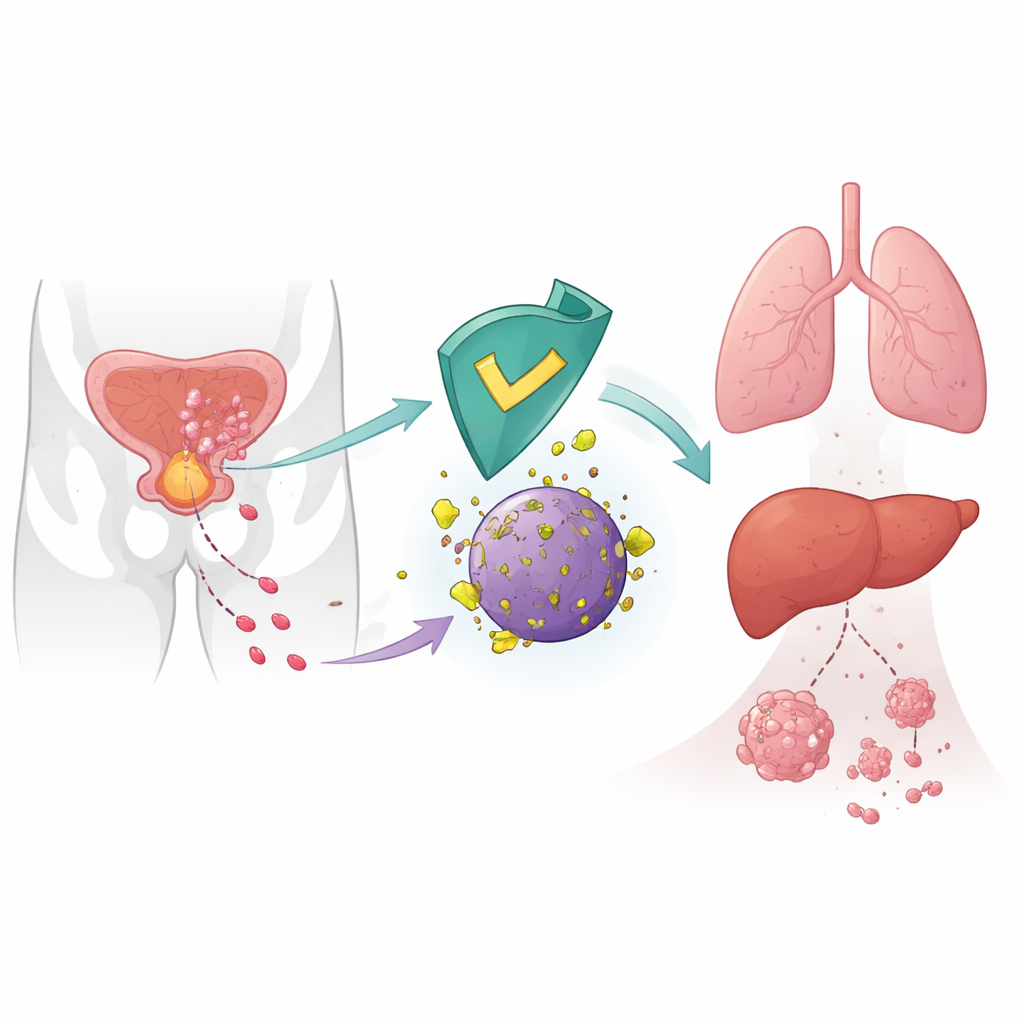
Kanser yayılımına karşı içsel bir fren
Kanser hücreleri rastgele yayılmaz; hareket etmek, istila etmek ve uzak organları kolonize etmek için iç mekanizmalarını yeniden düzenlerler. Yazarlar, en çok kan hastalıklarında kullanılan talidomid benzeri ilaçların hedefi olarak bilinen CRBN proteinine odaklandı. Sağlıklı hücrelerde CRBN, belirli proteinleri yıkım için işaretleyen moleküler bir bertaraf ünitesinin parçasıdır. Önceki çalışmalar tümörlerde düşük CRBN seviyelerinin daha kötü sonuçlarla ilişkili olabileceğine işaret etmişti, ancak doğrudan metastazdaki rolü belirsizdi. Bu çalışmada araştırmacılar, CRBN’nin prostat kanseri yayılımını bastıran doğal bir unsur olarak 6-fosfoglukonat dehidrogenaz (6PGD) adlı metabolik enzimi parçalayarak hedef aldığını gösteriyor.
Kanserin ele geçirdiği bir metabolik motor
6PGD, hücrelerin hem yapı taşları hem de antioksidan güç sağlayan NADPH üretmesine yardımcı olan oksidatif pentoz fosfat yolunda yer alır. Pek çok tümör bu yolu hızlandırarak daha hızlı büyür ve strese dayanır. Araştırma ekibi, hasta prostat kanseri örneklerinin normal prostat dokusuna göre genellikle daha az CRBN ve daha fazla 6PGD içerdiğini ve bu dengesizliğin özellikle agresif hastalıkta belirgin olduğunu buldu. Prostat kanseri hücre hatlarında CRBN’un susturulması veya tasarım bir bileşikle parçalanması 6PGD protein düzeylerini ve enzim aktivitesini artırarak NADPH’yi yükseltti. CRBN’in geri getirilmesi ters etki yaptı; 6PGD ve NADPH düştü fakat 6PGD gen mesajında değişiklik yoktu, bu da kontrolün protein düzeyinde olduğunu gösterdi.
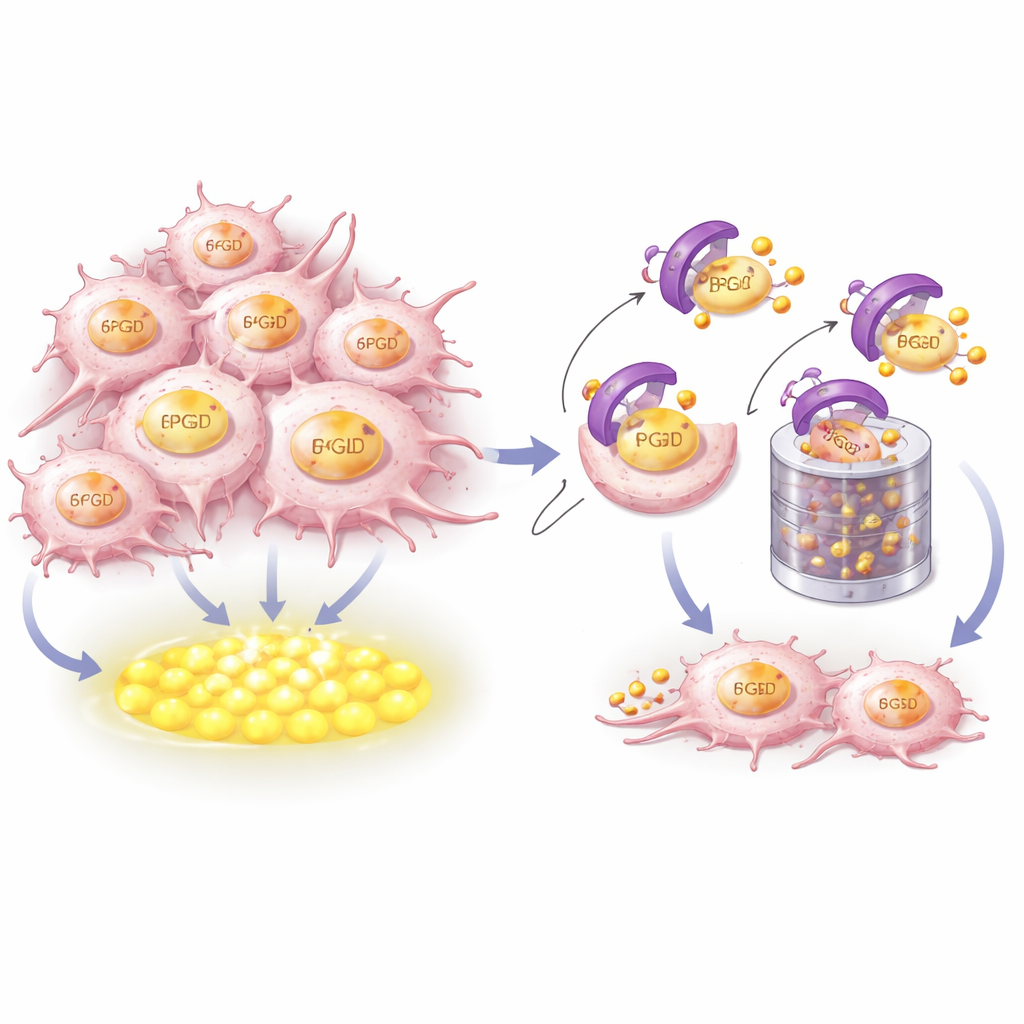
CRBN yakıt kaynağını nasıl tanır ve yok eder
CRBN’in 6PGD’yi nasıl kontrol ettiğini anlamak için araştırmacılar yapısal modelleme ile biyokimyasal deneyleri birleştirdi. CRBN’nin fiziksel olarak 6PGD’nin kuyruk ucuna yakın, kısa ve yüksek oranda korunmuş bir helikal segmenti yakaladığını gösterdiler. Her iki proteindeki kilit aminoasitler sıkı bir kenetlenme arayüzü oluşturuyordu. Bu temas noktaları değiştirildiğinde CRBN artık 6PGD’ye bağlanamıyor, yıkım için işaretleyen küçük ubiquitin etiketlerini takamıyor ya da onu proteazom olarak bilinen hücresel öğütücüye gönderemiyordu. Önemli olarak, bu tanıma yüzeyi CRBN’ye bağlanan immünomodülatör ilaçların bağlandığı cebin ayrı bir alanındaydı; bu da CRBN’nin 6PGD üzerindeki kontrolünün ilaç kaynaklı bir etki değil, doğal ev içi bakım rolünün bir parçası olduğunu gösteriyor.
Değişmiş metabolisandan göç eden hücrelere
Bu moleküler el sıkışmasının sonuçları hücre davranışı düzeyinde ortaya çıkıyor. CRBN eksikliği olan prostat kanseri hücrelerinde artmış 6PGD ve NADPH, yapay bariyerler üzerinden artmış hareket ve istila ile birlikteydi; bunlar metastatik potansiyelin ayırt edici özellikleridir. CRBN fazla üretildiğinde hücreler daha az hareketli ve invazif hale geldi, büyüme hızları değişmese bile. Gen aktivite profillemesi CRBN’in sıkı paketlenmiş epitel hücrelerle ilişkili CDH1 düzeylerini yükselttiğini ve doku parçalanması ile göçle ilişkili MMP1 düzeylerini düşürdüğünü gösterdi. Önemli olarak, bu değişimler doğrudan CRBN–6PGD bağlanmasını gerektiriyordu ve 6PGD’nin enzim aktivitesini engelleyerek geri çevrilebiliyordu; bu, metabolizmada değişikliklerin metastatik davranış değişikliklerine bağlandığını destekliyor.
Hayvan modelleri ve diğer kanserlerden kanıtlar
Araştırma ekibi bu fikirleri, prostat kanseri hücrelerini farelerin kan dolaşımına veya dalaklarına enjekte ederek test etti. Fazladan CRBN üreten hücreler, kontrol hücrelerine göre karaciğer ve akciğerde çok daha az metastatik nodül oluşturdu; bu, canlı hayvanlarda anti-metastatik rolü doğruladı. CRBN’den yoksun farelerde birkaç organda 6PGD protein düzeyleri daha yüksekti. Glioblastoma, akciğer ve böbrek kanseri hücre hatlarında benzer desenler görüldü: CRBN’in çıkarılması 6PGD’yi artırdı ve hücre hareketi ile istilasını hızlandırdı; genetik veya ilaçla 6PGD inhibisyonu ise bu agresif davranışı engelledi. Bu gözlemler CRBN–6PGD freninin yalnızca prostat kanserine özgü olmadığını düşündürüyor.
Gelecekteki tedaviler için ne anlama gelebilir
Genel olarak çalışma, CRBN’in kanser hücrelerinin gevşemesi, göç etmesi ve yeni tümörler tohumlaması için gereken enerji kaynağını sınırlayan bir metabolik kapı bekçisi olarak görev yaptığını öne sürüyor. CRBN kaybolduğunda veya düşük olduğunda 6PGD birikir, NADPH üretimi artar ve hücreler metastazı destekleyen değişikliklere daha yatkın hale gelir. Hastalar açısından bu iki olasılığa işaret ediyor: CRBN ve 6PGD düzeylerinin ölçülmesi yüksek metastatik risk taşıyan tümörleri işaretleyebilir ve CRBN işlevini artıran—veya CRBN düşük tümörlerde seçici olarak 6PGD’yi baskılayan—tedaviler prostat ve diğer kanserlerin yayılmasını yavaşlatmak veya önlemek için yeni yollar sunabilir.
Atıf: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
Anahtar kelimeler: prostat kanseri metastazı, kanser metabolizması, cereblon, 6PGD enzimi, NADPH yolak