Clear Sky Science · tr
L1TD1, ABCC3 mRNA stabilitesini artırarak kolorektal mukinöz adenokarsinom ilerlemesini teşvik eder
Bu yoğun mukuslu kanser neden önemli
Kolorektal kanser dünya çapında kanser ölümlerinin önde gelen nedenlerinden biridir. İçinde, tümör kütlesinin yarısından fazlasını kalın mukusun oluşturduğu mukinöz adenokarsinom adı verilen özel bir alt tip öne çıkar. Bu sümüksü bariyer, kanser hücrelerinin kemoterapiden ve vücudun savunma mekanizmalarından saklanmasına yardımcı olabilir. Bu çalışma temel ama hayati bir soruyu soruyor: bu büyük mukus üretimini ne kontrol ediyor ve onu kapatarak kanseri yavaşlatıp tedavilerin etkinliğini artırabilir miyiz?
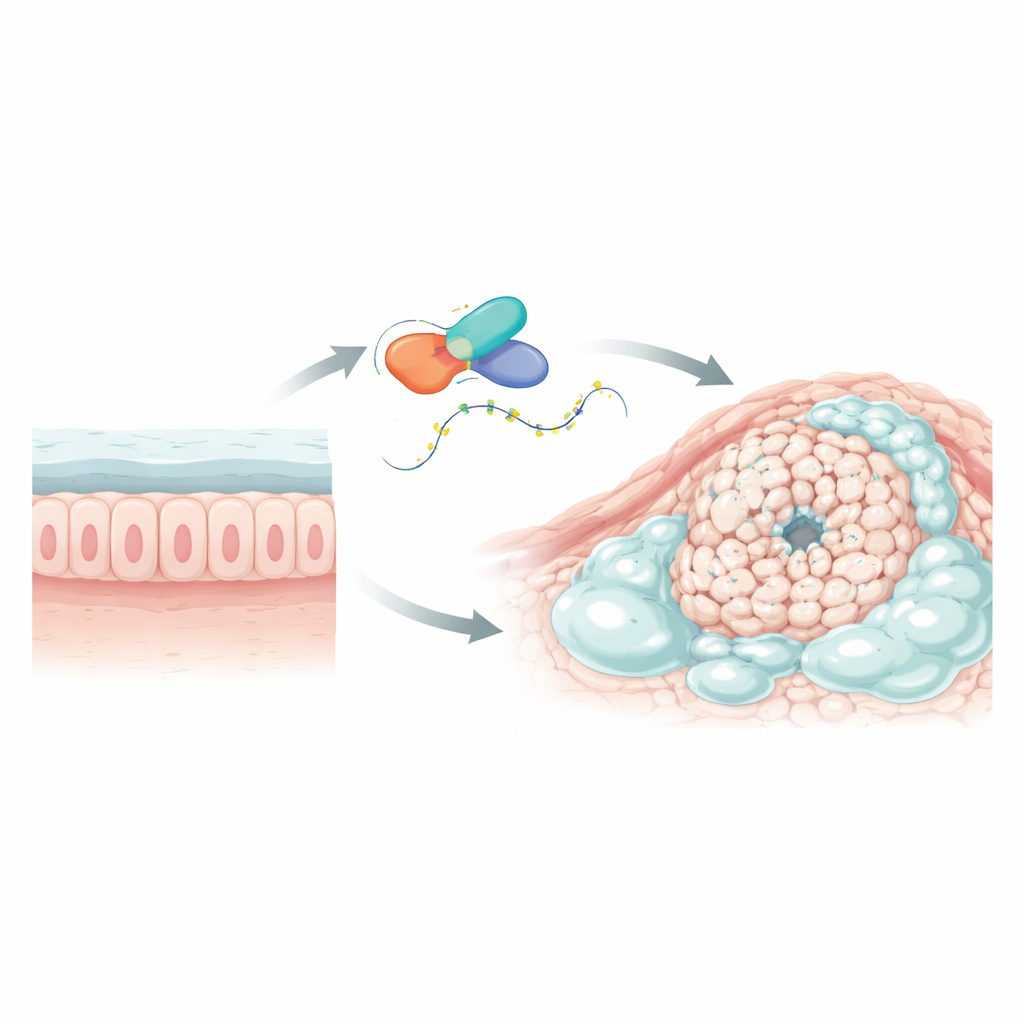
Soruna yol açan anahtar bir genin bulunması
Araştırmacılar önce büyük kanser veri tabanları ve tek hücre dizileme verilerini tarayarak mukus açısından zengin kolorektal tümörlerde normal kolorektal kanserlere ve çevreleyen sağlıklı dokuya kıyasla farklı davranan genleri saptadılar. L1TD1 adındaki bir gen belirgin biçimde öne çıktı. Mukinöz tümörlerde keskin şekilde artmıştı, sıradan tümörlerde değil ve tümör dokusunda çevreleyen normal bağırsağa göre daha yüksekti. L1TD1, DNA’dan hücrenin protein yapım makinesine genetik mesajları taşıyan RNA’ya bağlanan bir protein şifreliyor. RNA’ya bağlanan proteinler mesajların ne kadar süre yaşadığını ve ne kadar yoğun okunduğunu ince ayarlayabildiği için L1TD1, bu mukus yüklü kanserlerde ana düzenleyici rolü oynayabilecek güçlü bir aday olarak göründü.
L1TD1’in kanser büyümesini ve yayılmasını nasıl desteklediği
L1TD1’in gerçekte ne yaptığını test etmek için ekip kolon kanseri hücre hatları ve fare modellerine yöneldi. Kanser hücrelerinde L1TD1 düzeylerini artırdıklarında hücreler daha hızlı çoğaldı, daha kolay hareket etti ve doku benzeri bariyerleri daha agresif şekilde aştı. L1TD1’i azaltmak ters etki yaptı; büyüme yavaşladı ve invazyon azaldı. L1TD1 yüksek hücrelerle enjekte edilen farelerde tümörler daha büyük büyüdü ve karaciğer ile karın boşluğuna daha sık yayıldı. Hastalarda daha fazla L1TD1 taşıyan tümörler genellikle daha büyük, daha iyi farklılaşmamış ve daha ileri evrelerde olma eğilimindeydi; bu da bu geni klinikte daha kötü hastalık davranışıyla ilişkilendiriyor.
Mukusu ve ilaç direncini açmak
Mukus, L1TD1’in etkisinin merkezinde yer aldı. Daha fazla L1TD1 içeren hücreler özellikle MUC2 ve MUC5AC olmak üzere temel mukus oluşum proteinlerini daha yüksek miktarda üretti ve bağırsak mukus salgılayan normal goblet hücrelerinin özelliklerini gösterdi. Üç boyutlu kültürler ve hem hasta hem de fare dokularındaki boyamalar, daha yüksek L1TD1 ile daha kalın ve daha bol mukus arasında bir ilişkiyi doğruladı. Önemli olarak, bu mukus sadece yan bir ürün değildi. Araştırmacılar seçici olarak MUC2’yi azalttıklarında, L1TD1’in yol açtığı ekstra büyüme, invazyon ve kemoterapi direnci büyük ölçüde ortadan kalktı. L1TD1 bakımından zengin hücreler yaygın olarak kullanılan oksaliplatin ile öldürülmesi daha zor hücrelerdi ve bu hücreleri taşıyan tümörler tedavi edilen farelerde daha az küçüldü; bu da mukusun L1TD1’in inşa etmeye yardım ettiği bir kalkan olduğunun altını çiziyor.
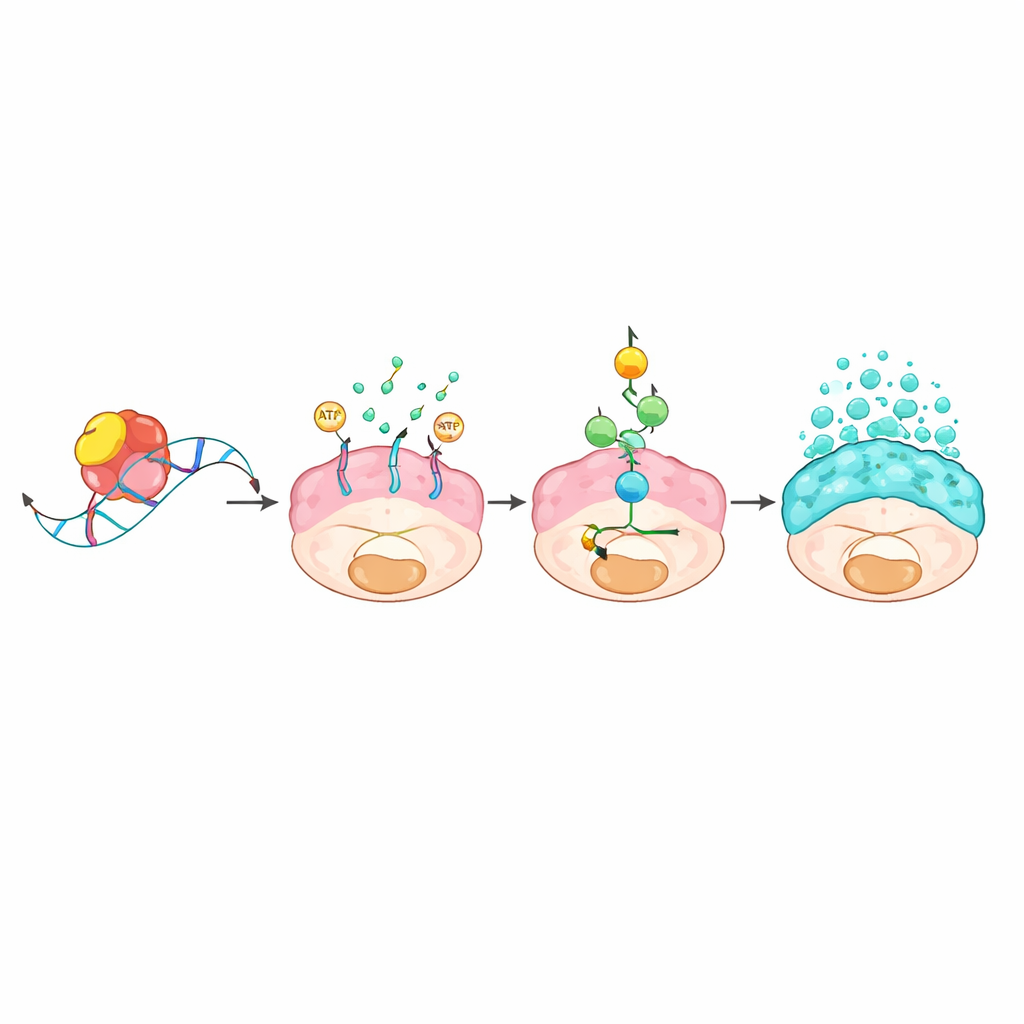
RNA kontrolünü mukus taşkınlarına bağlayan moleküler zincir
Ekip bir RNA-bağlayıcı proteinin nasıl bu kadar dramatik değişikliklere yol açabileceğini merak etti. L1TD1’e fiziksel olarak bağlı RNA moleküllerini ayıklayıp L1TD1 varken ve yokken gen aktivitesini karşılaştırarak ABCC3 adlı bir taşıyıcı genini birincil hedef olarak belirlediler. L1TD1, ABCC3’ün RNA mesajının kuyruk bölgesindeki kısa "GUGU" motifi üzerine tutunarak mesajı stabilize etti ve hücrenin daha fazla ABCC3 proteini (MRP3 olarak bilinen) üretmesine neden oldu. Bu taşıyıcı hücre zarında yer alır ve maddeleri hücre dışına pompalamak için enerji tüketir. Ortaya çıkan enerji tüketimi, AMPK sensörü merkezli bir metabolik alarm sistemini etkinleştirdi ve bu da klasik bir büyüme ve stres yolu olan MAPK’yi açtı. Bir kez etkinleşince bu kaskad, mukus proteinlerinin üretimini ve salınımını artırdı ve kanser hücrelerinin büyüme, göç ve ilaç direncini güçlendirdi. ABCC3’ü genetik olarak ya da deneysel bir bileşikle bloke etmek veya MAPK yolunu inhibe etmek, mukus üretimini azalttı ve tümörleri zayıflattı.
Bu hastalar için ne anlama geliyor
Bir araya getirildiğinde, çalışma mukuslu kolorektal kanser için adım adım bir kontrol sistemini ortaya koyuyor: L1TD1 ABCC3’ün RNA’sını stabilize ediyor, ABCC3 hücresel enerjiyi tüketiyor, AMPK–MAPK yolu devreye giriyor ve tümör buna mukus aşırı üretimi ve daha agresif, ilaç dirençli bir cevapla karşılık veriyor. Hastalar için bu birkaç umut verici açı öneriyor. L1TD1 ve ABCC3 düzeyleri, kötü davranma veya standart kemoterapiye direnç gösterme olasılığı yüksek tümörleri işaretleyebilir. Daha da önemlisi, L1TD1–ABCC3 etkileşimini bozan ilaçlar, MRP3 pompa aktivitesini bloke eden bileşikler veya aşağı akış sinyal yolunu hedefleyen tedaviler mukus bariyerini inceltebilir, tümör büyümesini yavaşlatabilir ve bu zorlu kolorektal kanser formunda mevcut tedavilerin etkinliğini artırabilir.
Atıf: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
Anahtar kelimeler: mukinöz kolorektal kanser, L1TD1, ABCC3 MRP3, mukus üretimi, kemorezistans