Clear Sky Science · tr
PMM2, E2F4’ü işe çekmek için TRIM28 ile etkileşir ve KIFC3 aracılı tümör glikolizini ve kolorektal kanser ilerlemesini teşvik eder
Bu Kanser Hikâyesi Neden Önemli
Kolorektal kanser, dünya genelinde en ölümcül kanserlerden biridir; bunun bir nedeni birçok tümörün kontrolsüz büyümeyi beslemek için vücudun enerji sistemlerini ele geçirmeyi öğrenmesidir. Bu çalışma, PMM2 adındaki az bilinen bir enzimin kolorektal tümörlerin şekeri daha agresif şekilde yakmasına ve yayılmasına nasıl yardımcı olduğunu ve bunun neden gelecekteki ilaçlar ve tanı testleri için umut verici bir hedef oluşturduğunu ortaya koyuyor.
Şekere Aç Bir Tümör Motoru
Kanser hücreleri sıklıkla glukoz kullanım biçimlerini yeniden düzenleyerek yüksek hızlı, düşük verimli bir şeker yakımı biçimi olan glikolizi tercih ederler. Araştırmacılar kolorektal tümör örneklerindeki binlerce geni yakın sağlıklı doku ile karşılaştırarak işe başladılar. Proteinlere şeker zincirleri bağlanmasında genellikle görevli olan PMM2, kanserde en güçlü artış gösteren genlerden biri olarak öne çıktı. Fazladan PMM2 taşıyan tümör hücreleri daha hızlı büyüdü, daha çok koloni oluşturdu ve laboratuvar kaplarında daha kolay yayıldı; PMM2 kapatılan hücreler ise büyümelerini yavaşlattı, daha az göç etti ve daha kolay ölüme yatkın hale geldi.
Tümör Hücreleri Şekeri Nasıl Hızlandırıyor
Araştırma ekibi kolorektal kanser hücrelerinde PMM2 düzeylerini azalttıklarında hücrelerin daha az glukoz aldığını, daha az ATP (ana enerji para birimleri) ürettiğini ve glikolizin atık ürünü olan daha az laktat saldıklarını gözlemledi. Hassas metabolik ölçümler çevreleyen ortamın genel asitleşmesinin düştüğünü, oksijen kullanımının ise arttığını doğruladı; bu da hücrelerin turbo beslemeli glikolizden daha normal solunuma kaydığını gösteriyor. Kritik glikoliz yardımcı proteinleri PKM2 ve LDHA da azaldı. Sürpriz bir şekilde, katalitik olarak “ölü” bir PMM2 versiyonu bile bu şekere aç davranışı tetikleyebiliyordu; bu da enzimin kanserdeki rolünün klasik kimyasıyla değil, hücre içinde kime bağlandığıyla ilgili olduğunu gösteriyor.
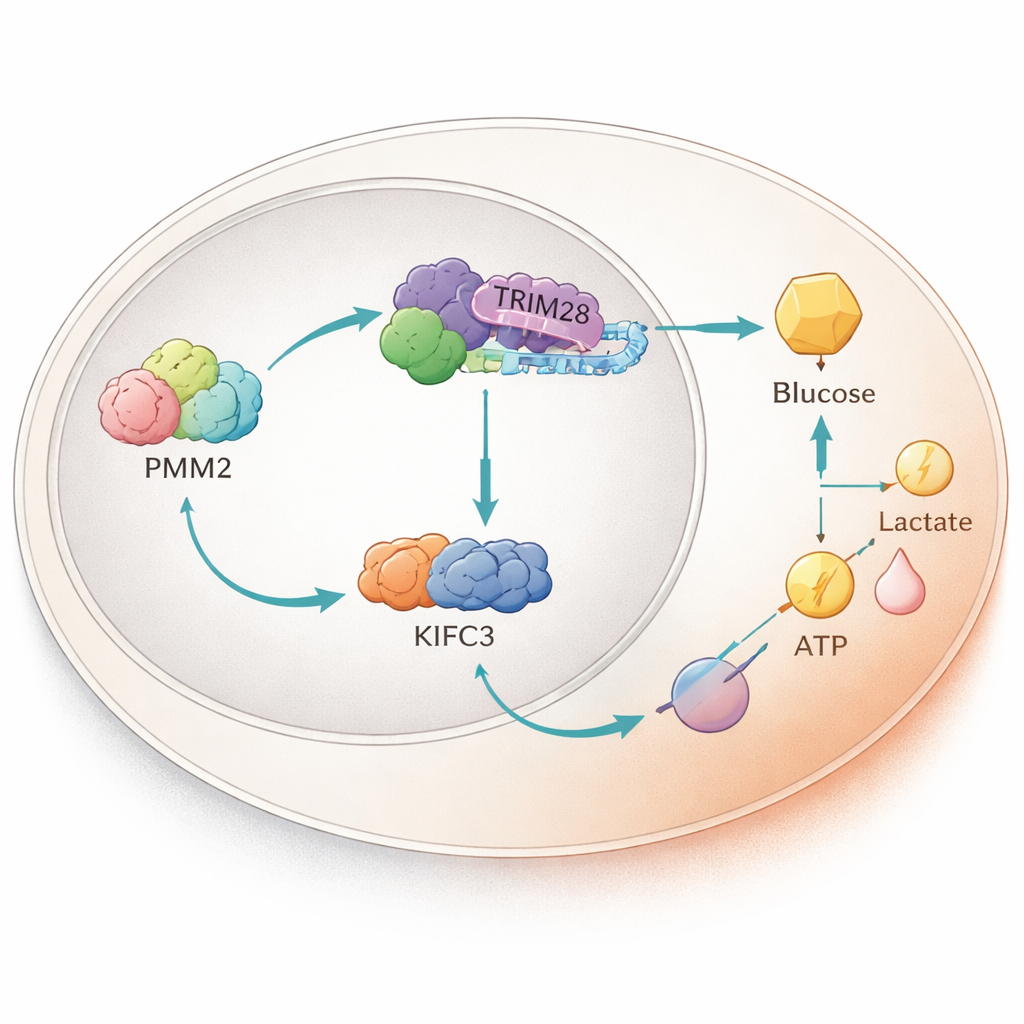
Çekirdek İçinde Bir Protein Rölesi
Daha derine indiklerinde bilim insanları PMM2’nin TRIM28 adlı başka bir proteine fiziksel olarak bağlandığını buldular; TRIM28 çekirdeğe geçebilen ve gen aktivitesini etkileyebilen bir protein. PMM2, TRIM28’in çekirdekte birikmesine yardımcı oluyor; burada TRIM28, E2F4 adlı bir transkripsiyon faktörüyle ortaklık kuruyor. Bu üçlü, KIFC3 adındaki bir motor proteinin üretimini, KIFC3’ün DNA kontrol bölgesindeki belirli bir parçaya bağlanarak artırıyor. PMM2’nin TRIM28 bağlanması için gereken bölgesini sildiren deneyler, PMM2’nin glikolizi ve hücre büyümesini artırma yeteneğini ortadan kaldırdı; bu da tümör avantajını sağlayanın PMM2’nin klasik enzim işlevi değil, bu protein ortaklığı olduğunu vurguluyor.
Önemli Bir Metabolik Anahtarı Açmak
Hücrenin iç iskeleti boyunca yük taşıma rolüyle daha çok bilinen KIFC3, önemli bir metabolik anahtar çıktı. Araştırmacılar KIFC3 düzeylerini düşürdüklerinde kolorektal kanser hücreleri daha az glukoz tüketti, daha az ATP ve laktat üretti ve daha zayıf glikolitik aktivite gösterdi; oksijen kullanımları ise arttı. Önemli olarak, KIFC3 sansı PMM2’nin normalde sağladığı glikoliz artışı ve büyüme avantajını kısmen iptal etti. İnsan kolorektal kanser hücreleri implante edilen farelerde, fazladan PMM2 taşıyan tümörler daha büyük büyüdü; ancak KIFC3 bastırıldığında bu etki zayıfladı. Bu hayvanlardaki tümör örnekleri daha yüksek PMM2, KIFC3 ve glikoliz belirteci seviyeleri göstererek olay zincirinin canlı dokuda da bir araya geldiğini ortaya koydu.
Laboratuvar Modellerinden Hasta Örneklerine
Çalışmayı kliniğe yaklaştırmak için ekip, hastalardan alınan kolorektal kanserlerden mini üç boyutlu tümörler (organoidler) oluşturdu. Daha yüksek PMM2 ve KIFC3 düzeylerine sahip organoidler, daha düşük düzeyli olanlara kıyasla daha hızlı büyüdü ve daha fazla ATP ile laktat üretti. Organoidlerde PMM2’yi zorlayarak artırmak KIFC3 ve glikolizi yükseltirken, PMM2’yi azaltmak ters etkiyi gösterdi. Hasta tümör dizilerinin analizleri ayrıca yüksek PMM2 seviyelerinin daha ileri hastalık, lenf nodu yayılımı ve daha kısa genel sağkalım ile ilişkili olduğunu gösterdi; bu da PMM2’yi güçlü bir aday biyobelirteç olarak işaretliyor.
Gelecekteki Bakım İçin Anlamı
Basitçe söylemek gerekirse, bu çalışma birçok kolorektal tümörün PMM2’yi TRIM28 ve E2F4 üzerinden çekirdek içi bir protein rölesine bağlayarak KIFC3’ü ve dolayısıyla şekeri yakma mekanizmalarını yükselttiğini gösteriyor. Bu metabolik sıçrama kanserlerin büyümesine ve yayılmasına yardımcı oluyor. Bu yol PMM2’nin geleneksel enzim görevinden çok protein etkileşimlerine bağlı olduğundan, tedavi için yeni fırsatlar açıyor: PMM2’nin TRIM28’e bağlanmasını bozan küçük moleküller, peptitler veya degrader ilaçlar; E2F4’ün DNA’ya erişimini engelleyen yaklaşımlar; ya da KIFC3 aktivitesini azaltan ajanlar prensipte tümörleri tercih ettikleri yakıttan mahrum bırakabilir. Bu tür tedaviler henüz mevcut olmasa da PMM2–TRIM28–E2F4–KIFC3 zinciri artık kolorektal kanserle mücadelede daha hedefe yönelik ve metabolizma odaklı stratejiler için umut verici bir yol haritası olarak öne çıkıyor.
Atıf: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
Anahtar kelimeler: kolorektal kanser, tümör metabolizması, glikoliz, onkogenik sinyalizasyon, biyobelirteç