Clear Sky Science · tr
ULK1, deneysel epitelyal over kanseri modellerinde metastatik ilerlemeyi teşvik ediyor
Bu araştırma neden önemli
Epitelyal over kanseri genellikle karın içinde sessizce yayıldıktan sonra keşfedilir ve bu yüzden kadınları etkileyen en ölümcül kanserlerden biridir. Bu yayılmanın kilit adımlarından biri, karın sıvısında yüzen, kemoterapiye dayanabilen ve yeni tümörleri tohumlayabilen küçük tümör hücre kümeleri olan sferoidlerin oluşmasıdır. Bu çalışma, sonuçları büyük olabilecek odaklı bir soruyu ele alıyor: ULK1 adı verilen hücresel bir “hayatta kalma anahtarı” bu kümelerin dayanmasına ve yayılmasına yardımcı oluyor mu ve onu kapatmak ileri evre over kanserini tedavi etmenin yeni yollarını açabilir mi?
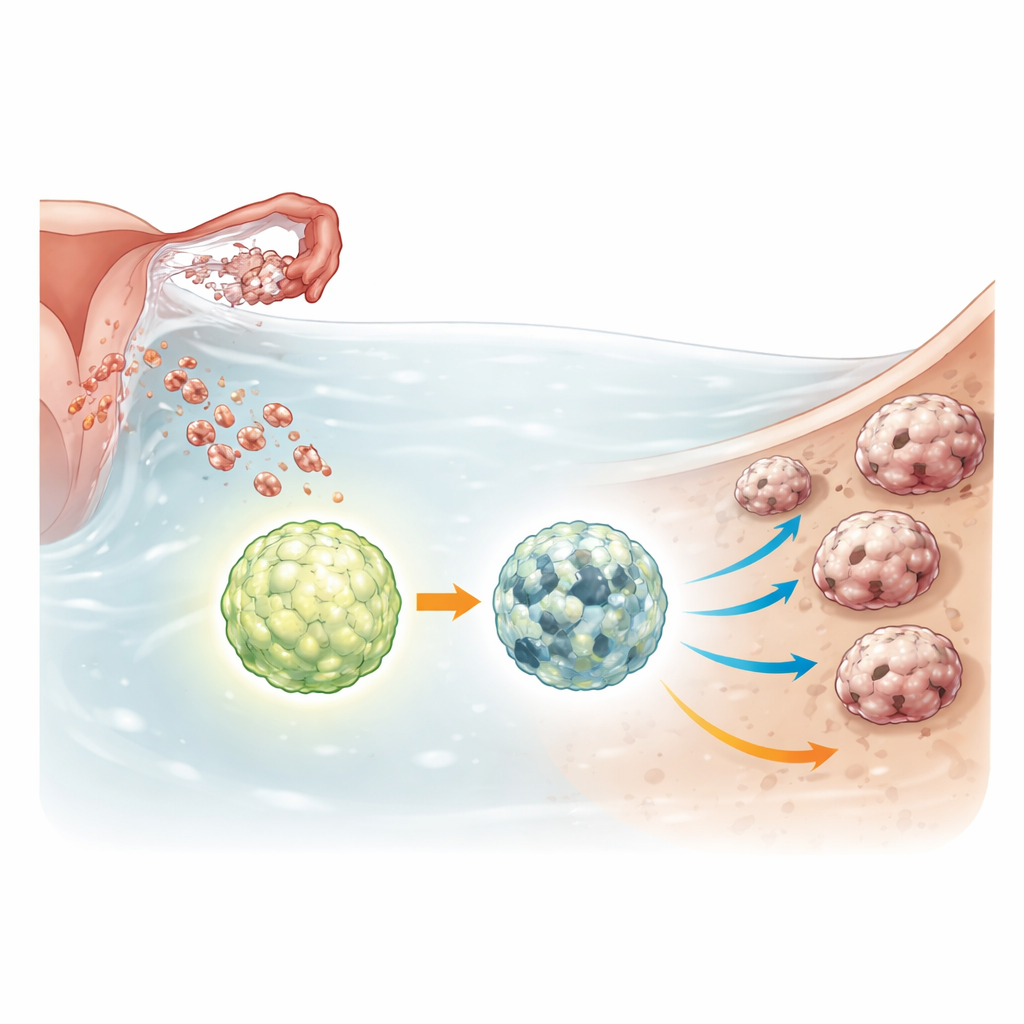
Tümör hücresi kümelerinin içindeki bir hayatta kalma anahtarı
Over kanseri sferoidleri düşük besin, yapışma eksikliği ve kemoterapi maruziyeti gibi zorlu koşullara dayanmak zorundadır. Bununla başa çıkmak için, hücreler iç bileşenleri parçalayarak ve yeniden kullanarak stresteki hücreleri canlı tutan otofaji olarak bilinen bir geri dönüşüm sürecini artırır. ULK1 bu geri dönüşüm sistemini açan ana kontrol noktasıdır. Araştırmacılar, birkaç over kanseri hücre hattından ve erken, kanser öncesi evreleri temsil eden kansersiz bir tüp (fallop tüpü) hücre hattından ULK1’i tamamen kaldırmak için gen düzenleme araçları kullandılar. Ardından, normal ve ULK1 eksik hücrelerin serbest yüzen sferoidler veya organoid adı verilen üç boyutlu mini-tümörler olarak yetiştirildiğinde nasıl davrandığını karşılaştırdılar.
Anahtar kapatıldığında ne oluyor
Over kanseri hücrelerinde ULK1 silindiğinde, sferoidlerde otofajiyi gerçekleştirme yetenekleri belirgin şekilde bozuldu; bu, kilit geri dönüşüm proteinlerindeki değişikliklerle gösterildi. Bu ULK1 eksik sferoidlerde daha az canlı hücre bulundu ve artan programlı hücre ölümü işaretleri görüldü; bu da kanser kümelerinin artık stresli koşullarla eskisi kadar iyi başa çıkamadığını gösteriyor. İlginç olarak, kansersiz öncü hücrelerden ULK1’in çıkarılması geri dönüşüm sistemini aynı derecede kapatmadı; bu durum kanser hücrelerinin sağlıklı hücrelere göre ULK1’e daha bağımlı olduğunu düşündürüyor. Bu kanser-spesifik bağımlılık ULK1’i çekici bir terapötik hedef haline getiriyor.
Yayılmayı yavaşlatmak ve tümör yerleşimlerini zayıflatmak
Süspansiyon halinde hayatta kalmanın ötesinde, sferoidlerin yeni tümörler oluşturmak için karın boşluğunun düz astarına tutunup burada invaze etmesi gerekir. Metastazın bu erken adımını taklit eden laboratuvar modelleri kullanılarak, ULK1 eksik sferoidlerin normalde karın organlarını kaplayan mezotelyal hücre katmanını itmeme ve içine girme konusunda belirgin şekilde daha kötü olduğu gösterildi. Jelleşmiş bir matrikse gömülü organoidler olarak büyütüldüğünde, ULK1 eksik kanser hücreleri daha küçük ve daha zayıf tümör yapıları oluşturdu. İnsan over kanseri hücrelerinin karın boşluğuna enjekte edildiği fare modellerinde ise ULK1 kaybı daha az tümör odağı ve daha az sıvı birikimine yol açtı; bunlar ileri hastalığın tipik işaretleri olmakla birlikte, hayvanların genel sağkalımı iyileşmedi.
Anahtar sinyalleri zayıflatmak ve hedefe yönelik ilaç etkilerini artırmak
ULK1’in yalnızca geri dönüşüme nasıl destek verdiğini anlamak için araştırmacılar ULK1 eksik sferoidlerde protein değişikliklerini haritaladılar. Hücre içindeki başlıca büyüme ve hayatta kalma yollarının—özellikle MEK–MAPK ve PI3K–AKT–mTOR yollarının—bozulduğunu buldular. Bu yollar normalde kanser hücrelerinin ölümden kaçınmasına ve bölünmeye devam etmesine yardımcı olur. Araştırmacılar ULK1 eksik sferoidleri MEK veya mTOR’u engelleyen ilaçlarla tedavi ettiklerinde, kanser kümeleri çok daha savunmasız hale geldi; canlılıkları ve yeniden tutunma yetenekleri keskin şekilde azaldı. Buna karşılık, ULK1’in kaldırılması karboplatin, paklitaksel veya PARP inhibitörü olaparib gibi standart kemoterapi ilaçlarının etkinliğini artırmadı ve bazı koşullarda bunların faydasını azaltıyor gibi göründü.
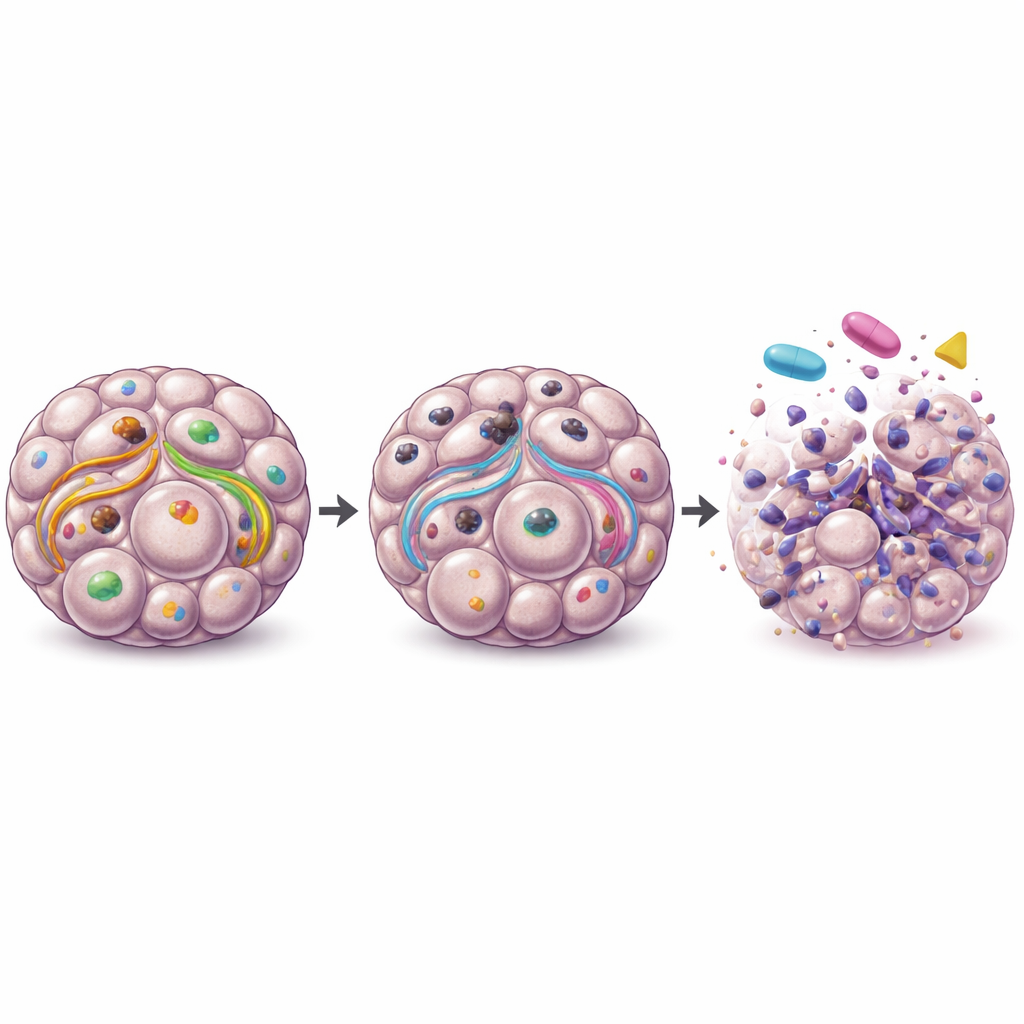
Hasta tümörleri ve minyatür hasta modellerinden ipuçları
Büyük kamu veri setlerindeki over tümörlerine bakıldığında, yazarlar daha yüksek ULK1 gen aktivitesinin daha kötü uzun dönem sağkalımla ilişkili olduğunu ve primer tümörler ile normal dokuya kıyasla metastatik örneklerde özellikle yükseldiğini buldular. Kliniğe daha yakın olmak için, metastatik tümör örneklerinden elde edilen hasta kaynaklı organoidlerde klinik bir ULK1 engelleyici hap olan DCC-3116 test ettiler. Bu hasta modellerinin bir alt kümesinde, tek başına ULK1 engellemesi veya tek başına MEK ya da mTOR ilaçları organoid hayatta kalmasını azalttı; ancak ajanların kombinasyonu sürekli olarak ek bir fayda sağlamadı. Diğer hasta organoidleri tüm tedavilere dirençliydi; bu durum over kanserlerinin ne kadar çeşitli olduğunu ve kimlerin yarar görebileceğini belirlemek için biyobelirteçlere duyulan ihtiyacı vurguluyor.
Gelecekteki bakım için ne anlama geliyor
Bir araya getirildiğinde bulgular, ULK1’i over kanserinin yayılmasının merkezi bir yardımcısı olarak resmediyor: sferoid kümelerinin canlı kalmasını sağlayan içsel geri dönüşümü güçlendiriyor, bunların yeni bölgeleri işgal etme yeteneğini destekliyor ve güçlü büyüme sinyallerini sürdürmelerine yardımcı oluyor. ULK1’in kapatılması bu süreçleri zayıflatıyor, deneysel tümörleri küçültüyor ve kanser hücre kümelerini bazı hedefe yönelik ilaçlara karşı daha duyarlı hale getiriyor; ancak standart kemoterapiye karşı aynı etki gözlemlenmiyor. Hastalar için bu çalışma, ULK1’in özellikle ULK1 seviyesi yüksek, metastatik hastalıkta bir duyarlılık-odaklı stratejinin parçası olabileceğini; ULK1 inhibitörlerinin MEK veya mTOR engelleyicileriyle kombinasyon halinde tümör büyümesini ve yayılmasını sınırlandırmak için kullanılabileceğini gösteriyor; tabii hangi tümörlerin yanıt vereceğini belirleyecek dikkatli testlerin yapılması koşuluyla.
Atıf: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
Anahtar kelimeler: over kanseri, metastaz, otofaji, ULK1, hedefe yönelik tedavi