Clear Sky Science · tr
Retinoidler, retinoik asit reseptörleri ve epigenetiğin meme kanserindeki ilişkisi
Meme Kanseri İçin A Vitamini Neden Önemli?
Çoğu kişi A vitaminini görme için önemli bir besin olarak bilir, ancak vücutta etkin formu olan retinoik asit aynı zamanda hücrelerin büyüyüp büyümemeye, farklılaşmaya veya hasar gördüğünde kendini yok etmeye karar vermesinde rol oynar. Bu derleme makale retinoik asit ve hücresel “bağlanma istasyonlarının” meme kanserinde nasıl değiştiğini, neden laboratuvardaki umut verici sonuçların henüz hastalar için başarılı ilaçlara dönüşmediğini ve kanser hücresinin “yazılımı” olan epigenetik kodu hakkındaki yeni bulguların bu tedavi stratejisini nasıl canlandırabileceğini inceliyor.
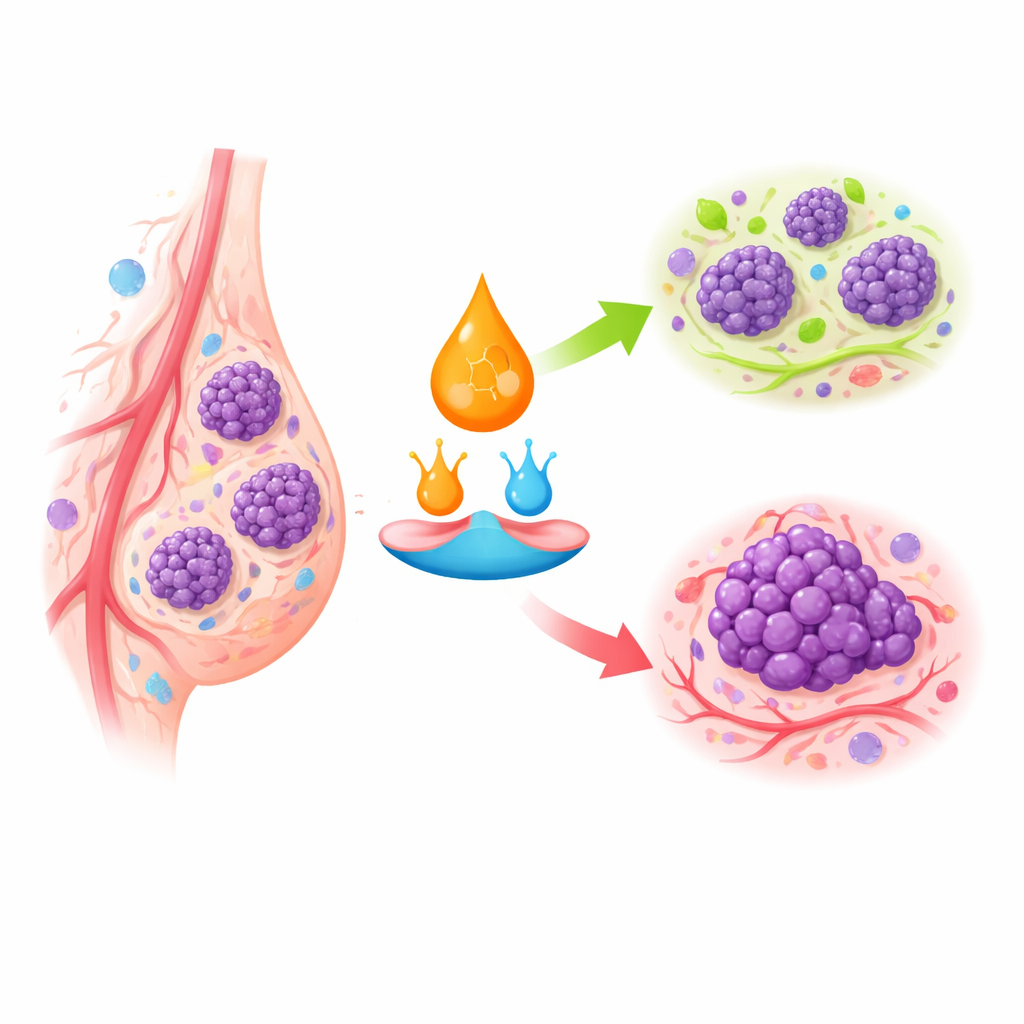
Büyüme ve Kendini Yok Etme İçin Hücresel Trafik Işıkları
Retinoik asit, hücre içindeki belirli reseptörlere bağlanarak çalışır ve bunlar ardından bütün gen kümelerini açıp kapatır. Sağlıklı meme dokusunda bu sistem hücrelerin bölünmeyi bırakmasını, stabil formlara olgunlaşmasını veya anormal hale gelirlerse ölmesini teşvik eder. Meme kanserinde, özellikle daha agresif alt tiplerde, anahtar reseptörler kaybolmuş veya susturulmuş durumda ve retinoik asidin hücre içi taşınması yeniden yönlendiriliyor. Büyümeyi yavaşlatan reseptörlere gitmesi yerine, hayatta kalma ve çoğalmayı teşvik eden yolaklara aktarılabiliyor. Bu durum, bazı meme tümörlerinin retinoid ilaçlara neredeyse yanıt vermemesini, oysa aynı ilaçların belirli kan kanserlerinde çok etkili olmasını açıklamaya yardımcı olur.
Kanser Hücresinin Yazılımındaki Gizli Anahtarlar
Yazarlar epigenetiğe — DNA ve paketleyen proteinler üzerinde yer alan, genom için yazılım ayarları gibi işleyen kimyasal etiketlere — odaklanıyor. Birçok meme kanserinde bu etiketler, özellikle RARβ2 adı verilen önemli retinoik asit reseptörünü, temel DNA dizisini değiştirmeden “kapalı” konuma kilitliyor. DNA üzerindeki ekstra metil grupları ve çevredeki protein makaralarının sıkılaşması bu reseptörü devre dışı bırakırken, diğer enzimler büyüme ve göçü destekleyen kromatin manzarasını yeniden şekillendiriyor. Protein üretmeyen ancak gen etkinliğini etkileyen kodlamayan RNA’lar ise sinyallemeyi hücre ölümü ve farklılaşma yönünden daha uzaklaştırıyor. Birlikte, bu değişiklikler kanser hücrelerine tedaviye direnme ve strese uyum sağlama esnekliği kazandırıyor.
Sinyal Yolaklarını Yeniden Kabllandırma
Önemli bir nokta, bu epigenetik kilitlerin geri çevrilebilir olmasıdır. Laboratuvar modellerinde DNA metilasyonunu kaldıran veya kromatini gevşeten ilaçlar RARβ2 ve retinoik asit yolunun diğer bileşenlerini yeniden ortaya çıkarabiliyor. Retinoik asit ve standart kemoterapi ile birlikte kullanıldığında, bu “hazırlayıcı” ajanlar tümörleri daha etkili küçültüyor ve nüksü beslediği düşünülen kök‑benzeri hücre havuzunu azaltıyor. Retinoik asidin hücre içinde nasıl taşındığı da önem taşıyor: bir taşıyıcı proteinin onu büyümeyi baskılayan reseptörlere götürmesi, diğerinin ise pro‑büyüme yolaklarına sevk etmesi söz konusu. Bu taşıyıcılar arasındaki dengeyi ayarlamak, retinoik asidi bir gübre gibi davranmaktan bir fren gibi davranmaya çevirebilir.
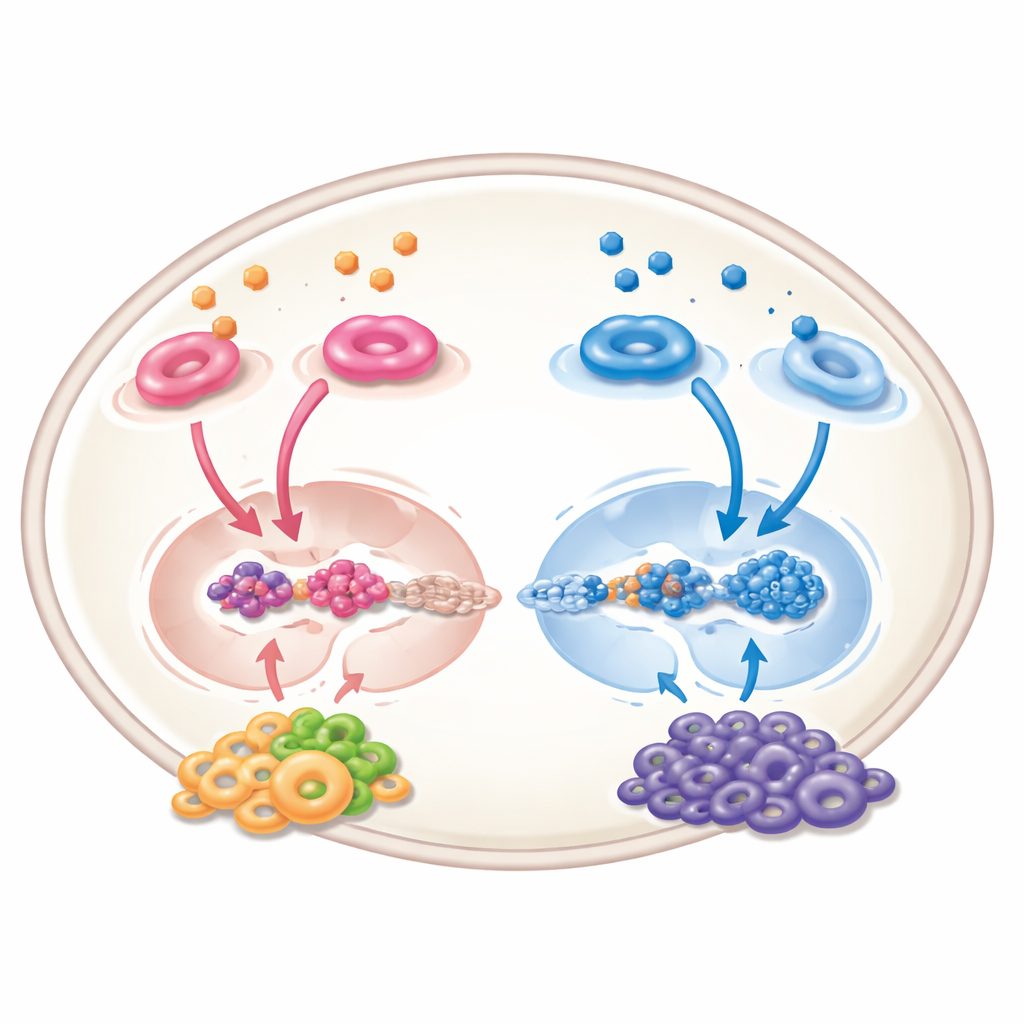
Tümörün Ötesinde: Mahalle Etkisi
Retinoik asit sadece kanser hücreleri üzerinde etki etmez; aynı zamanda tümörün etrafındaki kan damarları, bağışıklık hücreleri ve destek hücrelerinden oluşan “mahalleyi” de yeniden şekillendirir. Deneysel sistemlerde yeni damar oluşumunu azaltabilir, bağışıklık hücrelerini daha aktif, tümörle savaşan bir duruma itebilir ve vücudun savunmasını körelten baskılayıcı hücreleri sınırlayabilir. Yine de tablo tamamen olumlu değildir: tümörü çevreleyen belirli stromal hücrelerde retinoik asit sinyalinin aktivasyonu, kötü huylu hücreleri çeken ve destekleyen kimyasal iletişim kanallarını güçlendirerek kanser büyümesini teşvik edebilir. Bu karşıt etkiler, gelecekteki herhangi bir tedavinin doğru hücre türlerine doğru şekilde hedeflenmesini gerektirir.
Gelecek İçin Daha Akıllı Deney Tasarımları
Meme kanserinde retinoid ilaçların erken klinik deneyleri büyük ölçüde başarısız oldu, ancak bunlar bugün alt tipler, biyobelirteçler ve karmaşık farmakoloji konusundaki anlayışın öncesinde yürütüldü. Yazarlar, yeni çalışmalarda retinoide duyarlılık moleküler işaretlerini gösteren, örneğin reseptör ekspresyonunun korunduğu veya belirli DNA‑metilasyon desenlerinin bulunduğu hastaların seçilmesi gerektiğini; retinoidlerin epigenetik engelleri açan, büyüme yolaklarını hedef alan veya bağışıklık saldırısını artıran ilaçlarla eşleştirilmesi gerektiğini savunuyor. İlaç seviyelerini bünyede sabit tutan geliştirilmiş formulasyonlar ile tümör ve çevre dokunun yakından izlenmesi hayati olacak. Bu engeller aşılabilirse, retinoik asit temelli tedaviler seçilmiş meme kanseri formlarına karşı hassas araçlar olarak yer bulabilir.
Atıf: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
Anahtar kelimeler: retinoik asit, meme kanseri, epigenetik, diferansiyasyon tedavisi, tümör mikroçevresi