Clear Sky Science · tr
Tümör hücreleri ve sağlam kümelerinin yüksek verimli, çok ölçekli zenginleştirilmesi için kademeli atalet temelli mikroakışkanlık: kötü huyluluk tanısının geliştirilmesine yönelik
Neden Akışkan İçindeki Kanser Hücrelerini Ayırmak Önemli
Kanser yayıldığında, tümör hücreleri sıklıkla organlarımızı çevreleyen sıvılara karışır. Akciğer kanseri olan kişilerde bu, akciğerleri çevreleyen ve biriken sıvı olan plevral efüzyonu içerebilir. Bu sıvının içinde nadir tekil tümör hücreleri ve sıkı hücre kümeleri gizlidir. Bu kümelerin özellikle tehlikeli olduğu düşünülür; çünkü agresif hastalık ve kötü sonuçlarla güçlü şekilde ilişkilidir. Yine de mevcut laboratuvar yöntemleri, büyük hasta sıvısı hacimlerinden hem tek hücreleri hem de kümeleri nazikçe ve verimli biçimde ayırmakta zorlanır. Bu çalışma, plevral efüzyonlardan bu hücreleri hızlı ve dikkatli şekilde ayırabilen yeni bir çip tabanlı teknoloji tanıtıyor; bu da daha güvenilir kanser tanısı ve tümör yayılımına dair daha iyi içgörüler için kapı açıyor.
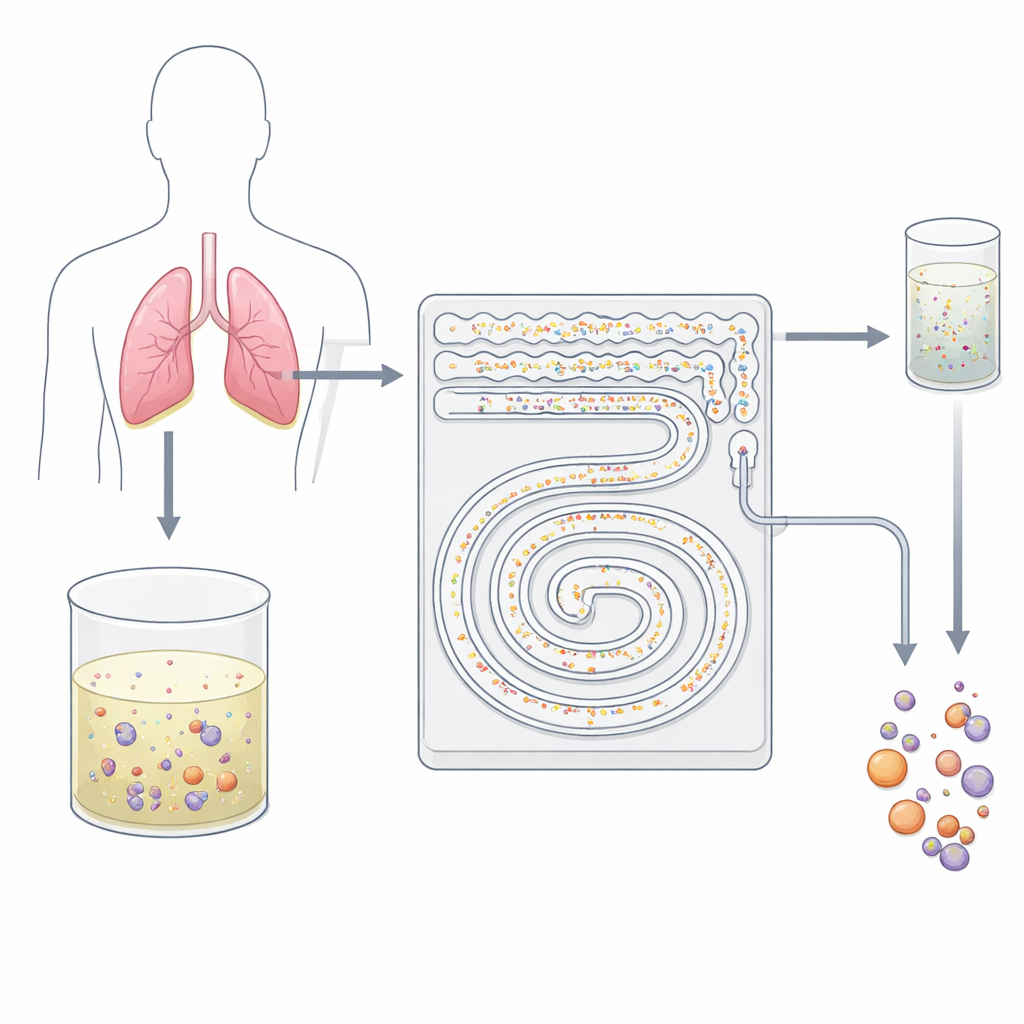
Çip Üzerinde Nazik Bir Hücre Süzgeci
Araştırmacılar, akıllı, iki aşamalı bir filtre gibi davranan minik kanallarla oyulmuş avuç içi büyüklüğünde plastik bir cihaz tasarladı. Yapışkan antikorlar veya sert eleme yerine çip, hücrelerin hızlı akan sıvı içindeki davranışına dayanır. Sıvı kıvrımlı mikrokanallardan hızla geçerken, görünmez kuvvetler farklı boyuttaki parçacıkları farklı akım çizgilerine iter. Ekip bu etkiyi—genel olarak atalet mikroakışkanlığı olarak bilinen—kullanarak küçük arka plan kan hücrelerini daha büyük tümör hücreleri ve kümelerinden etiketlemeden veya temas ettirmeden ayırıyor. Her şey sürekli, kapalı bir akışta gerçekleştiği için cihaz, geleneksel lam bazlı sitolojinin kolayca başaramadığı şekilde onlarca mililitre sıvıyı yalnızca birkaç dakikada işleyebilir.
Birinci Adım: Kalabalığı Temizlemek
Cihazın ilk aşamasında, fazla sıvı çıkarılıp hücreler yeniden süspanse edildikten sonra plevral efüzyon paralel sarmal kanallar dizisine sürülür. Burada dönen, kıvrımlı akım küçük beyaz kan hücrelerini kanal duvarlarına doğru iterken daha büyük tümör hücreleri ve kümeler akımın merkezine yakın kalır. Küçük hücreler atık çıkışlarına yönlendirilir ve arka plan dramatik biçimde seyreltilir. Bu yüksek verimli adım dakikada yaklaşık 8 mililitre hızla çalışabilir; bu da tipik 50 mililitrelik klinik örneğin tıkanma olmadan yaklaşık altı buçuk dakikada işlenebileceği anlamına gelir. Bu ilk aşamadan çıkan, potansiyel olarak malign hücrelerle zenginleşmiş ve daha hassas ayırım için hazır çok daha temiz bir karışımdır.
İkinci Adım: Tekilleri Kümelerden Ayırmak
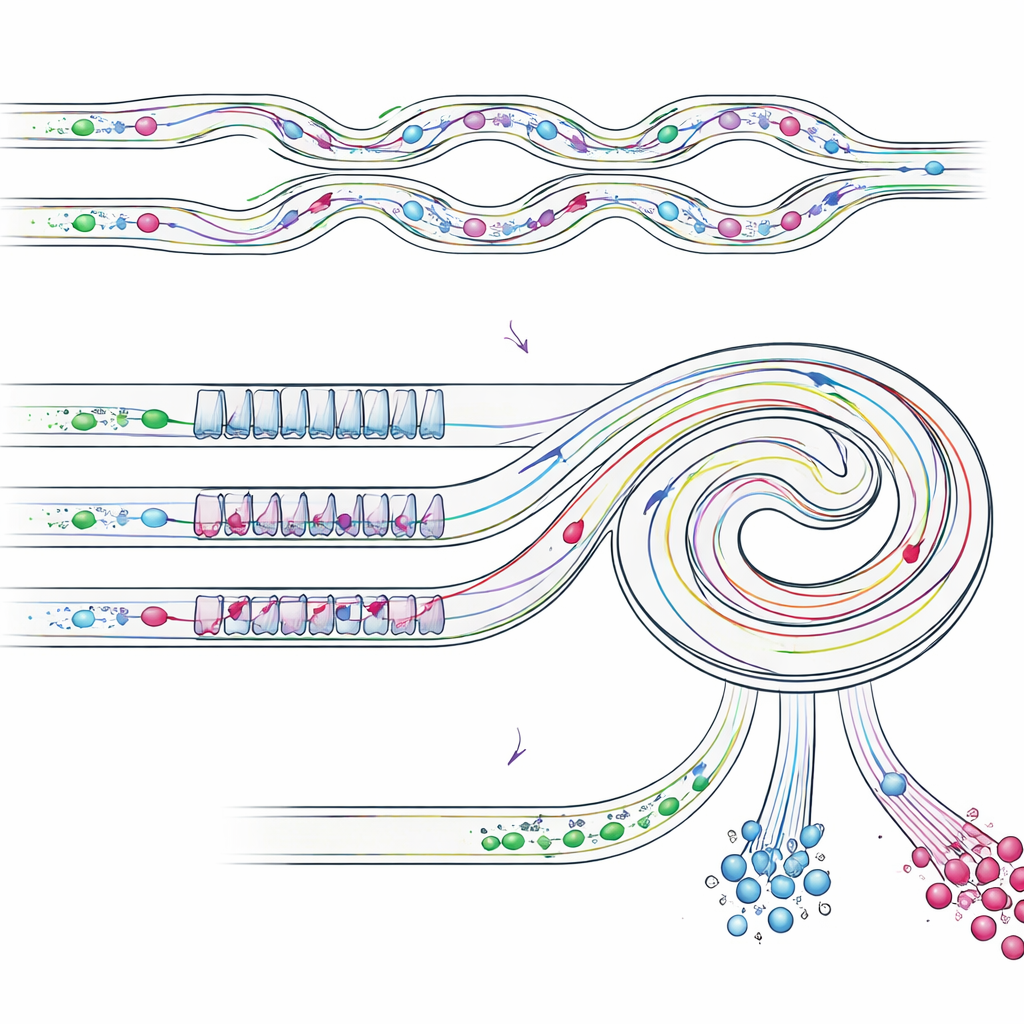
Kısmen zenginleştirilmiş örnek daha sonra dar ve geniş bölümlerin tekrar eden desenini içeren eğimli bir spiral kanala girer. Bu aşamada, farklı boyuttaki nesneler için birkaç akım kuvveti farklı dengelenir ve bunlar spiral iç veya dış duvarına yakın ayrı şeritlere yönlendirilir. Daha küçük olan tek tümör benzeri hücreler bir yan konumda hizalanırken, daha hacimli kümeler iç duvara daha yakın farklı bir konuma göç eder. Çıkışlar doğru noktalara yerleştirilerek çip bu akımları fiziksel olarak ayırır: bir çıkış ağırlıklı olarak tek tümör hücrelerini toplar, bir diğeri sağlam kümeleri toplar ve diğer çıkışlar kalan küçük hücreleri uzaklaştırır. Önemli olarak, kümeler bir parça halinde kalır; bu da geleneksel filtrasyon yöntemlerinde sık görülen hasar ve parçalanmayı önler.
Cihazı Sınamaya Koymak
Tasarımın ne kadar iyi çalıştığını kontrol etmek için ekip önce bilinen boyutlarda plastik boncuklar kullanarak kan hücrelerini, tek tümör hücrelerini ve kümeleri taklit etti. Kademeli çipin “tek hücre” boncuklarının %87’den fazlasını ve “küme” boncuklarının yaklaşık %92’sini geri kazandığını, daha küçük “kan hücresi” boncuklarının ise çoğunu uzaklaştırdığını gösterdiler. Ardından beyaz kan hücreleriyle karıştırılmış gerçek akciğer kanseri hücreleri (A549 hücreleri) üzerinde çalıştılar. Bu testlerde cihaz genel olarak kanser hücrelerinin yaklaşık %82’sini geri kazandı; zenginleştirilmiş fraksiyonda yaklaşık %76 saflık ve hücre kümeleri için neredeyse %80 saflık elde edildi. Son olarak üç akciğer kanseri hastasından alınan gerçek plevral efüzyon örneklerini işlediler. Başlangıçta tüm hücrelerin içinde tümör hücreleri ve kümelerin %1’den azını oluşturduğu sıvıdan çip, tek malign hücrelerin tüm hücrelerin yaklaşık %68’ine; kümelerin ise ayrılmış bir çıkış akımında hücrelerin yaklaşık %35’ini oluşturduğu fraksiyonlar üretti.
Bu Hastalar İçin Ne Anlama Gelebilir
Sadece sıvı akışı ve kanal geometrisini kullanarak, bu cihaz kimyasal etiketler veya karmaşık aletler gerektirmeden büyük hasta sıvı hacimlerinden hem tek tümör hücrelerini hem de sağlam kümeleri hızlı ve nazikçe ayırabilir. Zenginleştirilmiş hücreler immünofloresans boyama ve mikroskopi gibi standart testler için uygun kalır ve mevcut hastane iş akışlarına sorunsuzca uyum sağlar. Mevcut çalışma az sayıda hasta içerdiği ve tanı ile prognoz üzerindeki etkisini kanıtlamak için daha büyük denemelere ihtiyaç duyacağı halde, bu çalışma güçlü bir kavramı gösteriyor: plevral efüzyonlardaki hem hücre sayısını hem de hücrelerin kümelenme durumunu ortaya çıkaran hızlı, etiketsiz bir “hücre yoğunlaştırıcı.” Uzun vadede böyle araçlar kötü huyluluk değerlendirmesini keskinleştirebilir, kişiselleştirilmiş tedavi seçimlerine rehberlik edebilir ve kanserlerin metastaz yapma biçimine daha net bir pencere sağlayabilir.
Atıf: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
Anahtar kelimeler: sıvı biyopsi, mikroakışkan hücre ayırma, tümör hücre kümeleri, plevral efüzyon, kanser tanısı