Clear Sky Science · tr
Mikropipet direnç modellemesine dayalı robotik hücre taşıma sistemi
Mikroskop Olmadan Küçük Hücreleri Taşımak
Modern biyoloji sıklıkla şaşırtıcı derecede basit bir işe dayanır: tek bir hücreyi cam bir tüple alıp başka bir yere yerleştirmek. Bu, üreme tedavileri, embriyo dondurma, hücre tabanlı terapiler ve temel araştırma için elzemdir. Ancak bugün neredeyse her zaman hantal bir mikroskop ve her hareketi izleyen yüksek eğitimli bir insan operatör gerektirir. Bu makale, tek hücreleri herhangi bir mikroskobik görüntü olmadan damlacıklar arasında taşıyabilen yeni bir robotik sistemi tanımlıyor; bu, daha hızlı, daha ucuz ve narin hücrelere daha az zarar veren tamamen kapalı, otomatik “hücre fabrikaları”nın önünü açıyor.
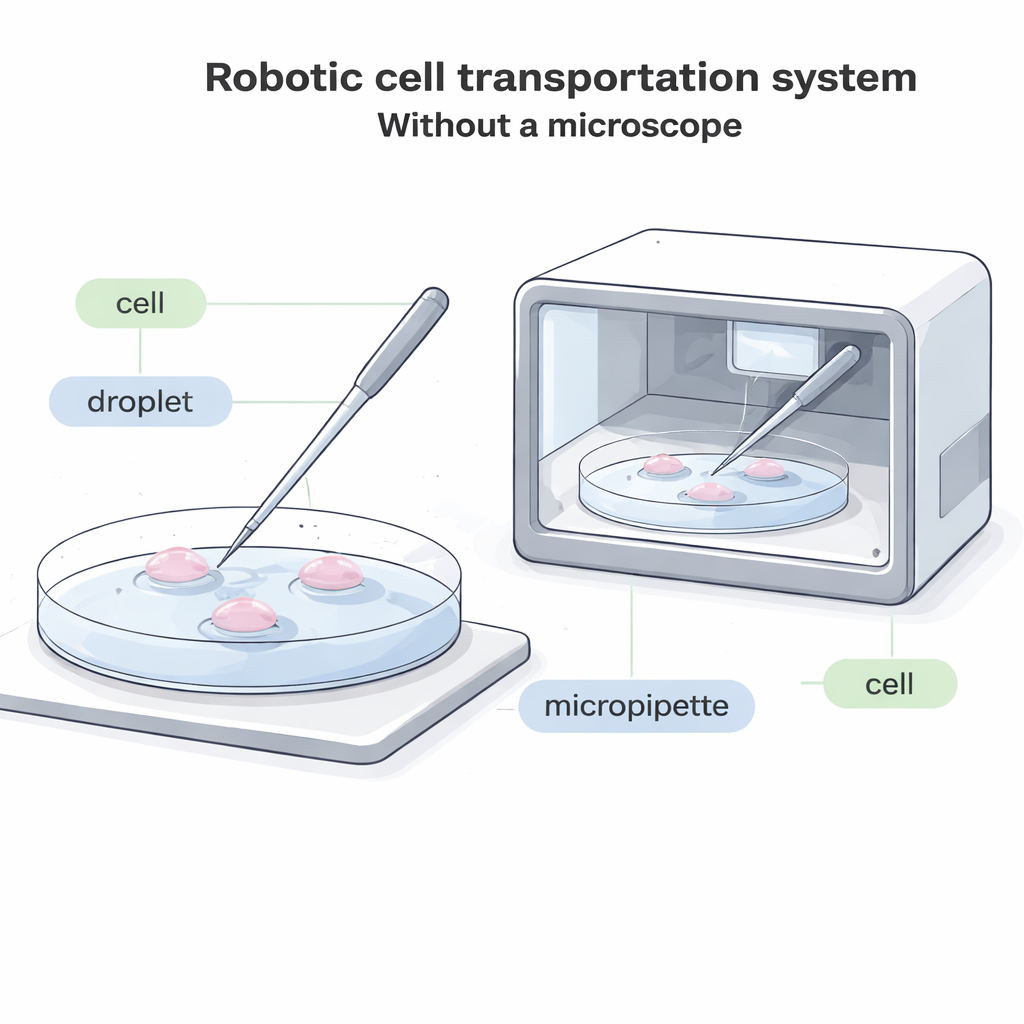
Hücre Taşımanın Neden Yenilenmesi Gerekiyor
Mevcut laboratuvarlarda operatör bir mikroskopla bakar ve mikropipet adı verilen ince cam tüple bir kabın dibine inerek bir hücreyi nazikçe emer, onu yeni bir sıvı damlacığına kaydırır ve sonra iterek çıkarır. Bu süreç yavaştır, görsel olarak yorucudur ve otomatikleştirmesi zordur. Gelecekteki birçok sistemde—örneğin içi kapalı, embriyoları veya diğer hücreleri bir kutu içinde büyüten kompakt cihazlarda—geleneksel bir mikroskopa yer yoktur. Başka durumlarda hücreler parlak boyalarla etiketlenir; bu boyalar solabilir veya ışıkla hasar görebilir, dolayısıyla yoğun mikroskobik gözlemi azaltmak önemlidir. Görüntüye dayanmayan mevcut “kör” sistemler yalnızca olağanüstü büyük hücreler için işe yarar; bu da çoğu yaygın hücre türünü iyi bir otomatik çözümden mahrum bırakır.
İçinde Durma Özelliği Olan Özel Bir Kamış
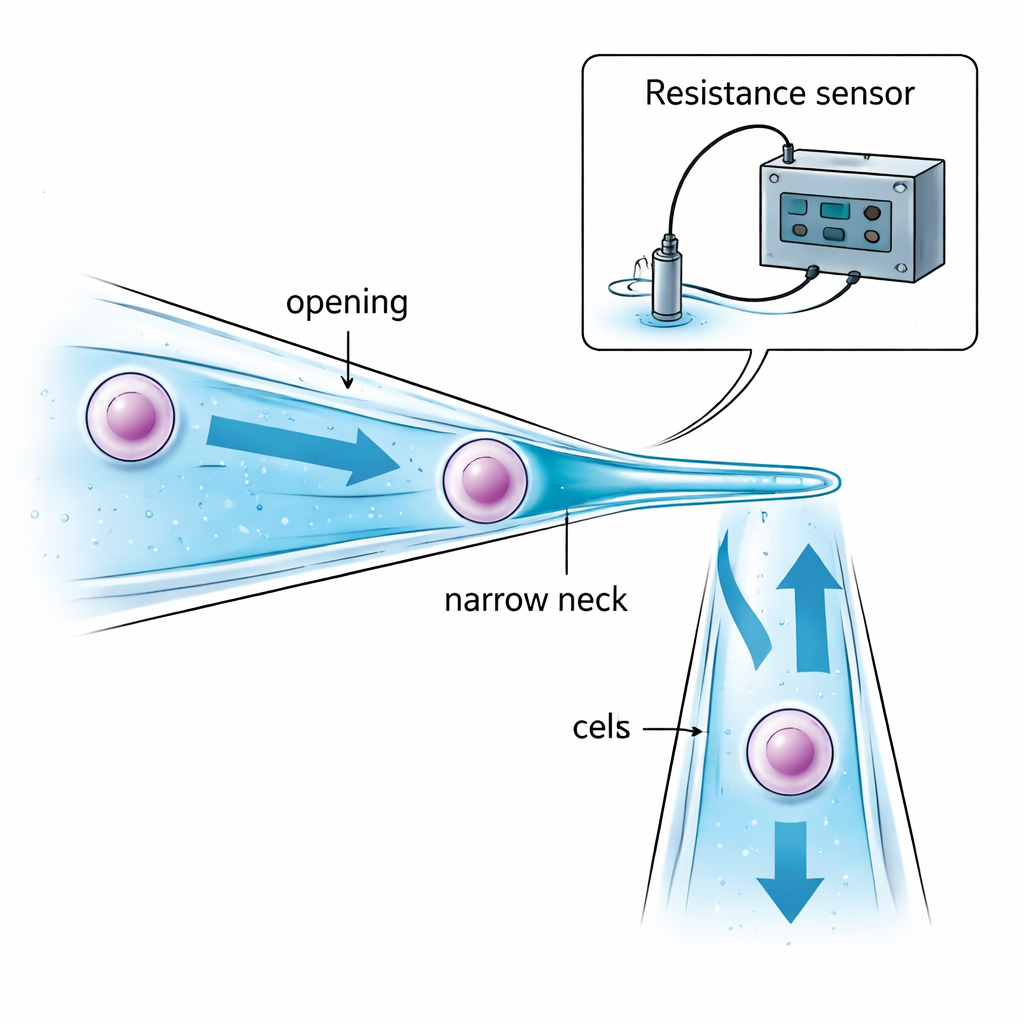
Yazarlar sorunu mikropipetin kendisini yeniden tasarlayarak ele alıyor. Sürekli aynı çapa sahip düz bir cam tüp yerine, dar boğazlı bir mikropipet oluşturuyorlar. Açıklığı hedef hücreden biraz daha geniştir, böylece hücre içeri çekilebilir. Daha derinde tüp hafifçe daralarak hücreden daha küçük bir “boğaz” oluşturur. Emme hücreyi bu daralmaya doğru çekerken, hücre boğazda durur ve tüpün içinde sabitlenir—uçta sarkıp damlacıklar arasındaki yağ veya havaya maruz kalmaz. Açılış, boğaz ve bunlar arasındaki mesafenin dikkatli seçimi, hücrenin aşırı sıkıştırılmadan güvenli şekilde yakalanmasını ve bir damlacıkta taşınan sıvı miktarının az tutulmasını sağlar; böylece kontaminasyon azalır.
Bakmak Yerine Elektriksel Sinyalleri Dinlemek
Mikroskop olmadan robotun yine de üç şeyi bilmesi gerekir: cam uç tabanına yeterince yaklaştığında, hücrenin boğazda başarıyla yakalandığında ve yeni damlacığa tamamen bırakıldığında. Ekip bunu, mikropipetin içindeki ve çevresindeki sıvıdaki küçük elektriksel direnç değişimlerini izleyerek çözüyor. Eğik pipet kabın dibine yaklaştıkça aradaki sıvı boşluğu daralır ve direnç öngörülebilir bir şekilde artar; bu, temas öncesinde güvenli bir inişi işaret eder. Bir hücre dar boğazı tıkadığında, sıvı yolundaki kesit azalır ve direnç aniden yükselir; hücre itildiğinde direnç aynı şekilde düşer. Bu “boşluk”, “emiş” ve “enjeksiyon” dirençlerinin matematiksel modelleri, bir bilgisayarın bu sinyalleri gerçek zamanlı yorumlayıp görsel geri bildirim olmadan emme veya basıncı ne zaman durduracağını belirlemesini sağlar.
Robotu Test Etmek
Bu yaklaşımın pratikte işe yarayıp yaramadığını görmek için araştırmacılar hareket kontrolü, basınç kontrolü, direnç algılama ve bir ana bilgisayarı birleştiren eksiksiz bir robotik düzenek inşa ettiler. Sistemi yaklaşık 10 mikrometre çapındaki küçük kanser hücreleri olarak bilinen HeLa hücreleri ve yaklaşık 150 mikrometre büyüklüğündeki domuz yumurta hücreleri üzerinde test ettiler. Sistem, pipet boyutlarının geniş bir aralığında inişi, yakalamayı ve bırakmayı yalnızca direnç sinyallerinden güvenilir şekilde algılayabildi. Doğrudan karşılaştırmalarda robot, HeLa hücrelerini yüzde 90 başarı oranıyla taşıdı—önceki görüntü tabanlı otomatik yöntemden daha iyi—ve domuz yumurtalarını yüzde 95 başarı oranıyla taşdı; bu, standart mikroskopik yaklaşımdan daha yüksekti. Hücre başına işlem süreleri, dar boğazın hücrenin konumunu ayarlamak için tekrarlayan ince ayar gereksinimini ortadan kaldırması nedeniyle insan kontrollü yöntemlerle benzer veya daha hızlıydı.
Hücreleri Canlı Tutmak ve Ölçeklendirmek
Bir biyoloji laboratuvarındaki herhangi bir robotik yardımcı, taşıdığı hücrelere zarar vermekten kaçınmak zorundadır. Yeni sistemle taşındıktan sonra hem HeLa hücreleri hem de domuz yumurta hücreleri bir gün boyunca kültüre alındı ve yalnızca canlı hücrelerde ışık saçan bir boya ile boyandı. Yeni yöntemin hayatta kalma oranları, geleneksel mikroskop rehberli transfer ve dokunulmamış kontrol hücrelerinin oranlarıyla eşleşti veya onlara yakındı; bu, dar boğazdaki nazik mekanik sıkıştırmanın, eşik değerler doğru şekilde ayarlandığında hücre canlılığını belirgin şekilde azaltmadığını gösterir. İleriye bakıldığında yazarlar aynı direnç tabanlı algılama ve basınç kontrolünün kompakt mikroakışkan çiplere yerleştirilebileceğini öne sürüyor. Bu, birçok kanalın paralel çalışmasına izin vererek, otomatik üreme tıbbı, hücre terapileri ve mikroskopların kolayca giremediği uzun süreli hücre kültürü cihazları için yüksek hacimli, tamamen kapalı hücre işleme sistemlerini mümkün kılar.
Gelecekteki Hücre Çalışmaları İçin Anlamı
Uzman olmayanlar için ana mesaj şudur: tek hücreleri taşımak artık bir kişinin mikroskop aracılığıyla izlemesine bağlı olmak zorunda değil. Bir cam tüpü dikkatlice şekillendirerek ve çevredeki sıvı boyunca elektriğin nasıl aktığını “dinleyerek”, bir robot iniş yaptığını, bir hücreyi yakaladığını ve bırakıp serbest bıraktığını hissedebilir—karanlıkta ve dar alanlarda bile. Bu, hassas örnekleri koruyan, klinik iş akışlarını basitleştiren ve laboratuvar kalitesinde hücre manipülasyonunu otomatik, fabrika benzeri işletmeye daha yakın hale getiren kapalı, kendi kendine çalışan hücre kültür sistemlerini tasarlamayı çok daha pratik hale getirir.
Atıf: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
Anahtar kelimeler: hücre manipülasyonu, mikropipet, robotik, mikroakışkanlar, otomasyon