Clear Sky Science · tr
Hücrelerin Mikro-fizyolojik Sistemlerde Mekansal Örgütlenmesini Kontrol Etme Stratejileri
Laboratuvarda Küçük Dokular İnşa Etmek
Organlarımız bu kadar iyi çalışır çünkü hücreleri rastgele dağılmamıştır—mekânsal olarak özenle düzenlenmişlerdir. Bu makale, bilim insanlarının bu karmaşık düzeni “organ-on-a-chip” ve diğer minyatür laboratuvar yapımı dokular içinde nasıl yeniden oluşturmayı öğrendiklerini inceliyor. Farklı hücrelerin nerede konumlanacağını ve nasıl etkileşime gireceğini yönlendirerek, araştırmacılar kalp, beyin, bağırsak, kan damarları ve hatta insan–mikrop ekosistemlerinin daha gerçekçi modellerini inşa edebiliyor. Bu gelişmiş sistemler daha güvenli ilaç testleri, daha az hayvan deneyi ve hastalıkları incelemek ile kişiye özel tedaviler geliştirmek için daha iyi araçlar vaat ediyor.
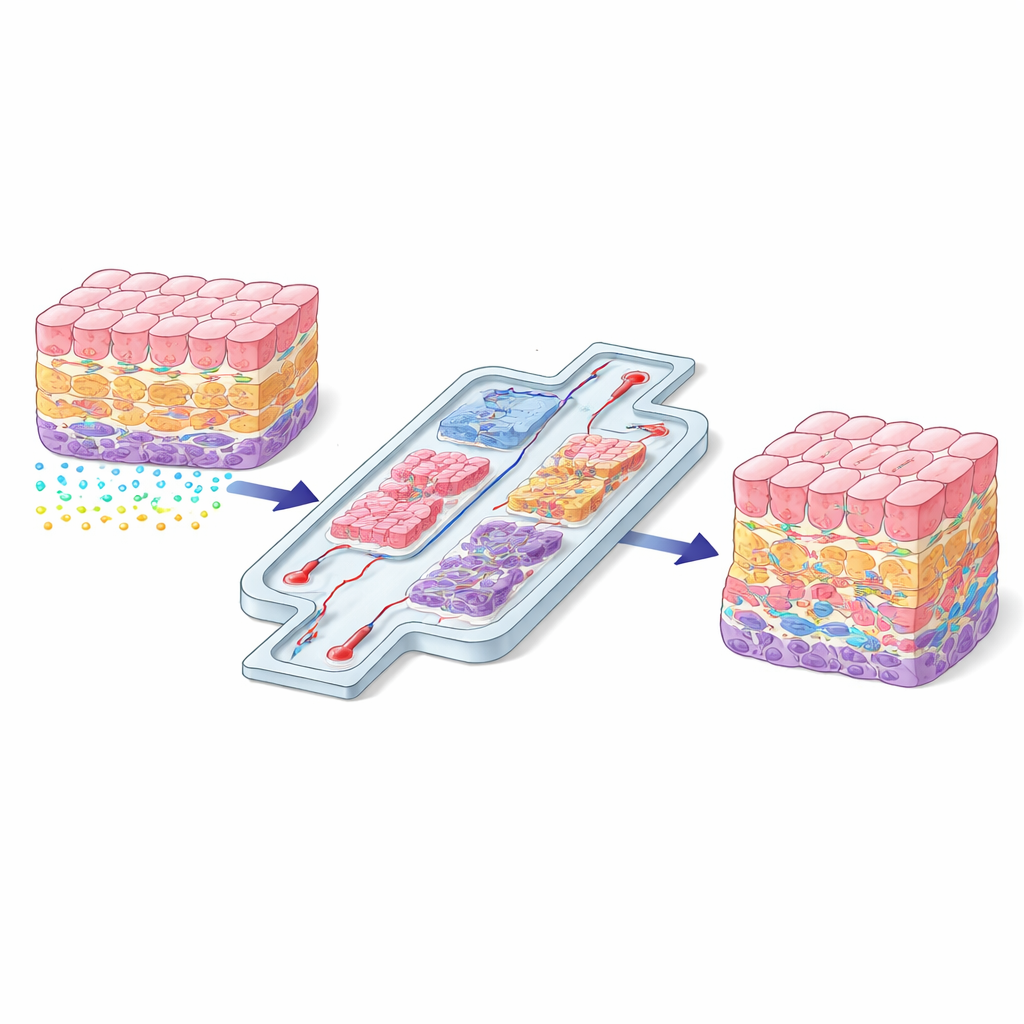
Hücrenin Konumu Neden Önemli?
Vücut içinde her hücre kendi destek yapıları, kimyasal sinyalleri ve fiziksel kuvvetleriyle özgün bir mahallede yaşar. Bir kan damarına yakın bir karaciğer hücresi, organın derinliklerinde gömülü bir hücreden çok farklı ipuçları alır. Konuma bağlı bu farklılıklar hücrelerin nasıl büyüdüğünü, neye dönüşeceğini ve yaralanma ya da ilaca nasıl yanıt vereceğini belirlemeye yardımcı olur. Bilim insanları hücreleri düz plastik kaplarda yetiştirdiğinde, bu mekânsal “konuşma” büyük ölçüde kaybolur ve hücreler sıklıkla doğal olmayan davranışlar sergiler. Makale, gerçekçi mekânsal örgütlenmenin isteğe bağlı bir iyileştirme değil; laboratuvarda yetiştirilen dokular gerçek organları taklit edecekse temel bir gereklilik olduğunu savunuyor.
Hücreleri Düzenlemenin İki Temel Yolu
Yazarlar mevcut stratejileri doğrudan kontrol ve dolaylı kontrol olmak üzere iki geniş aileye ayırıyor. Doğrudan yöntemler hücreleri veya bölmeleri tam gerektiği yere fiziksel olarak yerleştirir. Örnekler arasında hücreleri ve yumuşak jelleri biyolojik bir 3B yazıcı gibi katman katman yerleştiren 3B biyoyazdırma; dokuları bağlı odacıklar ve kanallara bölen mikroakışkan çipler; ışık, ses, mıknatıslar veya elektrik alanları kullanarak hücreleri konumlandıran fiziksel tutma yöntemleri yer alır. Bu yaklaşımlar, kan-beyin bariyerini, katmanlı bir damar duvarını veya bağırsaktan karaciğere giden akış yolunu yeniden oluşturmak gibi hassas geometrinin kritik olduğu durumlarda öne çıkar.
Hücrelerin Çevrelerini Okumasına İzin Vermek
Dolaylı yöntemler ise çevreyi yeniden şekillendirir ve gerisini hücrelere bırakır. Burada bilim insanları hücrelerin algıladığı “peyzajı” ayarlar: çevreleyen jel içeriği, yüzeylerin sertliği ve dokusu ile büyüme faktörleri veya ilaçlar gibi çözünmüş maddelerin gradyanları. Özenle yerleştirilmiş destek molekülleri belirli hücre tiplerinin belli bölgelere yerleşmesini sağlayabilir. Hücreler tarafından yeniden düzenlendiğinde yumuşayan veya sinyaller salan akıllı hidrojeller, kan damarları ağları veya bağırsak benzeri kript ve villus gibi kendiliğinden organize yapıları teşvik eder. Mikroakışkan cihazlar, kök hücrelerin bir kanal boyunca farklı kimlikler benimsemesine veya kanser hücreleri ile bağışıklık hücrelerinin ayrı bölgelere göç etmesine neden olan stabil kimyasal gradyanlar oluşturabilir; bu da hastalıkların nasıl yayıldığını açığa çıkarır.
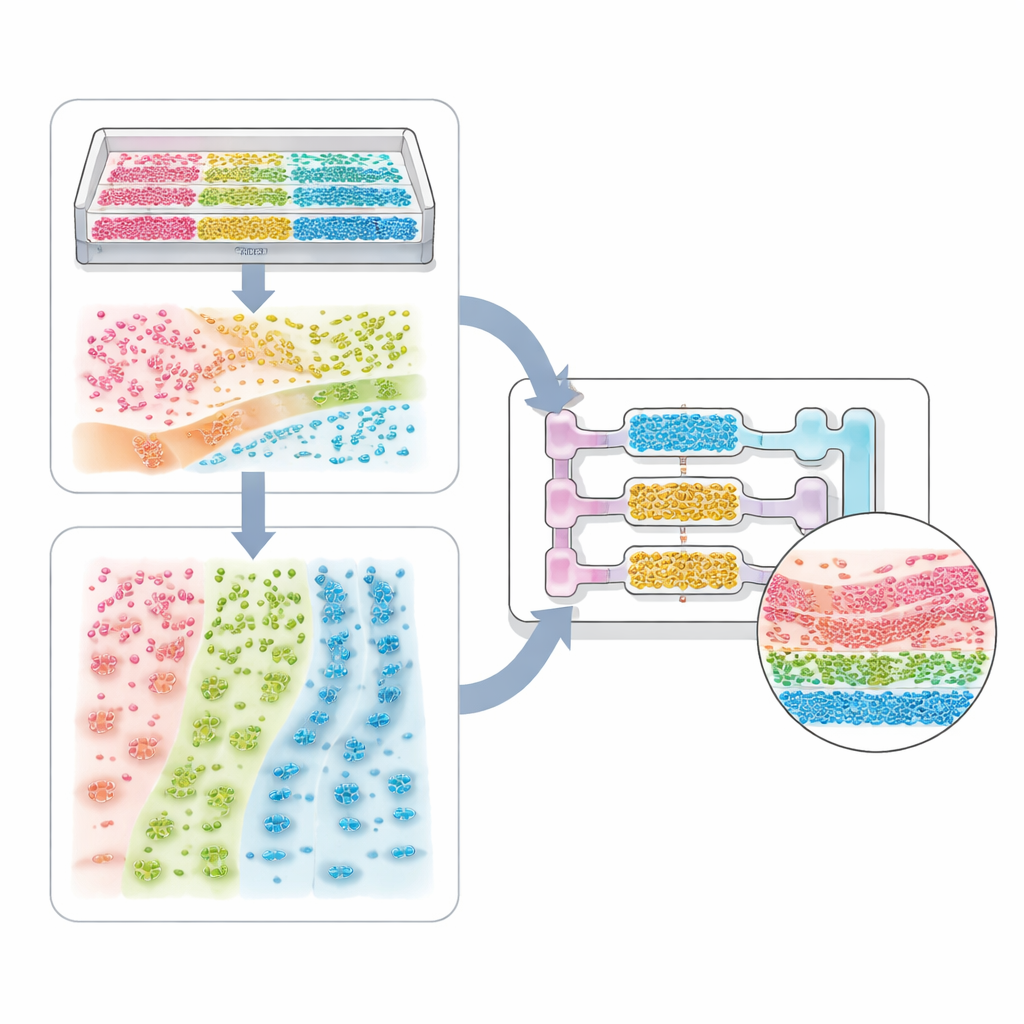
Tek Hücreli Sistemlerden Tüm Vücut Modellerine
Derleme bir uygulama yelpazesinin üzerinden geçiyor. En basit uçta, desenli oluklar veya sertlik gradyanları kalp hücrelerinin birbiriyle senkronize atmasını veya sinir hücrelerinin hizalanmış lifler uzatmasını sağlayan tek hücre tipi sistemleri bulunuyor. Daha karmaşık doku modelleri, tümör hücreleri, destek hücreleri ve kan damarı hücreleri gibi birkaç hücre tipini karıştırarak iç çekirdekli ve kabuklu sferoidler ve organoidler oluşturur. Mikrokanal çipleri ve biyoyazdırma daha sonra sınırlar ve akış ekleyerek akciğer hava keseciklerini, böbrek filtrelerini, karaciğer zonlarını ve bir ilacın nasıl emildiğini, dönüştürüldüğünü ve temizlendiğini izleyen çok organlı devreleri yeniden oluşturmayı mümkün kılar. Aynı fikirler, bağırsak duvarı boyunca veya mukus tabakası genelinde bakterilerin mekânsal düzeni koruyucu mu yoksa hastalık yapıcı mı olduklarını belirleyebildiği konakçı–mikrop sistemlerine de uzanır.
Desenlerin Gerçek Olduğunu Kontrol Etmek
Bu sistemler daha karmaşık hale geldikçe, bilim insanlarının hücrelerin olması gerektiği yere ulaştığını ve amaçlandığı gibi davrandığını doğrulamak için güvenilir yöntemlere ihtiyacı var. Makale, canlı hücrelerin zaman içinde hareketini ve değişimini izleyebilen görüntüleme yöntemlerini; her lokasyonda hangi genlerin, proteinlerin ve metabolitlerin ortaya çıktığını haritalayan gelişmiş boyama ve dizileme tekniklerini vurguluyor. Çiplere gömülü sensörler oksijen, besin, asitlik ve mekanik kuvvetleri izleyerek yerel koşulları hücre yanıtlarıyla ilişkilendiriyor. Bu araçlar birlikte, bir tasarımın sadece görsel olarak ikna edici değil, işlevsel olarak da gerçek dokuya sadık olduğunu doğrulamaya yardımcı oluyor.
Bu Çalışma Nereye Gidiyor?
Yazarlar en güçlü sistemlerin doğrudan ve dolaylı stratejileri harmanlayacağını sonuçlandırıyor: genel düzeni belirlemek için çipler ve biyoyazıcılar kullanmak, ardından dokuların zaman içinde olgunlaşıp yeniden şekillenmesine izin veren ayarlanabilir jeller, dokular ve gradyanlar katmak. Ayrıca üretimi ölçeklendirme, laboratuvarlar arasındaki değişkenliği azaltma ve karmaşık insan doku modelleri etrafındaki etik soruları ele alma gibi pratik engellere de dikkat çekiyorlar. Yine de mesaj açık: mekânsal örgütlenmenin ustalığı, mikro-fizyolojik sistemleri insan organlarının güvenilir vekilleri haline getirmenin anahtarıdır ve gelişim çalışmaları, tedavi testleri ve bireye özel tıbbın kapılarını aralar.
Atıf: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
Anahtar kelimeler: organ-on-a-chip, hücre mekansal örgütlenmesi, 3B biyoyazdırma, mikroakışkan doku modelleri, mikrofizyolojik sistemler