Clear Sky Science · tr
Önçoğaltma olmadan HPV 16’nın hızlı, özgül ve duyarlı tespiti için tek tüplü CRISPR tabanlı yatakbaşı platformu
Neden tek bir virüs türünü ayırt etmek gerçekten önemli
Servikal kanser sıklıkla insan papilloma virüsleri (HPV) ile ilişkilidir, ancak tüm HPV tipleri aynı riski taşımaz. Bu nedenle hekimlerin, özellikle yüksek riskli HPV16 gibi türleri, birbirine çok benzeyen virüsleri güvenilir şekilde ayırt edebilen testlere ihtiyacı vardır. Sorun şu ki, bugünkü genetik testler bazen yakın akrabaları karıştırabilir; bu da yanlış pozitiflere veya gözden kaçan vakalara yol açabilir. Bu çalışma, doğruluk ve kullanılabilirlik açısından belirgin biçimde iyileştiren yeni bir test yöntemini tanıtıyor; amaç, kesin HPV alt tiplemesini kliniklere ve yatakbaşı ortamlara taşımak.
Akıllı moleküler kilit ve anahtar
Araştırmacılar CASTSA adını verdikleri tek tüplü bir test geliştirdiler; bu test iki güçlü fikri birleştiriyor: bakterilerden uyarlanmış gen hedefleme sistemi CRISPR’ın hassasiyeti ve DNA’yı kopyalama konusunda standart yöntem olan PCR’ın sinyal artırıcı yeteneği. CASTSA’da Cas12a adlı bir CRISPR proteini, kısa bir RNA “anahtarı” tarafından HPV16 genetik dizisine yönlendirilir. Cas12a doğru eşleşmeyi ve yakınındaki kısa bir deseni bulduğunda, viral DNA’yı öngörülebilir bir noktadan keser. Bu kesim, tek bir DNA zincirinde özgün bir başlama ucu oluşturur ve bu uç amplifikasyon için benzersiz bir başlangıç noktası sağlar. Çok benzer dizilere sahip diğer HPV tipleri ya kesilmez ya da doğru başlama ucunu oluşturmaz; dolayısıyla amplifiye edilmezler.
Küçük bir kesiği güçlü bir sinyale dönüştürmek
Bu CRISPR kesimini tespit edilebilir bir sinyale çevirmek için ekip terminal‑özgül adı verilen özel bir DNA primeri tasarladı. Bu primer sadece Cas12a’nın kesimiyle oluşan zincire doğru biçimde bağlanır, ardından kendi üzerine katlanıp bir saç tokası (hairpin) yapısı oluşturur ve PCR için stabil bir şablon oluşturmaya yardımcı olur. Ek “evrensel” primer dizileri daha sonra ilişir ve konvansiyonel gerçek‑zamanlı PCR reaksiyonunu sürdürür. Kritik olarak, amplifikasyon yalnızca Cas12a önce görevini yapmışsa ve primer doğru şekilde katlanmışsa gerçekleşir; böylece iki katlı doğrulama sağlanır. Bu mimari, ayrı bir ön‑çoğaltma adımına dayanan önceki CRISPR‑tabanlı testlerin yaygın bir zayıflığı olan kısmi eşleşen hedef dışı DNA’nın kazara amplifiye edilme olasılığını büyük ölçüde azaltır.
Hepsi bir tüpte, daha az hata ile
Pratik bir ilerleme, CRISPR kesimi ile PCR amplifikasyonunun aynı kapalı tüp içinde birlikte gerçekleşmesidir; bu, adımlar arasında tüpleri açma ihtiyacını ortadan kaldırır—birçok laboratuvar iş akışında kontaminasyonun başlıca kaynağı. Yazarlar, özellikle magnezyum seviyeleri olmak üzere reaksiyon koşullarını dikkatle ayarladılar, böylece hem Cas12a hem de DNA kopyalayan enzim, sahte reaksiyonları teşvik etmeden iyi çalışıyor. Tek tüplü düzeneklerinin HPV16’yı HPV18, 33, 45 ve 52 dahil olmak üzere birkaç diğer yüksek‑riskli türden güvenilir şekilde ayırt edebildiğini gösterdiler; bu türler aralarında yüksek derecede korunmuş bölgelere sahip olsalar bile. Standart gerçek‑zamanlı PCR ile veya önce DNA’yı amplifiye edip ardından CRISPR tespiti yapan CRISPR testleriyle karşılaştırıldığında, CASTSA hedef dışı HPV tiplerinden kaynaklanan yanıltıcı sinyalleri çok daha az üretti.
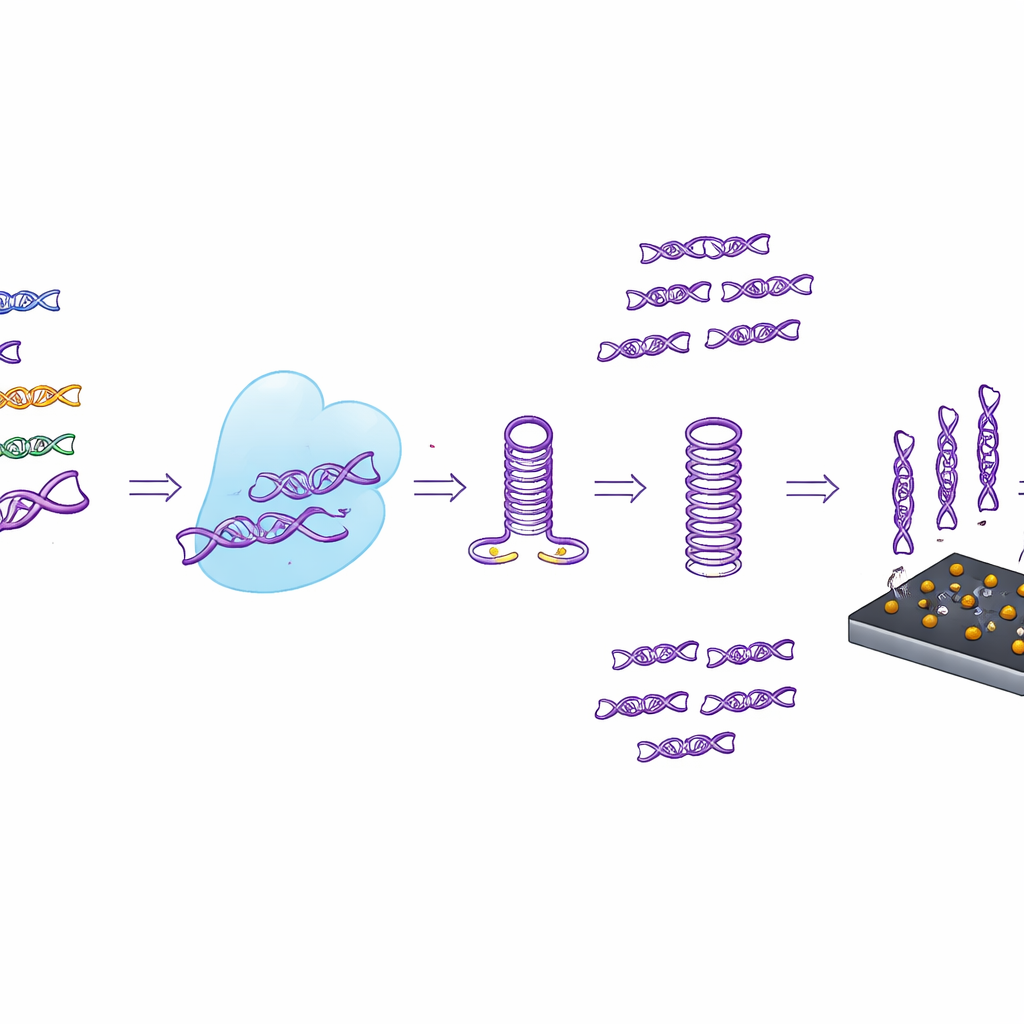
Deney tüpünden elde tutulan sensöre
Sadece floresan okumalara dayanmak yerine, araştırmacılar CASTSA’yı ayrıca lazer kaynaklı grafenden yapılmış kompakt bir elektrokimyasal sensörle eşleştirdiler. Bu gözenekli, yüksek iletkenlikli karbon yüzey altın nanoparçacıklarla kaplanmış olup, yalnızca CASTSA amplifikasyon ürünlerine bağlanacak şekilde dizayn edilmiş yakalama zincirleri taşır. Bu ürünler yapıştığında, sensörden geçen elektrik akımı ölçülebilir biçimde değişir. Üç ölçüm noktası ve bir dahili arka plan kontrolünden oluşan dört elektrotlu bir dizi kullanarak cihaz, özgül olmayan yapışmadan kaynaklanan gürültüyü çıkarabilir. Denemelerde bu entegre sistem, reaksiyon başına yalnızca 18 kopya HPV16 hedefini tespit edebildi; bu, yalnızca floresansla elde edilen duyarlılığı aştı ve mükemmele yakın tekrar edilebilirlik sağladı.
HPV testlerini nasıl değiştirebilir
Yöntemin gerçek hayatta nasıl çalıştığını görmek için ekip, HPV16 içerdiği bilinen 20 klinik örneği ve sağlıklı bağışçılardan alınan 10 örneği test etti. CASTSA, hem floresans biçiminde hem de grafen‑bazlı sensörle eşleştirildiğinde hastane standart PCR testleriyle tamamen aynı sonucu verdi. Aynı zamanda, yaygın karışıklığa neden olan diğer yüksek‑riskli HPV tiplerini görmezden gelme konusunda üstünlük gösterdi. Hastalar için bu, daha az belirsiz sonuç ve takip ile tedavi kararlarında daha fazla güven anlamına gelebilir. Daha geniş açıdan bakıldığında, CASTSA stratejisi—önce CRISPR tanıma, sonra amplifikasyon, hepsi kapalı tek bir tüpte—özellikle hızlı ve güvenilir cevapların istendiği ortamlarda birçok patojen ve mutasyon için uyarlanabilecek, yüksek özgüllükte ve düşük kontaminasyonlu genetik testler için bir şablon sunar.
Atıf: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
Anahtar kelimeler: HPV16 tespiti, CRISPR tanı yöntemleri, PCR tabanlı testler, elektrokimyasal biyosensör, yatakbaşı assayi