Clear Sky Science · tr
Hücre içindeki canlı örneklerde katkısız görüntüleme için 120 nm yanal çözünürlükte enterferometrik görüntü tarama mikroskopisi
Ek boya kullanmadan canlı hücreleri görmek
Modern biyoloji, hücrelerimizin içindeki gizli mimariyi ortaya çıkarmak için sıklıkla parlayan floresan etiketlere dayanır. Ancak bu etiketler hücrelere stres verebilir, davranışlarını değiştirebilir ve hassas veya genetik olarak kolayca değiştirilmesi mümkün olmayan örneklerde kullanılamayabilir. Bu makale, hücrelerin içindeki canlı süreçleri yüksek ayrıntıyla—hiçbir boya veya genetik etiket eklemeden—izlemenin yeni bir yolunu tanıtıyor; bu, hücrelerin gerçek işleyişini daha nazik, daha uzun süre ve daha doğal koşullarda gözlemleme olanağı vaat ediyor.
Hücreleri ışığı nasıl saçtıklarına göre görmek
Yöntem, floresansa dayanmayan ve bunun yerine küçük yapılar tarafından saçılan ışığı ölçen bir teknik ailesine dayanır. Bu yaklaşımlardan biri olan enterferometrik saçılma mikroskopisi (iSCAT), nanoskopik bir nesne tarafından saçılan ışığı cam yüzeyinden gelen bir referans yansımasıyla karıştırır. Ortaya çıkan enterferans deseni, proteinler, virüsler veya veziküller gibi çok küçük parçacıklara karşı son derece duyarlıdır. iSCAT daha önce izole parçacıklar gibi basit, temiz örneklerde en iyi sonucu vermiştir. Ancak, bunu canlı hücrelerin derinliklerine uygulamak zordu çünkü hücreler kalabalık ve karmaşıktır: çok sayıda örtüşen saçılma olayı ince detayları gizleyen benekli bir arka plan oluşturur.
Daha keskin, daha nazik görüntüleme için iki fikrin birleşimi
Bu sınırlamaları aşmak için yazarlar iSCAT’ı görüntü tarama mikroskopisi (ISM) adlı güçlü bir görüntüleme stratejisiyle birleştirdiler. ISM’de örnek, odaklanmış bir ışınla nokta nokta taranır ve tek bir detektör kullanmak yerine, bir detektör dizisi her noktanın birçok hafifçe kaymış görünümünü kaydeder. Bu görünümler akıllıca yeniden hizalanıp birleştirildiğinde, kıymetli fotonlardan vazgeçmeden nihai görüntü keskinleştirilebilir. Yeni teknik—enterferometrik görüntü tarama mikroskopisi veya iISM—bu fikri enterferometrik saçılmanın daha karmaşık, fazdan duyarlı sinyallerine uyarlıyor. Mikroskop, mavi bir lazer, ışık polarizasyonunu simetrik hale getiren özel optikler ve her tarama konumu için saçılan ve yansıyan ışığı kaydeden hassas bir kamera kullanır. Ardından özel bir hesaplamalı iş akışı, sinyalin dalga benzeri doğasına saygı göstererek piksel bilgisini yeniden atar ve standart kırınım sınırlı optikten yaklaşık iki kat daha ince, yaklaşık 120 nanometre yanal çözünürlükte görüntüler elde eder.
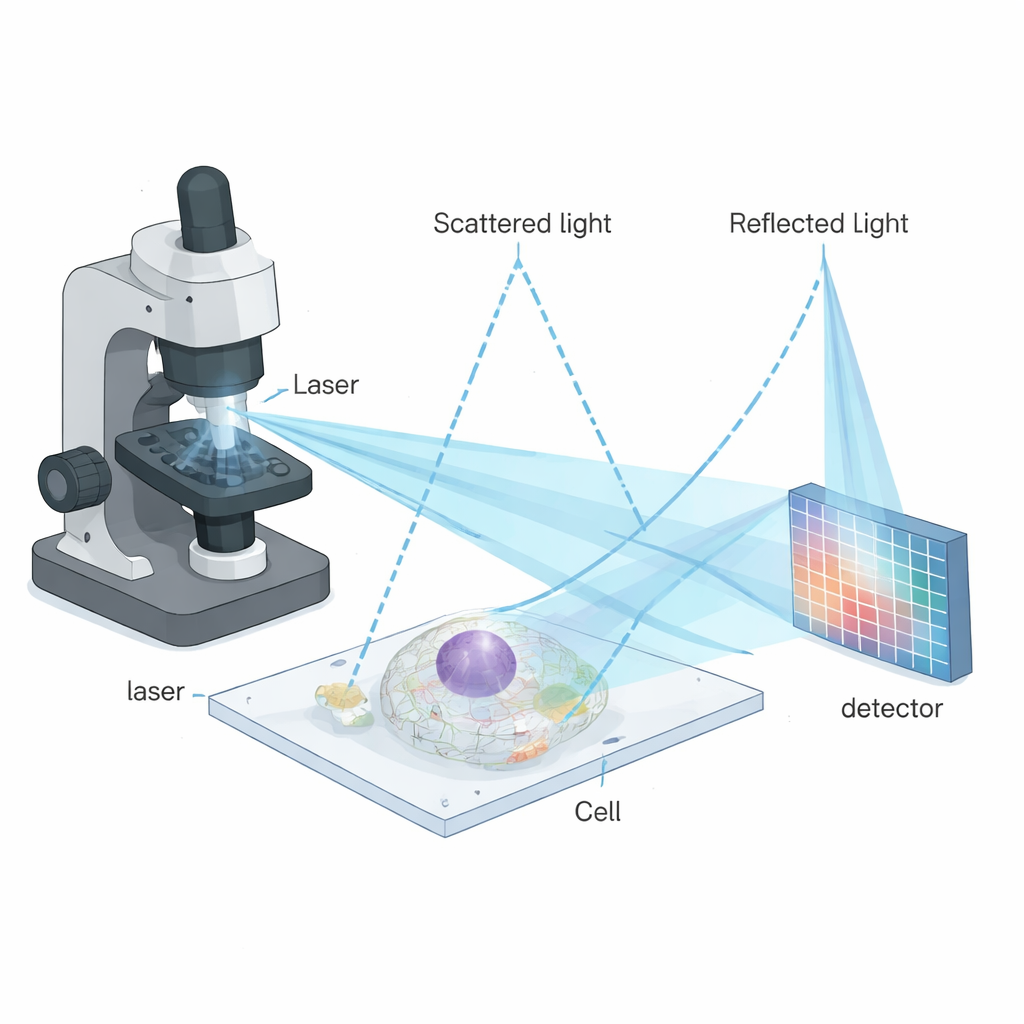
Zorlu desenleri net resimlere çeviren akıllı algoritmalar
Enterferometrik sinyaller parlaklık ve faz bilgisi beraber taşıdığından, floresans görüntülemeden gelen olağan işleme püf noktaları yeterli değildir. Yazarlar, koherent ışık için uyarlanmış bir adaptif piksel-yenidenatanama (APR) prosedürü tasarladılar. Önce, her küçük enterferometrik deseni, sinyalin pozitif mi yoksa negatif mi olduğuna bakmaksızın simetri merkezlerini öne çıkaran bir “radyal varyans” haritasına dönüştürüyorlar. Bu adım, karmaşık enterferans halkalarını, geleneksel yoğunluk görüntüleri gibi davranan görünümlere etkili biçimde çeviriyor. Sonra açık kaynaklı yazılım kullanarak her detektör pikselinin görüntüsünün merkeze göre ne kadar kaydığını belirleyip, bunları toplama işleminden önce uygun şekilde geri kaydırıyorlar. Bu rafine hizalama, faydalı sinyali yoğunlaştırırken gürültüyü ortalayıp düşürür ve sıkı bir pinhole’lü konfokal iSCAT görüntüsüne kıyasla kontrast-gürültü oranını aynı ışık seviyesinde yaklaşık dört kat artırır.
Organelleri ve iskelet sistemlerini hareket halindeyken izlemek
Bu teknik gelişmelerle ekip, iISM’nin pratikte nasıl performans gösterdiğini test etmek için canlı COS-7 hücrelerine yöneldi. Çok düşük aydınlatma gücünde—odaklanmış nokta başına tipik konfokal mikroskopların kullandığından yaklaşık on kat daha düşük—endoplazmik retikulum, mitokondri, veziküller, aktin iskeleti, plazma membranı ve lamellipodia adı verilen ince önde gelen kenar yapıları gibi temel organelleri net biçimde ayırt edebildiler. Enterferometrik kontrast dikey konuma hassas olduğundan, benzer organeller pozitif veya negatif kontrastla görünebilir ve yalnızca birkaç yüz nanometrelik ince yükseklik farklarını açığa çıkarabilir. Zaman atlamalı diziler kaydederek, veziküllerin hareketini ve endoplazmik retikulum tübüllerinin birkaç dakika boyunca yeniden şekillenmesini izlediler; belirgin bir fotohasarlanma gözlemlenmedi ve görüntülemenin hücre davranışlarını bozduğuna dair bir işaret görünmedi.
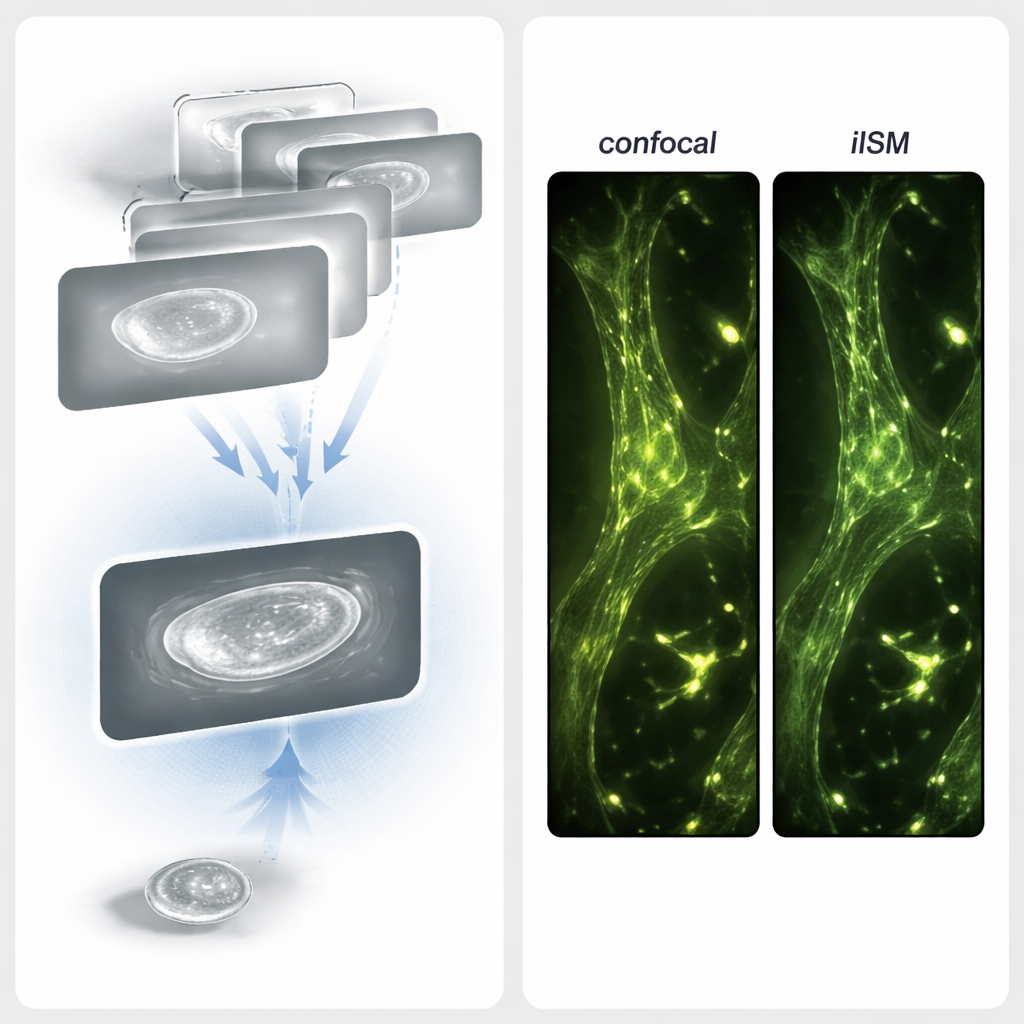
Katkısız görünümleri floresan haritalarla eşleştirmek
Katkısız görüntülerin gerçekten gerçek hücresel yapıları yansıttığını kontrol etmek için araştırmacılar sabitlenmiş hücrelerde hem iISM hem de floresans ISM ölçümleri yaptılar. Aktin iskeleti kırmızı bir floresan boya ile boyandı ve aynı bölgenin süper çözünür floresans görüntüleri katkısız iISM görüntüleriyle birlikte kaydedildi. İkisini üst üste koyduklarında, floresans kanalındaki parlak aktin filamentleri iISM görüntülerindeki filament benzeri yapılarla yakın doğrulukta hizalandı. Bazı bölgelerde, iISM filamentler boyunca veya yakınlardaki boyanmamış yapılar (örneğin fokal adezyonlar) gibi ilave saçılma ayrıntılarını ortaya çıkardı; bunlar floresans kanalında görünmezdi. Birlikte, bu sonuçlar iISM’nin bilinen yapıları doğrulayabildiğini ve ayrıca boyanmamış çevre hakkında ek bilgi açığa çıkarabildiğini gösteriyor.
Daha az rahatsızlıkla hücrelere yeni bir pencere
Uzman olmayanlar için ana mesaj şudur: iISM hücreleri yapay olarak parlatmadan içlerindeki ince detayları görmenin bir yolunu sunar. Enterferometrik saçılmanın duyarlılığını görüntü taramanın keskinleştirici gücüyle birleştirerek yaklaşık 120 nanometre çözünürlük elde ederken birçok mevcut mikroskoptan çok daha az ışık kullanır. İleri konfokal sistemlerde zaten yaygın olan bileşenlerden inşa edildiği için, prensipte ticari cihazlara eklenebilir. Gelecekte iISM, geleneksel floresans, hızlı detektörler veya hatta makine öğrenmesi tabanlı “sanal boyamalar” ile eşleştirilerek enfeksiyonları, yük taşımayı veya sitoskeletal yeniden düzenlemeleri hücrelerin daha doğal, bozulmamış koşulları altında izleyebilir.
Atıf: Küppers, M., Moerner, W.E. Interferometric Image Scanning Microscopy for label-free imaging at 120 nm lateral resolution inside live cells. Light Sci Appl 15, 129 (2026). https://doi.org/10.1038/s41377-026-02210-y
Anahtar kelimeler: katkısız görüntüleme, canlı hücre mikroskopisi, enterferometrik saçılma, süper çözünürlük, hücresel organeller