Clear Sky Science · tr
microRNA işleme makinesindeki hastalıkla ilişkili mutasyonlara ilişkin yapısal içgörüler
Hücrenin Küçük RNA Makasları Sağlığı ve Hastalığı Nasıl Şekillendirir
Her hücrenin içinde, genetik mesajlar okunmadan önce düzeltilip kısaltılan gizli bir düzenleme sistemi vardır. Bu sistem, aynı anda binlerce gen için ince ayar düğmeleri gibi davranan microRNA adı verilen küçük RNA parçalarına dayanır. microRNA’ları üreten moleküler “makineler” düzgün çalıştığında hücreler kontrol altında büyür, bölünür ve özelleşir. Ancak bu makineler mutasyonlarla hasar gördüğünde, gen aktivitesi dengesi kansere, kan hastalıklarına veya beyin gelişiminde bozukluklara kayabilir. Bu makale, bu makinelerin 3B formlarını anlamanın bilim insanlarının neyin yanlış gittiğini ve nasıl düzeltilebileceğini belirlemesine nasıl yardımcı olduğunu açıklar.
Hücrenin Gen-Susturma Takımı
MicroRNA’lar kendileri protein kodlamayan yaklaşık 22 yapı taşı uzunluğunda kısa RNA parçalarıdır. Bunun yerine, daha uzun haberci RNA’lara tutunur ve onları ya yok edilmek üzere işaretler ya da çeviriyi engelleyerek genleri tamamen kapatmak yerine kısıtlar. Bu microRNA’ları yapmak için hücreler daha uzun RNA öncüllerini aşamalı bir montaj hattından geçirir. Önce, DROSHA enzimi hücre çekirdeğindeki kaba primer transkriptleri daha kısa saç tokası (hairpin) şeklindeki parçalara kısaltır. Bu parçalar daha sonra sitoplazmaya taşınır; orada başka bir enzim olan DICER, saç tokasının ucunu tuttuğu yer ile katalitik merkezinin kestiği yer arasındaki sabit mesafeyi ölçerek microRNA boyutunda çift sarmallar keser. Son olarak, bu çiftlerin bir ipliği Argonaute 2 (AGO2) adı verilen bir proteine yüklenir; AGO2 microRNA’yı kılavuz olarak kullanarak eşleşen mesajları bulur ve sessizleştirir. 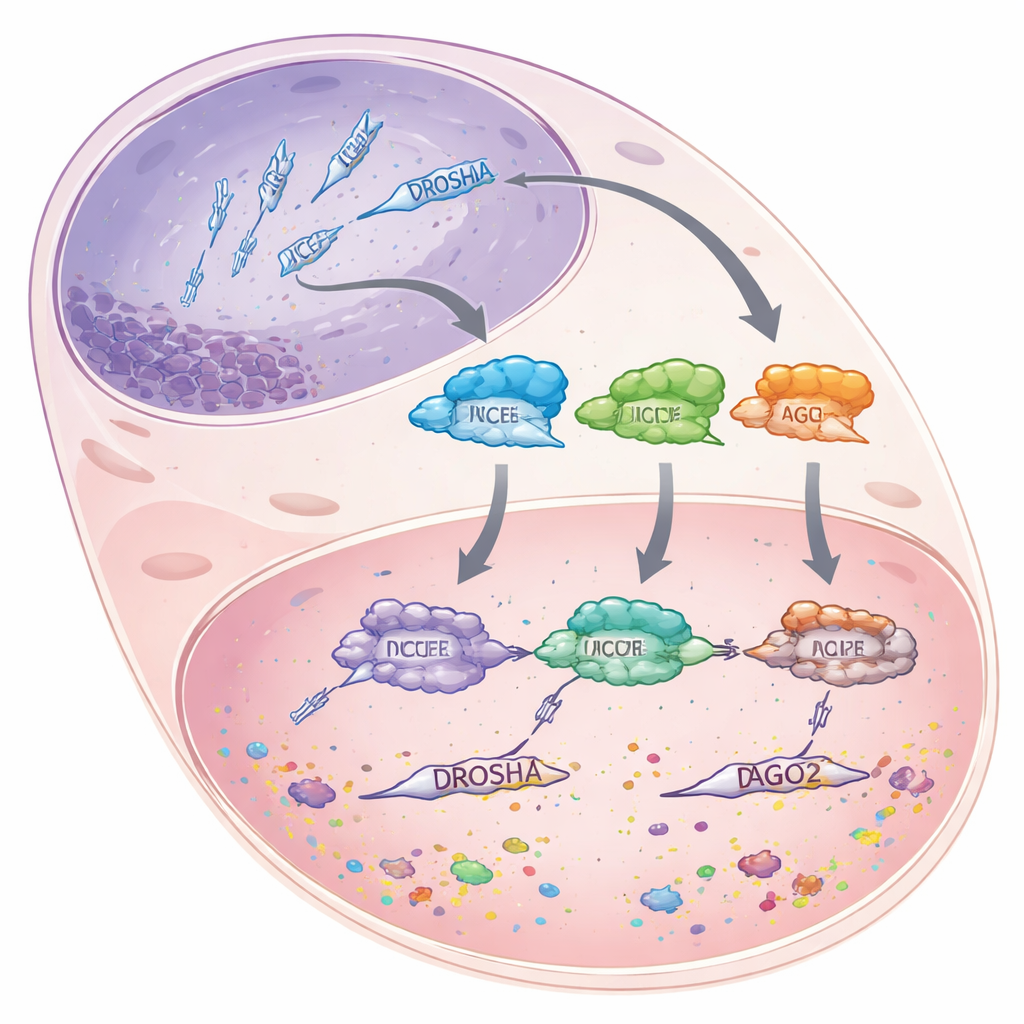
Hassas İşler İçin İnce Yapılar
DROSHA, DICER ve AGO2 basit makaslar değildir; her biri koreografik bir şekilde hareket etmesi gereken birden çok etkileşen parçadan oluşur. DROSHA, primer microRNA saç tokasının uçlarını kavramak ve tam olarak nereden keseceğine karar vermek için ortak bir protein olan DGCR8 ile birlikte çalışır. DICER, saç tokası ucunu tuttuğu yer ile katalitik merkezinin kesik yaptığı yer arasında sabit bir mesafe belirleyen yapısal bir cetvel işlevi gören domain’lere sahiptir. AGO2 ise tek bir microRNA ipliğini sarar; böylece “seed” (tohum) bölgesi hedef mesajları tanımak için mükemmel şekilde açığa çıkar ve çekirdekteki metal iyonları ile kritik aminoasitler, eşleşme yeterince güçlü olduğunda bu hedefleri kesmek üzere hizalanır. Üç protein genelinde pozitif yüklü oluklar ve esnek bağlantılar RNA ipliklerini doğru yerlere yönlendirirken, metal bağlayan cepler ve katalitik kalıntılar kimyasal kesimleri gerçekleştirir.
Makaslar Eğrildiğinde veya Körleştiğinde
Kanser, kan hastalıkları ve nörogelişimsel sendromları olan hastalardaki genetik çalışmalar, bu microRNA makinelerinde mutasyon kümeleri ortaya çıkarmıştır. En zararlı değişikliklerin çoğu doğrudan katalitik merkezlerde veya sıkı RNA tutan yüzeylerde yer alır. Örneğin DROSHA’da E1147K ve D1219G gibi yer değiştirmeler kesme bölgesinin merkezinde bulunur ve gerekli metal iyonlarını tutma yeteneğini bozar; bunun sonucu enzim primer microRNA’ları işleyemez. DROSHA’daki diğer mutasyonlar, kesme bölgesini kaldıran kırpmalar veya destek helikslerini destabilize eden değişiklikler tüm kompleksi zayıflatır ve Wilms tümörü, kemik iliği bozuklukları ve sinir sistemi hastalıklarında global microRNA seviyelerinin düşmesine yol açar. DICER’da tekrarlayan mutasyonlar iki kesme domain’inden birinde kümelenir; bu durum microRNA çiftinin bir kolunun kaybolmasına neden olarak büyümeyi teşvik eden ve baskılayan sinyaller arasındaki dengeyi kaydırır. 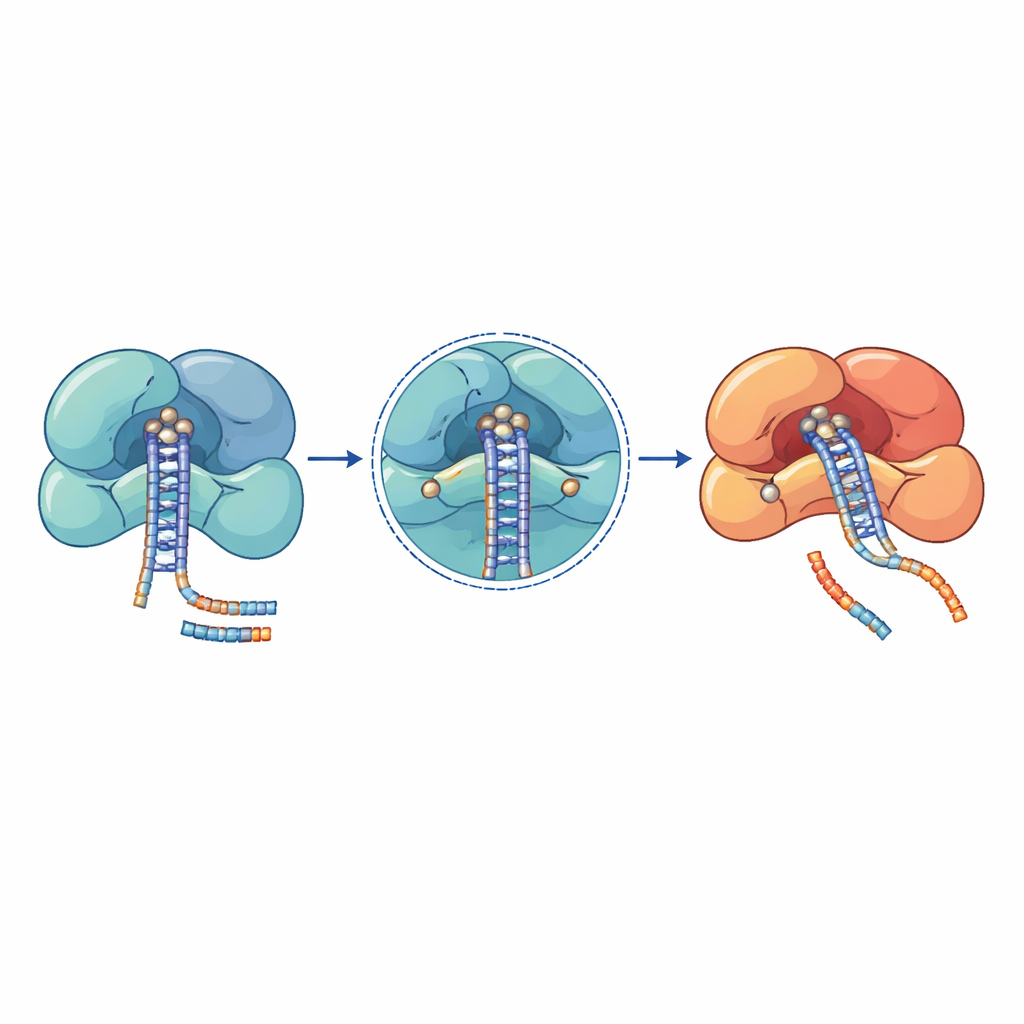
Beyinde ve Ötesinde Hizasız Kılavuzlar
AGO2 mutasyonları farklı ama bağlantılı bir tablo sunar. Katalitik çekirdeğe doğrudan isabet eden değişiklikler nadirdir; muhtemelen bunlar gelişimin erken döneminde öldürücü olurdu. Bunun yerine hastalıkla ilişkili varyantlar genellikle esnek bağlantı bölgelerinde ve AGO2’nin şeklini bir arada tutan domain birleşim noktalarında ortaya çıkar. Lessel–Kreienkamp sendromu gibi bir nörogelişimsel durumda, bu bağlantılardaki ve çevresindeki yüzeylerdeki mutasyonlar AGO2’nin PAZ, MID ve PIWI parçalarının nasıl paketlendiğini ve hareket ettiğini ince bir şekilde bükebilir. Bu, kılavuz microRNA’nın hizasını bozabilir veya hedef RNA’lara tutunmasını zayıflatabilir; böylece beyin gelişimi sırasında gen susturmanın hassasiyeti bulanıklaşır. DROSHA, DICER veya AGO2’da microRNA yolunun herhangi bir yerindeki benzer yapısal değişiklikler, hücre büyümesi, kan oluşumu veya nöronal bağlantılanma ile ilgili tüm gen ağlarını etkileyerek dalga etkisi yaratabilir.
Yapısal İpuçlarını Geleceğin Tedavilerine Dönüştürmek
Hastalık mutasyonlarını bu proteinlerin yüksek çözünürlüklü 3B haritalarının üzerine yerleştirerek araştırmacılar her bir değişikliğin nasıl sorun yarattığını—kesme ucunun körleşmesi, ortak proteinlerle kritik temasların gevşemesi veya önemli helikslerin hizasının bozulması gibi—tam olarak sınıflandırabilirler. Bu yapısal içgörüler hedefe yönelik müdahalelerin kapısını açar: zayıflamış ara yüzleri stabilize eden küçük moleküller, kısmen işlevsel enzimleri doğru substratlara yönlendiren tasarlanmış RNA’lar veya mutasyonlu proteinleri daha aktif konformasyonlara iten allosterik bileşikler. Bir gözlemci için çıkarılacak temel mesaj şudur: hücrenin RNA makaslarındaki küçük yapısal değişiklikler sağlık üzerinde orantısız etkiler yapabilir, ancak aynı zamanda mutasyona duyarlı yeni nesil tedaviler tasarlamak için çok kesin tutamaçlar sağlar.
Atıf: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
Anahtar kelimeler: microRNA, RNA interferansı, DROSHA DICER AGO2, kanser genetiği, nörogelişimsel bozukluklar