Clear Sky Science · tr
Snail proteininin stabilitesinin düzenleyici mekanizmaları: ubikitin–proteazom sistemi ve şaperon aracılı otofaji
Kanserin Yayılması Neden Kırılgan Bir Proteine Bağlıdır
Kanser, hücrelerin orijinal tümörden kopup uzak organlara taşındığında gerçekten hayatı tehdit eden bir hâl alır. Bu yayılma veya metastaz kısmen hücrelerin bağlarını gevşetip daha hareketli hâle gelmesine yardımcı olan güçlü bir "ustalık anahtarı" proteini olan Snail’e bağlıdır. Bu makale, hücrelerimizin Snail’i normalde hızla parçalayarak iki ana atık bertaraf sistemiyle nasıl dizginlediğini açıklıyor. Bu dengenin anlaşılması, metastazı yavaşlatma veya önleme konusunda yeni fikirler sunuyor.
Sıkı Paketlenmiş Hücrelerden Gezgin İstilacılara
Sağlıklı dokularda epitel hücreleri düzenli, tuğla gibi katmanlar oluşturur; yerinde kalır ve komşularına sıkı sıkıya yapışırlar. Bir tümör hücresinin kaçması için sıklıkla epitel–mezankimal geçiş (EMT) adlı bir değişimden geçmesi gerekir; bu süreçte sıkı bağlantılarını kaybeder ve hareket edip istila etme yeteneği kazanır. Snail bu dönüşümün kilit sürücüsüdür: çekirdekte bulunduğunda hücre–hücre adezyonunu sağlayan genleri kapatır, hareket ve istila lehine genleri açar. Yüksek Snail düzeyleri agresif kanserler ve kötü hasta sonuçlarıyla ilişkilidir, bu yüzden hücreler normal koşullarda Snail’i az ve kısa ömürlü tutacak yollar geliştirmiştir.
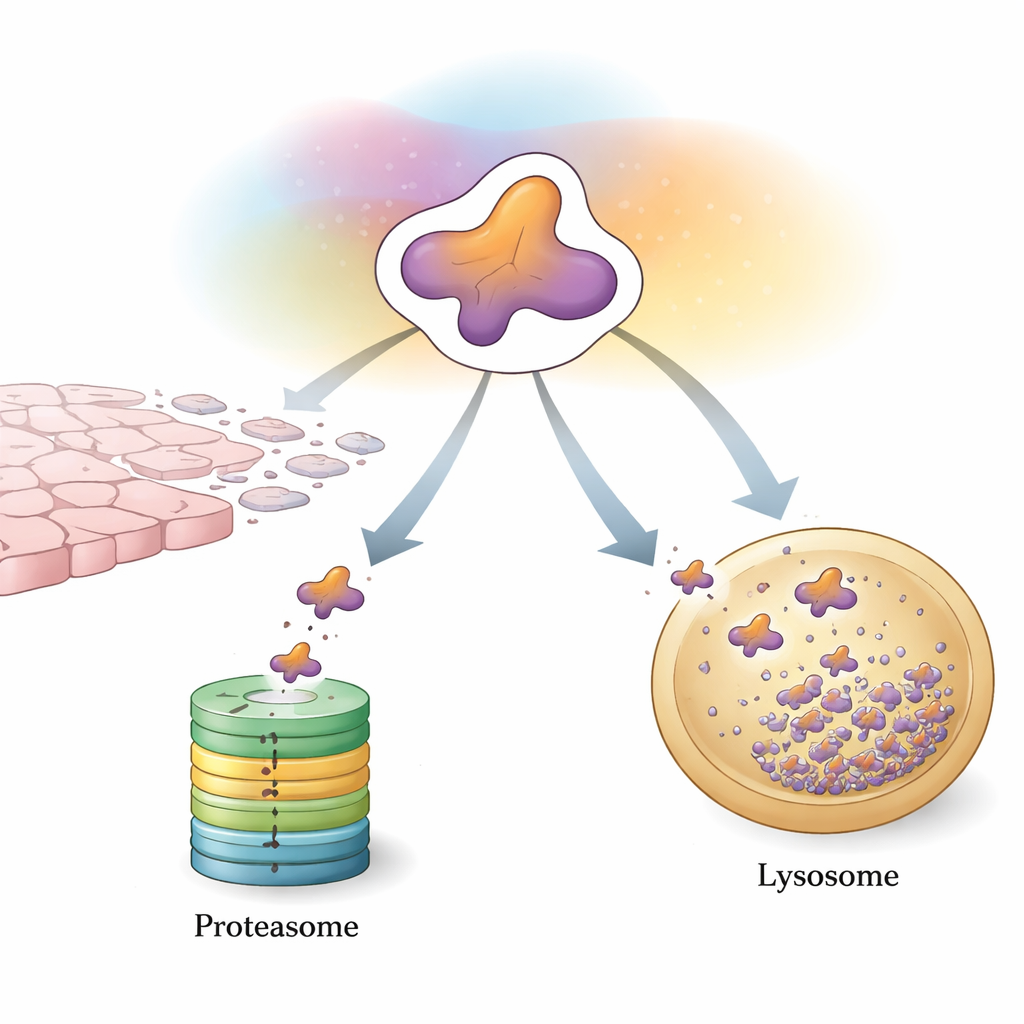
Hücrenin İlk Kontrol Hattı: Etiketle ve Parçala
Hücrelerin Snail’i kontrol etme yollarından biri, istenmeyen proteinler için etiketle ve parçala makinesi olan ubikitin–proteazom sistemidir. Özelleşmiş enzimler, küçük bir protein olan ubikitinden yapılmış “bayrakları” Snail’e ekler. Bu bayraklar belirli bir örüntüde yeterince biriktiğinde, Snail’i bir fıçı şeklindeki kompleks olan proteazoma yönlendirir ve burada parçalara ayrılır. Çok sayıda yardımcı protein bu süreci ince ayarlar. Bazı enzimler Snail’i hızla öğütücüye göndererek yıkımı destekleyen zincirler ekler ve tümör büyümesi ve yayılmasını kısıtlamaya yardımcı olur. Diğerleri ise Snail’i stabilize eden veya dolaylı yoldan gen üretimini artıran zincirler ekleyerek dengeyi EMT ve metastaz lehine kaydırır. Fosforilasyon ve asetilasyon gibi kimyasal değişiklikler, hangi yardımcıların Snail’e bağlanabileceğini ve onun yok edilip edilmeyeceğini kontrol eden ek anahtarlar gibidir.
Frenleri Kaldıranlar: Snail’i Kurtaran Enzimler
Snail’e yıkım etiketi takmakla hikâye bitmez. Deubikitinazlar adı verilen başka bir enzim grubu, ubikitin bayraklarını sökerek Snail’i proteazomdan kurtarabilir. Bu enzimlerin birçoğu kanserlerde etkinleşir veya güçlenir, böylece Snail parçalanmaktan kurtulur ve çekirdekte kalıcı olur. Bu enzimlerin etkileri hücresel bağlama güçlü biçimde bağlıdır: bazı durumlarda doğrudan Snail’i stabilize ederken, diğer durumlarda Snail’in hücre içindeki konumunu veya partner proteinlerle etkileşimini değiştirirler. Büyüme faktörleri ve stres yanıtları gibi kanserle ilişkili yollardan gelen sinyaller bu ağa girdi sağlar ve Snail’in hızlıca ortadan kaldırılıp kaldırılmayacağını veya EMT programını sürdürmesine izin verilip verilmeyeceğini belirler.
İkinci Bir Emniyet Ağı: Hücrenin Geri Dönüşüm Merkezi İçin Seçici Teslimat
Proteazomun ötesinde hücreler, proteinleri parçalanma için asidik keseciklere, lizozomlara taşıyan otofaji yollarına güvenir. Bu derleme, Snail’i kontrol etmede ikinci ana yol olarak şaperon aracılı otofaji (CMA) olarak bilinen yüksek düzeyde seçici bir biçimi vurgular. CMA, Snail içinde kısa bir diziyi tanır ve eşlik eden proteinlerin yardımıyla sitoplazmik Snail’i yıkım için lizozoma teslim eder. Daha az agresif meme kanseri hücrelerinde bu sistem, Snail’i büyük ölçüde çekirdek dışında tutar ve lizozomal ortadan kaldırmaya eğilimli kılar. Daha agresif, üçlü-negatif meme kanserlerinde ise Snail çekirdekte birikme eğilimindedir ve CMA’yı atlatır, bu da EMT ve metastazı tetikleme yeteneğini güçlendirir.
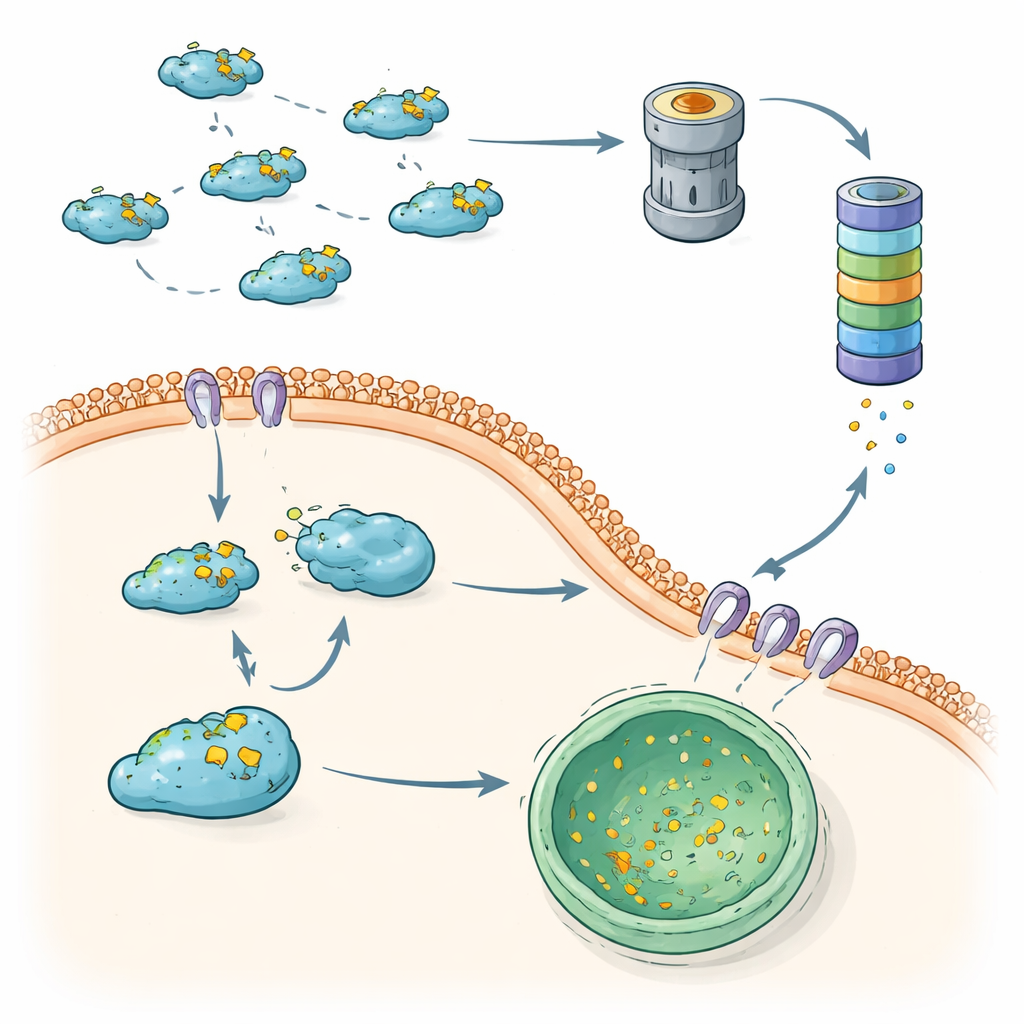
Kalite Kontrol Başarısız Olduğunda Metastaz İlerler
Bir arada ele alındığında bu bulgular, hücrelerin Snail’i dizginlemek için iki tamamlayıcı "kalite kontrol" ekseni kullandığını ortaya koyar: ubikitin–proteazom yolu ve CMA tabanlı lizozomal yıkım. Her iki sistem düzgün çalıştığında Snail hızla söner, EMT’yi sınırlayarak tümör hücrelerinin yayılmasını önlemeye yardımcı olur. Etiketleme enzimleri, deubikitinazlar veya CMA bileşenlerindeki değişikliklerle bu eksenlerden biri zayıfladığında, Snail daha kararlı hale gelir, çekirdekte birikir ve invaziv davranışı güçlü biçimde destekler. Bu birbirine bağlı yıkım yollarını haritalandırarak makale yeni terapötik olasılıkların çerçevesini çizer: Snail yıkımını yeniden sağlayan veya güçlendiren ilaçlar ya da Snail’i yeniden CMA veya proteazomal yok edilme yoluna yönlendiren yaklaşımlar, bu hayati protein geri dönüşüm sistemlerini tamamen kapatmadan metastaz üzerinde frenleri yeniden uygulamaya yardımcı olabilir.
Atıf: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
Anahtar kelimeler: kanser metastazı, epitelyal–mezankimal geçiş, Snail proteini, protein parçalanması, otofaji