Clear Sky Science · tr
UBE2M: Kolorektal adenokarsinomda neddylation ile hücre döngüsü düzenlemesini birbirine bağlayan bir köprü
Bu araştırma bağırsak kanseri için neden önemli
Kolorektal kanser, tüm dünyada en yaygın ve ölümcül kanserlerden biridir; bunun başlıca nedeni tümör hücrelerinin kontrolsüz biçimde bölünmeyi öğrenmesidir. Bu çalışma, kolorektal kanser hücrelerinin hücre bölünmesinin kritik bir kontrol noktasından hızla geçmesini sağlayan daha önce gizli olan bir anahtarı ortaya çıkarıyor. Bu anahtarın moleküler düzeyde nasıl çalıştığını göstermenin yanı sıra mevcut bir antifungal ilacın bunu bozabildiğini göstermesi, tümör büyümesini yavaşlatmaya veya durdurmaya yönelik potansiyel yeni bir yaklaşımı işaret ediyor.
Tümör hücreleri içinde gizli bir kontrol katmanı
Hücreler rastgele bölünmez; DNA’yı kopyalamak ve ikiye bölünmek güvenli mi diye doğrulayan kontrol noktalarının bulunduğu düzenli bir döngüden geçerler. Kanser hücreleri sıklıkla bu kontrol noktalarını bozar. Yazarlar, proteinler üretildikten sonra onları ince şekilde değiştiren neddylation adlı kimyasal etiketleme sürecine odaklandı. Önceki çalışmalar neddylation’ın birçok kanserde daha aktif olabileceğine işaret etmişti, ancak bunun kolorektal kanser hücrelerinin bölünme döngüsüyle nasıl bağlantılı olduğu belirsizdi. İnsan tümörlerinden elde edilen büyük tek hücre veri setleri ve 1.800’den fazla hastanın toplu gen ifade verilerini kullanarak ekip, neddylation aktivitesinin hücre bölünmesinden önceki son kapı olan G2/M evresinde bulunan malign bağırsak hücrelerinde özellikle yüksek olduğunu buldu.
Moleküler bir “köprü” proteine odaklanma
Neddylation’ı hücre bölünmesine bağlayan molekülleri belirlemek için araştırmacılar, binlerce geni elemek üzere ağ tarzı hesaplamalı analizler kullandı. Bir protein öne çıktı: küçük NEDD8 etiketini diğer proteinlere bağlamaya yardımcı olan bir enzim olan UBE2M. UBE2M verilerde yalnızca neddylation ve hücre döngüsü yollarıyla güçlü bir bağlantı göstermedi; aynı zamanda kolorektal tümörlerde çevre normal dokudan çok daha yüksek düzeylerde bulundu. Tümörlerinde daha yüksek UBE2M bulunan hastaların hayatta kalma oranları genellikle daha kötüydü; bu da UBE2M’yi yolcu değil olası bir sürücü olarak işaretliyor. Ekip UBE2M’yi kanser hücre hatlarında ve fare tümör modellerinde azalttığında, tümör büyümesi yavaşladı, hücre bölünmesi azaldı ve daha fazla hücre programlı hücre ölümü geçirdi. Buna karşılık, hücrelere ekstra UBE2M üretmeleri zorlandığında büyüme ve hücre döngüsü ilerlemesi hızlandı.
Büyümeyi destekleyen ana proteini koruyan bir röle
Daha derine inen bilim insanları, UBE2M’nin hücrelerin bölünmesine nasıl yardımcı olduğunu sordular. UBE2M’nin tek başına hareket etmediğini, aksine USP39 ve PABPC1 adlı iki başka proteini içeren bir röleyi başlattığını keşfettiler. Normalde PABPC1, ubiquitin etiketleri zinciriyle işaretlenir ve hücrenin protein geri dönüşüm mekanizmasına gönderilerek yok edilir. Ekip, UBE2M’nin USP39’u NEDD8 etiketiyle kimyasal olarak modifiye ettiğini gösterdi. Bu modifikasyon, USP39’un PABPC1 üzerindeki ubiquitin zincirlerini kesme yeteneğini artırarak PABPC1’i yok olmaktan kurtarıyor ve onu daha kararlı hale getiriyordu. Daha fazla PABPC1 olduğunda, hücre belirli haberci RNA’ları proteinlere çevirme konusunda daha yetkin hale geliyor; bunların arasında G2/M kontrol noktası için bir gaz pedalı görevi gören siklin olan CCNB1 mRNA’sı da var. Özetle UBE2M, PABPC1’i stabilize ederek CCNB1 üretimini artırıyor ve böylece hücrelerin bölünmeye daha kolay girmesini sağlıyor.
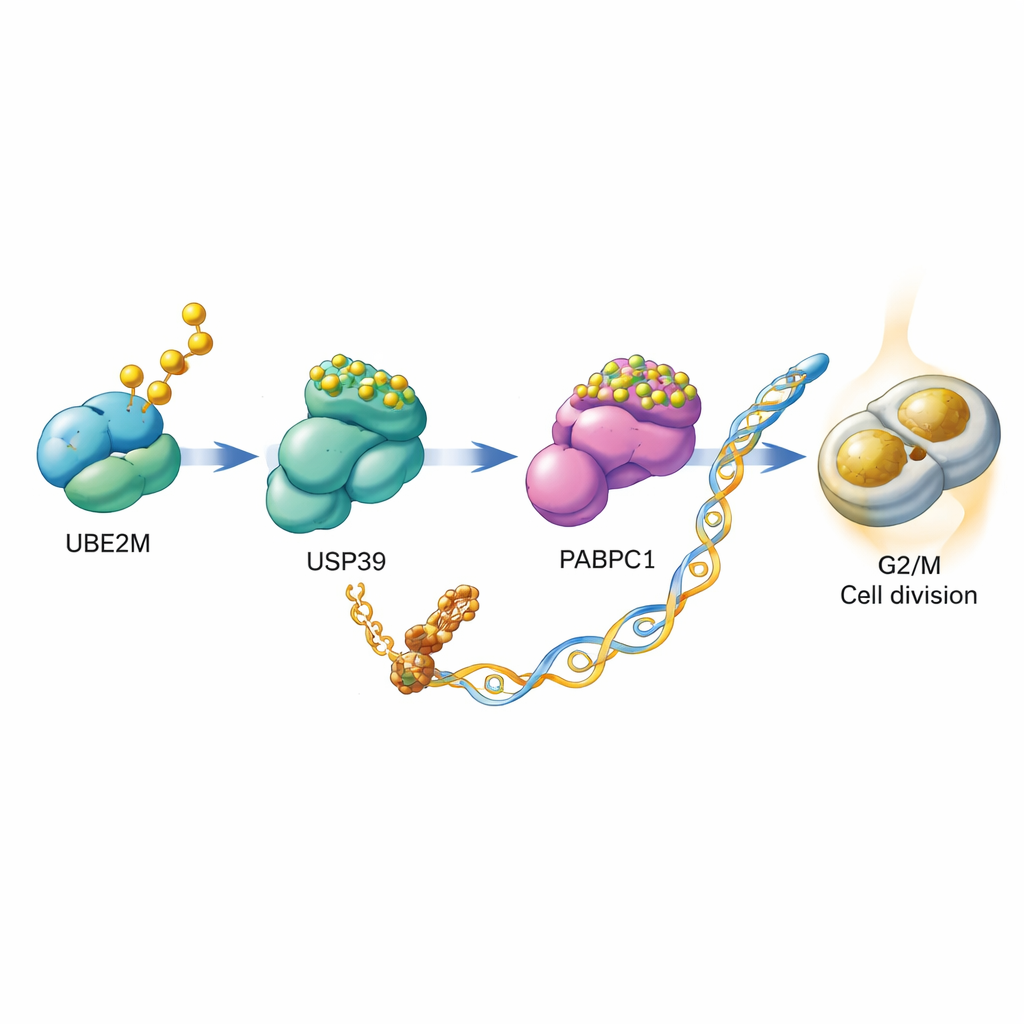
Moleküler mekanizmadan ilaç fırsatına
UBE2M–USP39–PABPC1–CCNB1 zincirinin keşfi, kolorektal kanser hücrelerinde yeni bir zayıf halka olduğunu öne sürdü. Yazarlar, zaten mantar enfeksiyonlarını tedavi etmek için kullanılan ve yakın zamanda UBE2M’nin neddylation aktivitesini inhibe edebilen bir ilaç olarak tanımlanan mikafungine yöneldiler. Laboratuvarda yetiştirilen bağırsak kanseri hücrelerinde mikafungin, USP39 neddylation’ını zayıflattı, PABPC1’in yıkımını artırdı ve CCNB1 protein düzeylerini düşürdü. Sonuç olarak hücre bölünmesi yavaşladı, daha fazla hücre G2/M kontrol noktasında takıldı ve apoptoz (programlı hücre ölümü) arttı. Kolorektal kanser hücreleri nakledilmiş farelerde, günlük mikafungin tedavisi, UBE2M’yi ortadan kaldırmaya gerek kalmadan, tedavi edilmeyen hayvanlarla karşılaştırıldığında tümörleri önemli ölçüde küçülttü.
Uzun vadede hastalar için ne anlama geliyor
Bu çalışma, tek bir enzim olan UBE2M’nin nasıl ince bir protein etiketleme sistemini bağırsak kanseri hücresinin bölünme kararına bağlayabildiğini açıkça gösteriyor. UBE2M, USP39 aracılığıyla bir çeviri faktörünü (PABPC1) stabilize ederek dolaylı olarak güçlü bir hücre döngüsü sürücüsü olan CCNB1 düzeylerini yükseltiyor ve tümörlerin daha hızlı büyümesine izin veriyor. Daha fazla araştırma ve klinik test gerekli olmakla birlikte, bulgular bu röleyi engellemenin—örneğin mikafungin gibi yeniden kullanılabilecek ilaçlarla—kolorektal kanserin ilerlemesini yavaşlatmaya ve hasta sonuçlarını iyileştirmeye yönelik yeni bir hedeflenmiş strateji sunabileceğini öne sürüyor.
Atıf: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
Anahtar kelimeler: kolorektal kanser, hücre döngüsü, neddylation, UBE2M, hedefe yönelik tedavi