Clear Sky Science · tr
İnsan Hastalıklarında Deaminasyon Yoluyla İki RNA Düzenleme Kodu
Hücrelerin Kendi Mesajlarını Nasıl Yeniden Yazdığı
Vücudunuzdaki her hücre, sizi inşa etmek ve sürdürmek üzere DNA’dan sürekli talimatlar okur. On yıllar boyunca bu talimatların RNA’ya kopyalandığını ve ardından sadakatle proteinlere çevrildiğini varsaydık. Bu derleme makale, hikâyenin çok daha katı olmadığını gösteriyor: hücreler aslında oluşturulduktan sonra birçok RNA mesajını “yeniden yazar”, tek tek kimyasal harfleri değiştirir ve bunun vücudumuzun işleyişini ince ya da dramatik biçimde etkileyebileceği görülür. Bu gizli düzenleme katmanını anlamak, otoimmün hastalıklar, nörolojik bozukluklar, metabolik problemler, enfeksiyonlar ve kanserin neden geliştiğini ve bunları nasıl tedavi edebileceğimizi açıklamaya yardımcı olur.
Tek Harfi Değiştirmenin İki Yolu
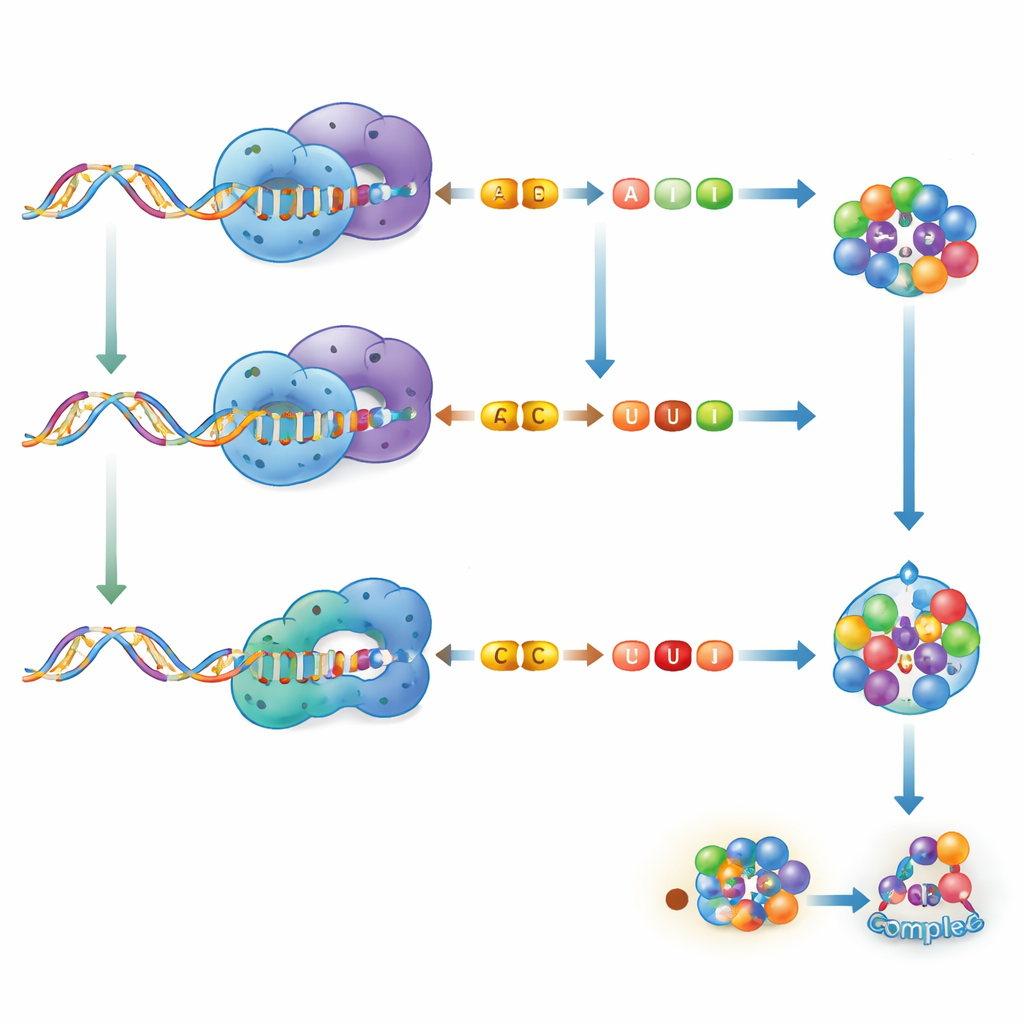
Yazarlar, insanlarda bulunan iki ana RNA düzenleme türüne odaklanıyor. Birincisi ADAR olarak bilinen enzimlerin gerçekleştirdiği A-to-I (A’dan I’ye) düzenlemedir. Bunlar adenosini (A) inosine (I) olarak değiştirir; hücresel mekanizma bunu çoğunlukla guanosin (G) gibi okur. Diğeri APOBEC ailesi enzimlerinin yürüttüğü C-to-U (C’den U’ya) düzenlemedir; bunlar sitidini (C) uridinə (U) dönüştürür. Her iki süreç de tek bir bazdan küçük bir kimyasal grup çıkarır, ancak etki yerleri, tercih ettikleri RNA’lar ve RNA yapısını yeniden şekillendirme güçleri bakımından farklılık gösterir. A-to-I düzenleme sıklıkla RNA zincirlerinin eşleşme biçimini değiştirir, protein çeşitliliği yaratabilir veya diğer moleküllerin RNA’ya bağlanma şeklini değiştirebilir. C-to-U düzenleme yapısal olarak genellikle daha ince etkiler yapma eğilimindedir, ancak yine de durdurma sinalleri ekleyebilir, protein dizilerini ince ayarlayabilir veya RNA’nın düzenleyici bölgelerini hassaslaştırabilir.
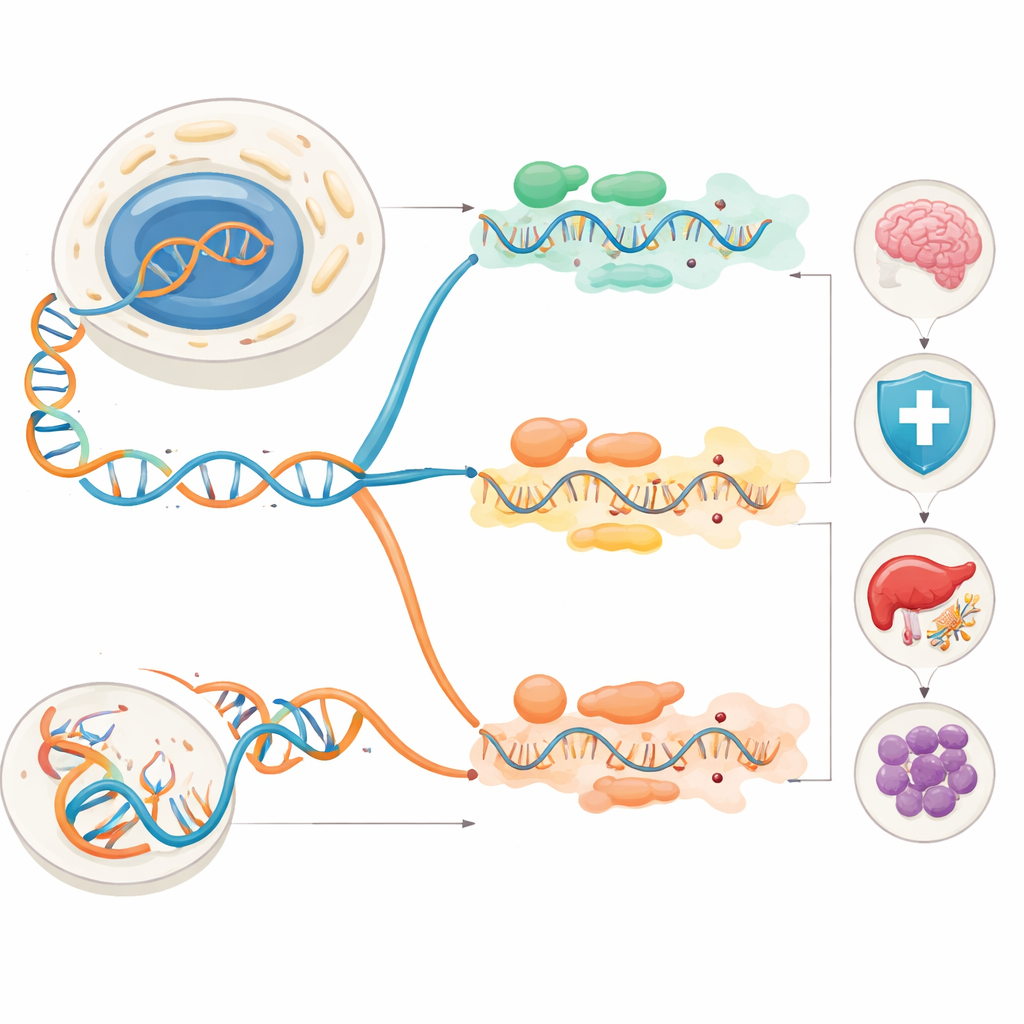
Düzenlenmiş Mesajlardan Sağlık ve Hastalığa
Bu düzenleme olayları protein parçalarını veya çevrelerindeki düzenleyici bölgeleri değiştirebileceği için normal biyolojinin pek çok yönünü etkiler. İmmün sistemde ADAR1, hücrelerin kendi yaptığı çift sarmallı RNA’ları düzenleyerek viral algılayıcıların onları yabancı olarak yanlış tanımasını engeller. ADAR1 başarısız olduğunda, bağışıklık alarmları sürekli “açık” kalır ve kronik interferon sinyallemesine, Aicardi–Goutières sendromu gibi otoimmün durumlara yol açar. APOBEC enzimleri de immün hücrelerde RNA düzenler; makrofajların stres ve iltihaba tepkisini şekillendirir ve sistemik lupus gibi hastalıklara katkıda bulunabilir. Sinir sisteminde ADAR2 düzenlemesi, kalsiyum akışını kontrol eden beyin reseptörlerinin ayarlanması için kritik öneme sahiptir; bu düzenleme yoksa farelerde nöbetler görülür ve erken ölümler olur. APOBEC kaynaklı düzenleme belirli nöron reseptör RNA’larını etkileyerek duyarlılığı artırabilir ve epilepsi, dejenerasyon ile bilişsel sorunlarla ilişkilidir.
Virüsler, Metabolizma ve Kanser Bağlantısı
RNA düzenleme, virüslerle etkileşimimizi, enerji yönetimini ve kanser gelişimini de etkiler. ADAR1 viral genomları doğrudan düzenleyebilir; bazen virüsü zayıflatır, bazen de hepatit delta virüsünde olduğu gibi yaşam döngüsünün tamamlanmasına yardımcı olur. Retrovirüslere saldırmasıyla ünlü APOBEC enzimleri, SARS-CoV-2 RNA’sında güçlü bir C-to-U izi bırakır; bu hem virüsü sınırlarken hem de viral evrim için yararlı olabilecek mutasyonlar üretir. Metabolizmada ADAR2, pankreatik beta hücrelerinin diyete yanıt olarak insülin salgısını ayarlamasına yardımcı olurken, ADAR1 ve ADAR2 aktivitesi diyabet riski ve karaciğer yağlanmasını etkiler. APOBEC1’in klasik rolü, apolipoprotein B RNA’sını düzenleyerek diyet yağlarının taşınması için gerekli kısa bir protein üretmektir; bu düzenleme eksik olduğunda farelerde ciddi lipid ve kolesterol sorunları gelişir.
Düzenlenmiş RNA Tümörleri Nasıl Şekillendirir
Bizi koruyan aynı enzimler yanlış düzenlendiğinde kanseri de tetikleyebilir. Büyük kanser dizileme projeleri on binlerce A-to-I düzenleme sitesi ve yaygın APOBEC ile ilişkili mutasyonlar ortaya koydu. Meme kanserinde ADAR1 düzenlemesi, hedef RNA’ya bağlı olarak tümör davranışını ya teşvik edebilir ya da sınırlayabilir; hücre istila, metastaz ve hayatta kalmayı etkiler. Ölümcül bir beyin tümörü olan glioblastomada ADAR1 kanser kök hücrelerini desteklerken, ADAR2 genellikle hem protein kodlayan RNA’ları hem de kanseri teşvik eden mikroRNA’ları düzenleyerek büyümeyi frenler. Lösemilerde ADAR1 sıklıkla malign kök-hücre benzeri popülasyonları artırır ve tümör baskılayıcı mikroRNA’ları azaltırken, ADAR2 belirli hedefleri düzenleyerek hastalığı yavaşlatır. APOBEC kaynaklı C-to-U düzenleme, kanserli kan hastalıklarında belirli RNA’larda ya hastalığı kötüleştirebilir ya da hastane sonuçlarını iyileştirebilir; bu da bu değişikliklerin bağlama güçlü şekilde bağımlı olduğunu vurgular.
Cevapsız Sorular ve Gelecekteki Olanaklar
Kataloglanan düzenleme sitelerinin patlamasına rağmen, bilim insanları anlamlı düzenlemeleri arka plan gürültüsünden ayırmakta hâlâ zorlanıyor. Tespit edilen birçok değişiklik az etkili olabilir, ancak azınlık bir grup açıkça hücreler ve organizmalar için hayati sonuçlar doğuruyor. Yazarlar, gelecekteki çalışmaların hangi enzimlerin ve yardımcı proteinlerin bireysel siteleri kontrol ettiğini belirlemesi gerektiğini ve ardından bu tek bazların her zaman düzenlenmiş veya asla düzenlenmemiş hale getirildiğinde neler olduğunu test etmesi gerektiğini savunuyor. Bu tür çalışmalar RNA düzenlemenin belirli hastalıklara nasıl katkıda bulunduğunu netleştirecek ve düzenleme desenlerini ayarlamanın aşırı aktif bağışıklığı sakinleştirmek, beyin devrelerini ince ayarlamak, metabolik dengesizlikleri düzeltmek veya kanserleri tedaviye karşı daha hassas hale getirmek için yeni bir hassas tedavi sınıfı olup olamayacağını ortaya koyacaktır.
Günlük Sağlık İçin Neden Önemli
Basitçe söylemek gerekirse, bu makale hücrelerimizin sadece genetik kodu okumadığını; iki paralel “düzenleme kodu” kullanarak RNA aşamasında etkin bir şekilde düzeltme ve revizyon yaptığını gösteriyor. Bu küçük düzenlemeler doğru yerde ve miktarda gerçekleştiğinde bağışıklık sistemimizi dengede, beyinlerimizi istikrarlı, metabolizmamızı esnek ve virüslere karşı savunmalarımızı keskin tutmaya yardımcı olur. Düzenleme mekanizması aşırı aktif, yanlış yerde veya bozuk olduğunda, aynı değişiklikler bizi otoimmüniteye, enfeksiyona, demansa, metabolik hastalığa veya kanserlere savurabilir. Bu tek harflik yeniden yazmaları haritalayarak ve anlayarak, bilim insanları hastalıkları daha erken teşhis etmeyi, kimin risk altında olduğunu tahmin etmeyi ve nihayetinde düzenleme sürecini sağlığa doğru yönlendirecek tedaviler tasarlamayı umuyor.
Atıf: Min, D.J., Lee, S., Lee, Ys. et al. Two codes of RNA editing by deamination in human diseases. Exp Mol Med 58, 382–395 (2026). https://doi.org/10.1038/s12276-025-01633-8
Anahtar kelimeler: RNA düzenleme, ADAR, APOBEC, otoimmünite, kanser