Clear Sky Science · sv
Ultrasensitiv detektion av Alzheimer’s sjukdomsmarkörer med nanopelar‑fotonic crystal‑biosensorer
Varför ett enkelt blodtest för minnesförlust spelar roll
När nya läkemedel dyker upp som kan bromsa Alzheimers sjukdom behöver läkare snabbt enkla tester som visar vem som löper risk långt innan symtomen blir tydliga. Idag innebär en bekräftelse av Alzheimer vanligtvis dyra hjärnavbildningar eller lumbalpunktioner som få får i rutinvård. Denna studie beskriver en liten ljusbaserad sensor som kan upptäcka centrala Alzheimer‑relaterade molekyler i en bloddroppe vid kliniskt meningsfulla nivåer, vilket potentiellt banar väg för snabba, lågkostnadstester som kan användas i vardagliga kliniker eller till och med vid sängkanten.
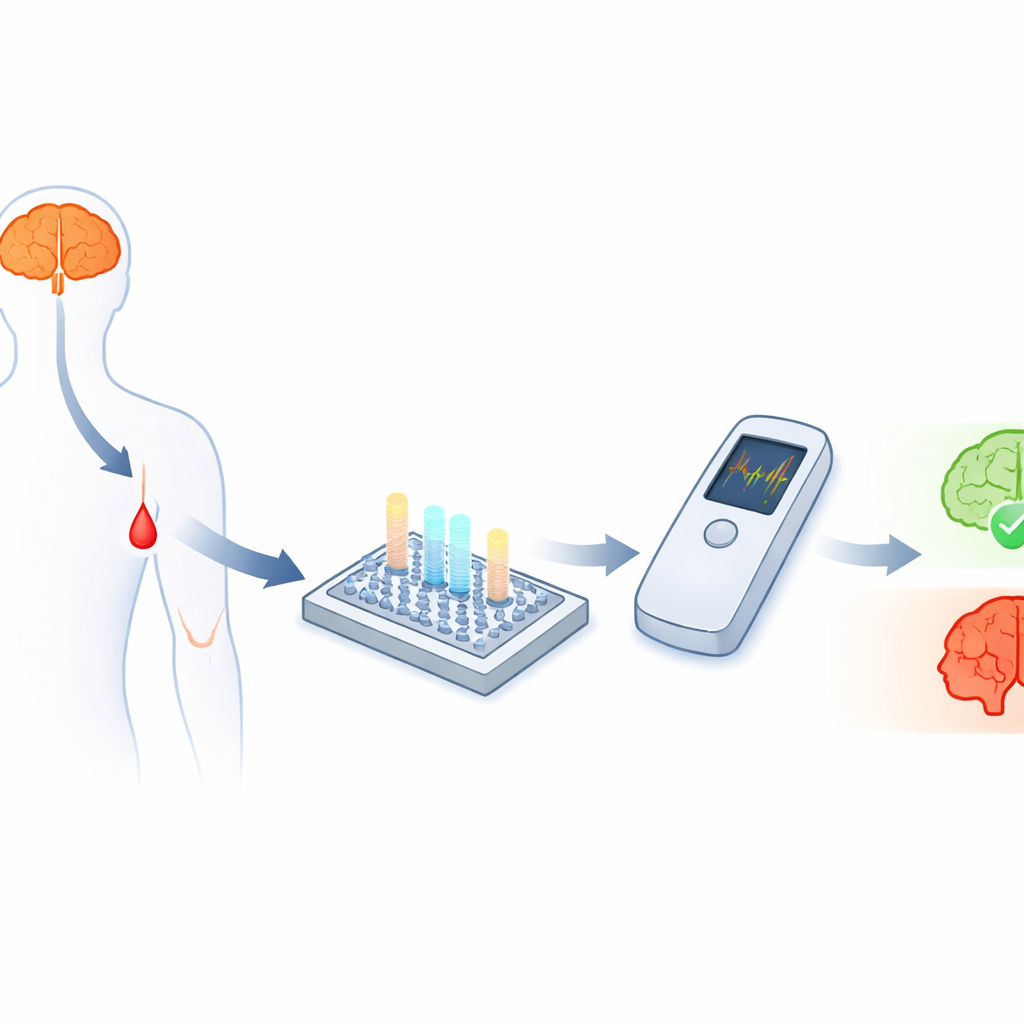
Söker ledtrådar i blodet
Alzheimers sjukdom är starkt kopplad till små proteinfragment kallade amyloid‑beta, särskilt två former kända som Aβ40 och Aβ42. Deras mängder, och särskilt deras kvot, bär viktiga ledtrådar om sjukdomen är närvarande och hur den utvecklas. Utmaningen är att dessa fragment är mycket små och cirkulerar i blodet på extremt låga nivåer — triljondelar av ett gram per milliliter — vilket gör dem mycket svåra att mäta noggrant utanför specialiserade laboratorier. Även om elektrokemiska sensorer i princip kan detektera sådana låga koncentrationer har det visat sig svårt att omvandla dem till robusta, prisvärda punkt‑av‑vård‑tester som kan spåra flera markörer samtidigt.
Vägleda ljus genom små pelare
Teamet tacklade denna utmaning med hjälp av nanofotonik — strukturer som kontrollerar ljus på en skala mindre än våglängden för ljuset. De byggde ett chip täckt av ett regelbundet gitter av parvisa, hårfint tunna kiselpelare på glas. När ljus träffar denna mönstrade yta fångas det i ett särskilt resonansläge som är extremt känsligt för förändringar nära pelartopparna, ungefär som tonen hos en stämgaffel ändras om material läggs till. Genom att noggrant justera avståndet mellan pelarna i varje par balanserade forskarna tre avgörande egenskaper samtidigt: hur skarpt definierad den optiska resonansen är, hur starkt den ändrar sig med omgivningen och hur stor signal den producerar. Denna ”sweet spot”‑design gör chippet särskilt väl lämpat för att känna av mycket små mängder material.
Göra osynliga molekyler synliga
Även med denna optimerade design skulle Alzheimer‑markörerna på egen hand knappt påverka ljuset. För att förstärka effekten använde forskarna en sandwich‑strategi med guldnanopartiklar. Först belade de sensorsytan med lager av klibbig kemi som orienterar specialiserade antikroppar så att deras bindningsställen pekar in i vätskan. Dessa antikroppar fångar antingen Aβ40 eller Aβ42 från provet. Därefter strömmar man guldnanopartiklar, vardera dekorerad med en andra antikropp som känner igen en annan del av samma amyloidfragment, över chippet. När ett amyloidfragment finns närvarande bildar det en bro mellan ytan och en guldpartikel, vilket effektivt ”flaggar” dess närvaro. Eftersom guld starkt påverkar den lokala optiska miljön ger varje fångat fragment en mycket större förskjutning i sensorresonansen än peptiden ensam, vilket ökar känsligheten med ungefär en till två storleksordningar samtidigt som en ren optisk signal bibehålls.
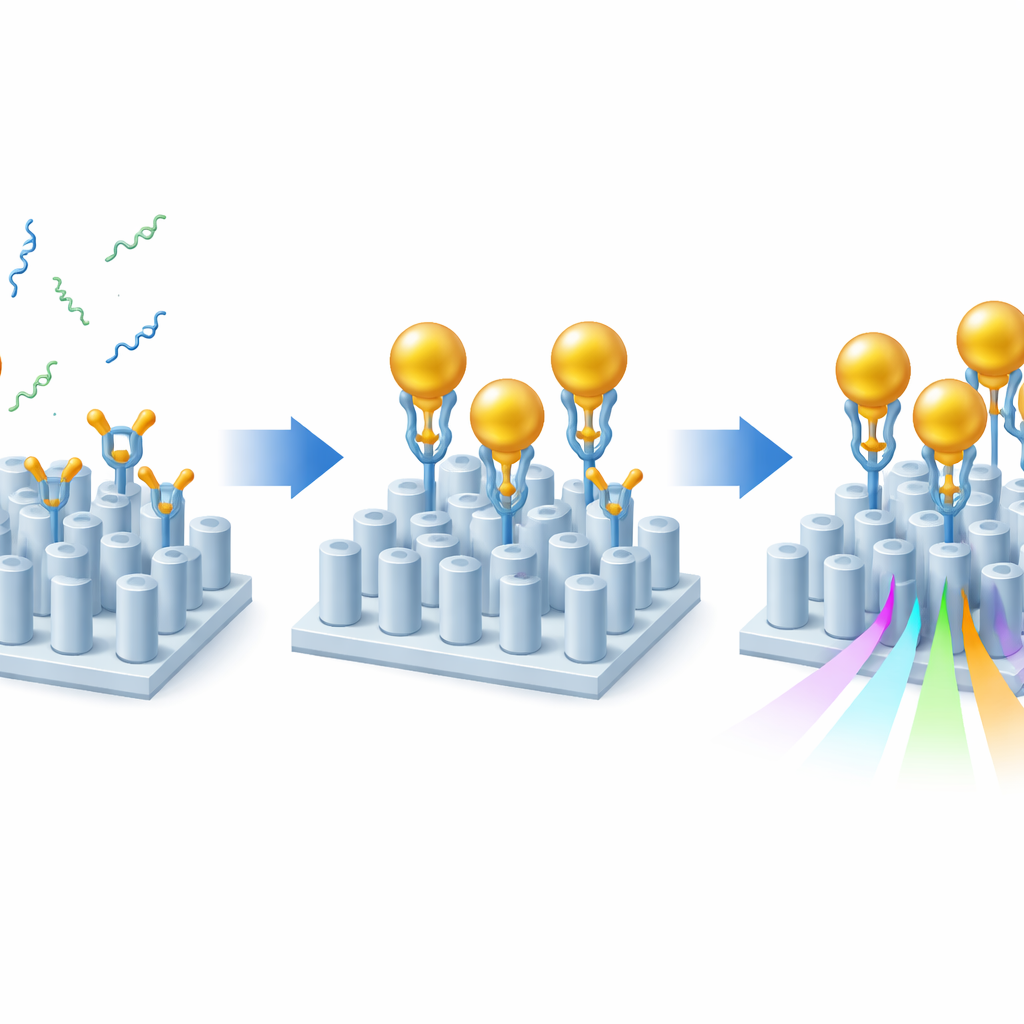
Testa realistiska prover
För att visa att tillvägagångssättet fungerar bortom enkla laboratoriebuffrar testade teamet sensorn med mänskligt blodserum. De spädde serum för att göra det kompatibelt med mikrofluidisk hantering men behöll amyloidnivåerna representativa för dem som finns hos patienter. Viktigt är att de kunde detektera både Aβ40 och Aβ42 vid 0,2 pikogram per milliliter i detta utspädda serum — motsvarande den kliniskt relevanta nivån 20 pikogram per milliliter i helblod. Genom att placera olika capture‑antikroppar i separata områden på samma chip mätte de båda formerna av amyloid samtidigt inom en enda liten kanal, ett viktigt steg mot att bedöma deras kvot från ett enda litet prov. Signalerna skiljde tydligt prover som spikats med extra amyloid från de som endast innehöll de naturliga bakgrundsnivåerna som finns även hos friska personer.
Vad detta kan betyda för framtida vård
Tillsammans visar dessa framsteg att en kompakt, ljusbaserad sensor, förstärkt med guldnanopartiklar, kan nå de känsligheter som krävs för meningsfulla Alzheimer‑blodtester samtidigt som den hanterar mer än en markör åt gången. Även om mer arbete krävs för att omvandla detta till en robust kommersiell apparat och för att lägga till andra markörer som former av tau‑proteinet, är den underliggande tekniken byggd av skalbara material och kan kopplas till enkel, handhållen optik. Om den utvecklas fullt ut skulle den kunna göra det möjligt för kliniker att övervaka hjärnhälsa med endast ett litet blodprov, vilket gör det mycket enklare att upptäcka Alzheimer tidigt och att följa hur väl behandlingar fungerar över tid.
Citering: Guilherme S. Arruda, Katie Morris, Augusto Martins, Yue Wang, Sian Sloan-Dennison, Duncan Graham, Steven D. Quinn, Emiliano R. Martins, and Thomas F. Krauss, "Ultrasensitive Alzheimer’s disease biomarker detection with nanopillar photonic crystal biosensors," Optica 12, 1587-1596 (2025). https://doi.org/10.1364/OPTICA.566672
Nyckelord: Alzheimers blodtest, nanofotonisk biosensor, amyloid beta, guldnanopartiklar, tidig diagnostik