Clear Sky Science · sv
Den kvartära strukturens ursprung till fibrilleringen av sickle-hemoglobin: en molekylär dynamikstudie
Varför den här blodberättelsen är viktig
Sickle cell–sjukdom börjar med en liten förändring i ett blodprotein, men kan ändå omforma röda blodkroppar, blockera kärl och ge livslång smärta. Denna studie undersöker, utifrån fysikens principer, hur just den enda förändringen får proteinet hemoglobin att staplas till styva fibrer inne i cellen. Genom avancerade datorbaserade simuleringar kopplar författarna atomära detaljer till hela cellers problem och ger nya ledtrådar för hur framtida läkemedel skulle kunna hindra hemoglobin från att fastna i vårt blodomlopp.
En liten utbyte med stora följder
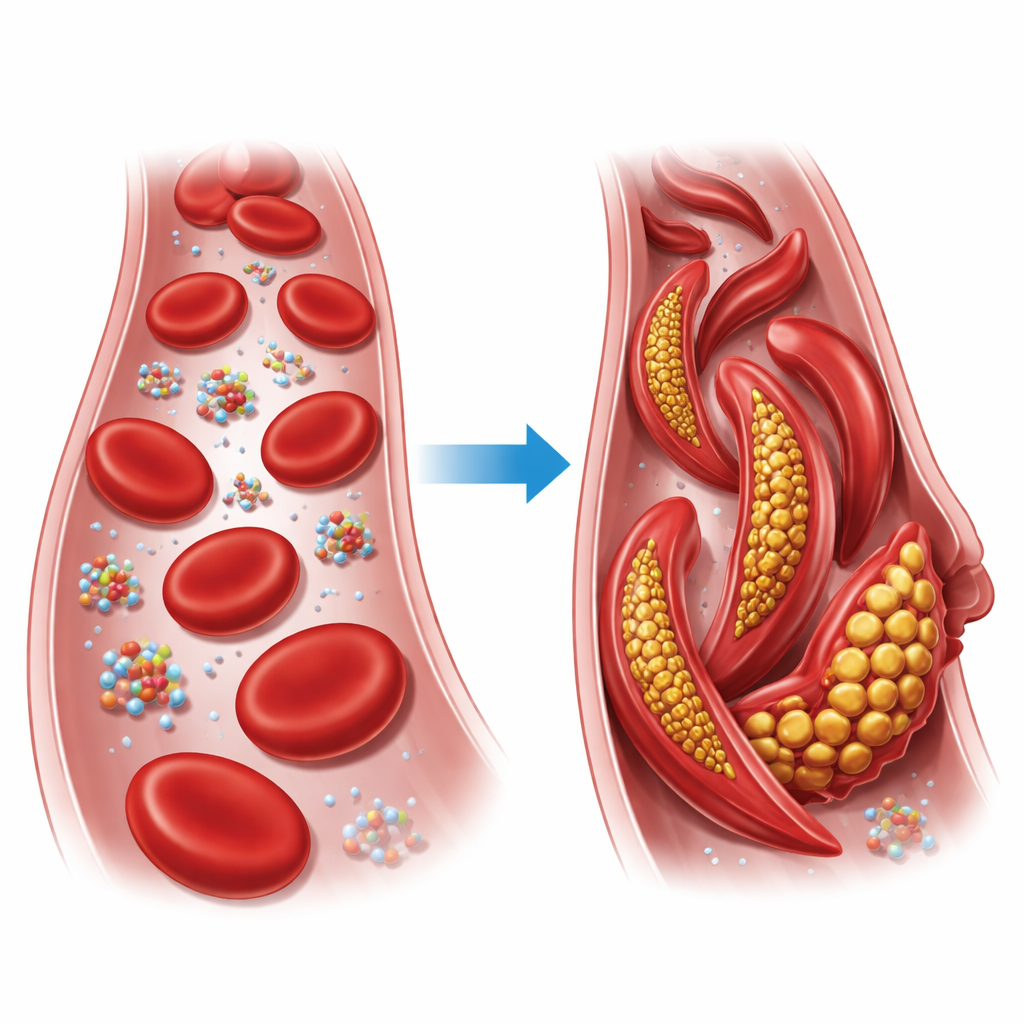
Hemoglobin är syrebindande proteinet som fyller våra röda blodkroppar. Varje hemoglobinmolekyl byggs av fyra kedjor som kan ordna sig i två huvudkonformationer, kallade den relaxerade (R) och den spända (T) staten. Vid sickle cell–sjukdom byts bara en byggsten i en av dessa kedjor ut: en laddad glutamat ersätts av en fettliknande valin vid position sex i betakedjan. Vid låga syrenivåer länkar denna förändrade form, kallad sickle-hemoglobin, ihop sig till långa fibrer som förvränger normalt runda röda blodkroppar till stela, sickle-liknande former, vilka kan täppa igen små kärl och beröva vävnader syre.
Att följa hemoglobinets formskiftningar
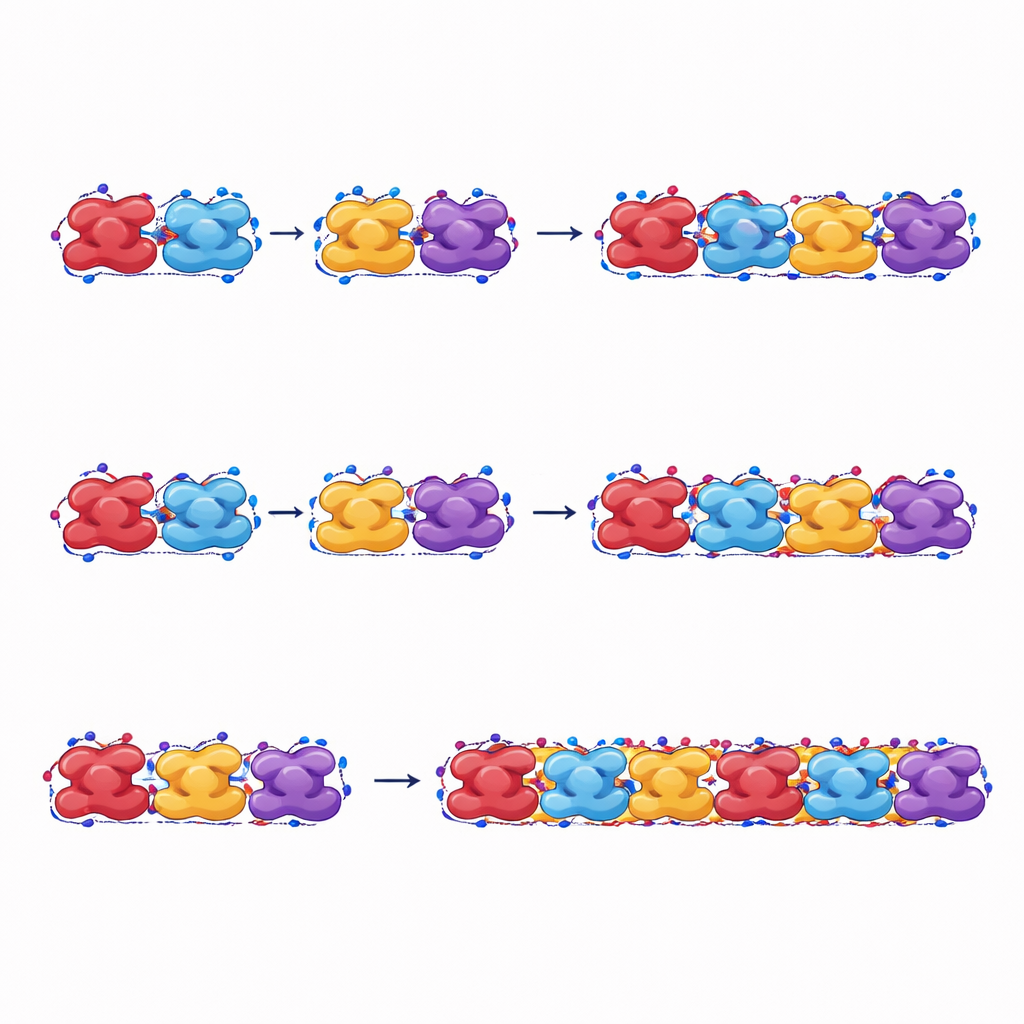
Författarna fokuserar på hur hela hemoglobinheter roterar och packas ihop i en fiber. De följer denna storskaliga formändring med en enda vinkel som mäter hur två halvor av proteinet vrider sig i förhållande till varandra. Genom molekylär dynamik-simuleringar—virtuella experiment som beräknar hur atomer rör sig över tid i vatten och salt—pressar de försiktigt denna vinkel över ett brett spektrum och beräknar hur mycket energi varje form kräver. De finner att både normalt och sickle-hemoglobin kan utforska många sådana former vid kroppstemperatur. Sickle-hemoglobin visar en svag preferens för en viss vinkel, men dessa formpreferenser räcker inte ensamt för att förklara varför det endast är sickle-varianten som bildar stabila fibrer.
Varför sickle-fibrer håller ihop medan normala faller sönder
För att nå kärnan i fibrilleringen mäter studien hur starkt intilliggande hemoglobinheter attraherar varandra längs och tvärs fibern. Teamet beräknar den kohesiva energin—det resulterande draget som håller enheterna ihop—för många olika övergripande former. För sickle-hemoglobin förblir denna kohesiva energi negativ (det vill säga attraktiv) över hela det undersökta formintervallet, så fibrerna förblir stabila och faller inte lätt isär. För normalt hemoglobin däremot har vissa former faktiskt positiv kohesiv energi, vilket gör fibrer vid dessa vinklar instabila och benägna att spontant gå sönder. En nyckelskillnad är hur de muterade valin-sidokedjorna trycks in mot närliggande proteiner: i sickle-hemoglobin bildar dessa fettiga ytor robusta kontakter både i sidled och längs fiberaxeln, vilket direkt gynnar fiberbildning.
Hur dessa fibrer bär last och går sönder
Författarna töjer också sina simulerade fibrer för att efterlikna mekanisk belastning. När de dras längs sin längd tål fibrer gjorda av sickle-hemoglobin högre krafter och töjningar och dissipera mer energi innan brott än fibrer gjorda av normalt hemoglobin. Även den relaxerade formen av sickle-fibrer, som inte är den form där fibrer först uppträder, kan ändå behålla kedjan genom plastiska formförändringar och därigenom hjälpa till att hålla fibern intakt när den väl bildats. Fibrer av normalt hemoglobin separerar däremot lättare mellan intilliggande enheter och absorberar mindre energi innan brott, vilket bekräftar att de är mindre stabila under belastning.
Ledtrådar för framtida behandlingar och nya material
Sammanslaget visar simuleringarna att en enda aminosyreförändring omformar hur hemoglobinenheter möts, vrider den övergripande sammankopplingen till vinklar som gynnar stark attraktion, särskilt i den spända staten. Denna kombination av geometri och vidhäftighet gör att sickle-hemoglobin kan bilda långa, styva fibrer som motstår både termisk rörelse och mekaniskt drag, vilket i förlängningen deformerar röda blodkroppar och blockerar blodflödet. Genom att peka ut specifika drag i den övergripande proteinarrangemanget som styr fiberstabilitet antyder arbetet att effektiva antisickling-läkemedel skulle kunna verka genom att knuffa hemoglobin mot former där fibrer blir energimässigt ofördelaktiga och mekaniskt sköra—och därmed förvandla en dödlig molekylär kö till ett åter frittflytande blodström.
Citering: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
Nyckelord: sickle cell disease, hemoglobin fibers, protein aggregation, molecular dynamics, blood disorders