Clear Sky Science · sv
Dynamin optimerar protein-membran-interaktioner för fission
Hur celler prydligt nypper av sina egna membran
Varje sekund är dina celler upptagna med att nypa av pyttesmå membranblåsor för att transportera last, omforma interna fack och bekämpa virus. Denna till synes enkla handling — att dela ett smalt membranrör i två bitar — visar sig vara förvånansvärt svår ur ett fysikaliskt perspektiv. Denna artikel ställer en bedrägligt grundläggande fråga: hur gör ett protein kallat dynamin membranskärelser möjlig och pålitlig, och vilka egenskaper hos proteinet är verkligen nödvändiga för uppgiften?
De cellulära nyporna i arbete
Dynamin är en molekylär maskin som bildar en krage runt tunna membranrör och drar ihop sig som en snara för att hjälpa dem att gå av. Sådana fissionstillfällen ligger bakom processer som endocytos, där celler tar in material, liksom delningen av interna strukturer som mitokondrier. Om ett membranrör lämnas oangripet motstår det starkt att brytas, eftersom det först måste klämmas ner till nästan membranets egen tjocklek och passera genom ett instabilt mellanläge. Detta energimässiga hinder är mycket högre än den slumpmässiga kinetiska energin som finns i en cell, så specialiserade fissionsproteiner som dynamin är avgörande.
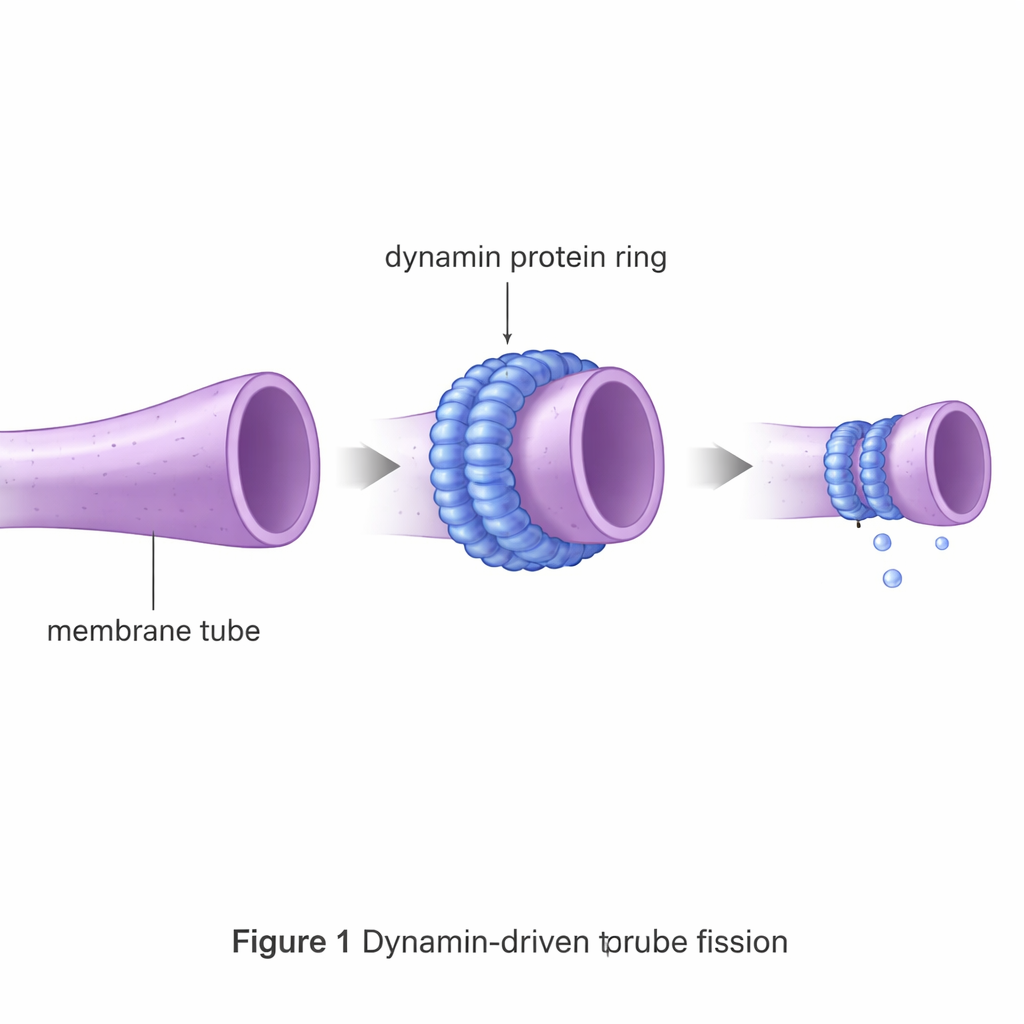
Använder virtuella membran för att testa proteindesigner
Att direkt iaktta det kritiska ögonblicket när ett rör brister är extremt svårt i experiment: snabb avbildning saknar molekylär detalj, och högupplösta metoder fryser systemet i tiden. För att överbrygga denna klyfta använder författarna ett kraftfullt teoretiskt verktyg kallat själv-konsistent fälttheori. Istället för att följa varje atom beskriver de lipider och lösningsmedel som flexibla kedjor som känner av jämnt varierande fält. Proteiner introduceras inte som fulla atomstrukturer utan som torusformade externa potentialer som antingen helt enkelt utesluter utrymme, fäster vid membranytan eller tränger in i det yttre lagret. Med detta ramverk kan de beräkna både de resulterande membranformerna och den fulla frienergi-kostnaden för att gå från ett intakt rör till fissionsmellanläget.
Vilken typ av grepp hjälper ett rör att brytas?
Gruppen varierar systematiskt hur ett dynamin-liknande protein interagerar med membranet. Vissa modellproteiner tränger bara ihop ytan och fungerar som ett stelt manschett; andra är måttligt eller starkt klibbiga mot de yttre huvudgrupperna; ytterligare andra imiterar det verkliga dynamin PH-domänen genom att infoga hydrofoba delar i det yttre skiktet och "splayar" huvudgrupperna åt sidan. För varje fall undersöker de tre sammankopplade kvantiteter: hur starkt proteinet binder till ett okomprimerat rör, hur mycket kurvatur och sammandragning det framkallar medan det är bundet, och hur högt energibarriären förblir för att röret ska passera till ett hemifissions-tillstånd där de inre skikten har gått samman. De finner att enkel klämning sänker barriären men inte tillräckligt för att förklara effektiv fission, och att stark ytbinding faktiskt kan hindra brottet eftersom membranet först måste släppa taget om proteinet för att fullborda kollapsen.
Varför grund insättning slår enkel klämning
Den mest effektiva konstruktionen är en där proteinet delvis tränger in mellan lipidhuvudena och drar deras svansar uppåt, vilket skapar en lokal, kils-formad böj i membranet. Denna "splay" förskjuter rörens smalaste punkt något åt sidan om proteinringen snarare än direkt under den. Som en följd kan membranet genomföra den kritiska kollapsen till hemifissions-mellanläget utan att lossna från proteinet, och den totala energibarriären sjunker med mer än en storleksordning jämfört med ett naket rör. När författarna låter proteinparametrarna justera sig automatiskt för att minimera denna barriär överensstämmer den optimala lösningen nära med storleken och verkan hos dynamins PH-domän: en måttligt bred hydrofob fläck som tränger in grunt, inte en bred, överdrivet klibbig yta som skulle avlägsna lipider från lösningen.
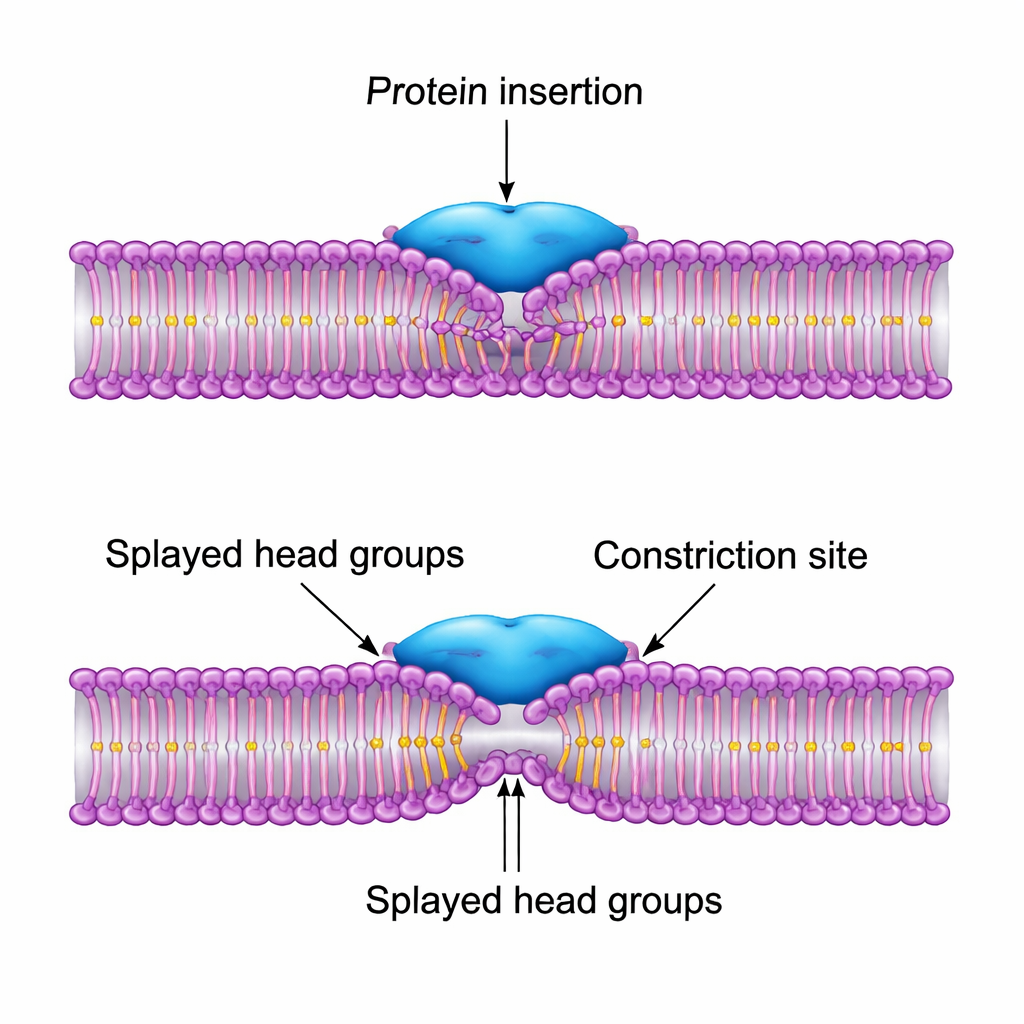
Designregler för naturen och för nanoteknik
För en icke-specialist är huvudbudskapet att dynamin inte bara fungerar genom att dra åt ett bälte runt membranet, utan genom att noggrant ställa in hur och var den griper det yttre lagret. En grund kil som splayar de yttre lipiderna och fokuserar kurvaturen precis bredvid proteinet visar sig vara mycket effektivare än rå kraftig åtstramning eller starkt fäste. Dessa resultat hjälper till att förklara varför evolutionen gynnat dynamins särskilda arkitektur och föreslår designprinciper för syntetiska proteiner eller läkemedel som behöver kunna skära eller omforma membran på ett kontrollerat sätt inom medicin och nanoteknik.
Citering: Spencer, R.K.W., Müller, M. Dynamin optimizes protein-membrane interactions for fission. npj Soft Matter 2, 6 (2026). https://doi.org/10.1038/s44431-026-00018-9
Nyckelord: membranfission, dynamin, protein–membran-interaktioner, membrankurvatur, själv-konsistent fälttheori