Clear Sky Science · sv
APP E590D-mutation ökar bildningen av Aβ- och Aη-peptider och förvärrar tauopati
Varför denna ovanliga mutation är viktig
Alzheimers sjukdom ses vanligen som en långsam ansamling av två skadliga proteiner, amyloid och tau, i hjärnan. De flesta utvecklar Alzheimer utan en enskild tydlig orsak, men några familjer bär på sällsynta genförändringar som kan rubba balansen dramatiskt. Denna artikel undersöker en sådan ovanlig förändring i genen för amyloidprekursorprotein (APP) och visar hur den kan öka produktionen av giftiga proteinfragment och förvärra den hjärntvinande process som kallas tauopati. Att förstå detta sällsynta fall ger ledtrådar som kan gälla mer allmänt för hur Alzheimer startar och sedan accelererar.
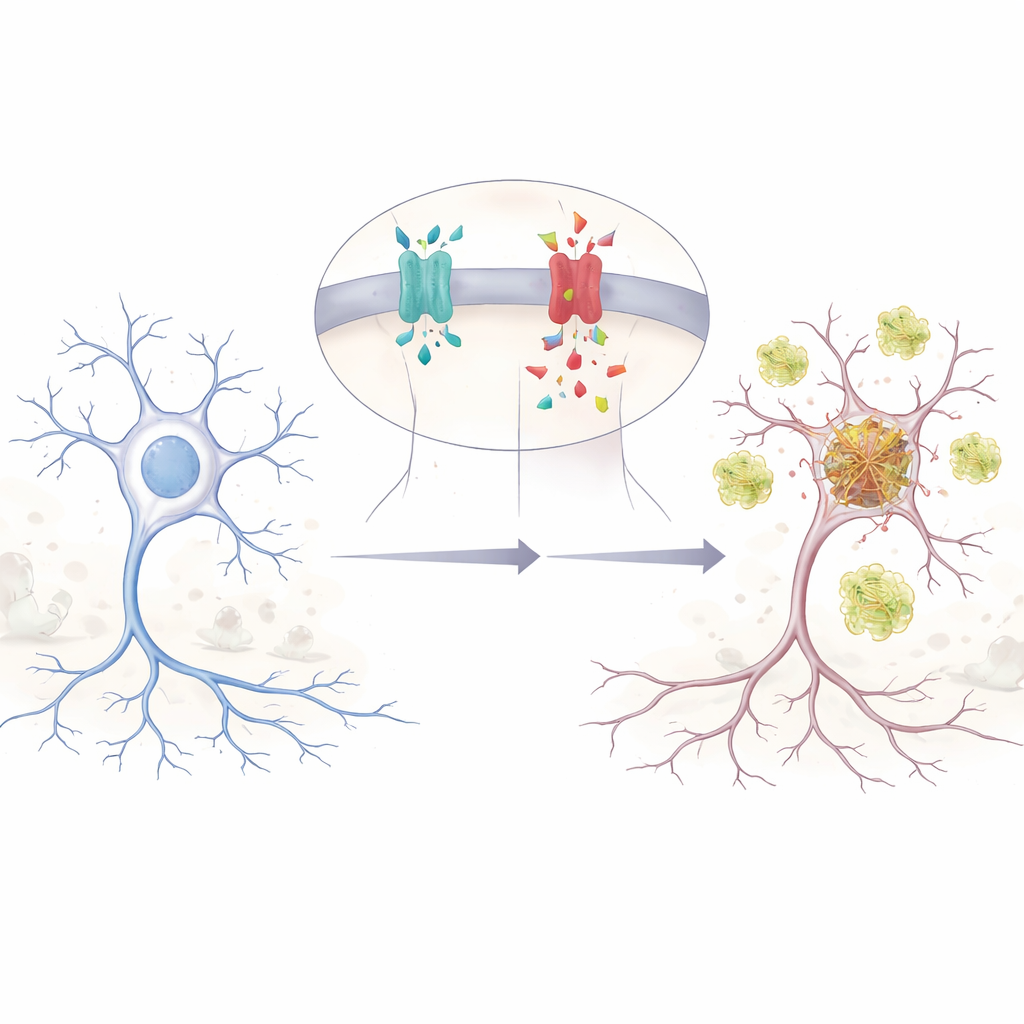
En liten genetisk förändring med stora effekter
Författarna fokuserar på en enda bokstavsändring i APP-genen, kallad E590D i hjärnans huvudform av APP. Denna mutation har rapporterats hos endast två personer, båda med bekräftad Alzheimers sjukdom i relativt ung ålder och med ovanliga, mycket tidiga minnes- och beteendeproblem. Eftersom den är så ovanlig var forskarna osäkra på om den verkligen orsakar sjukdom eller bara är en oskyldig åskådare. För att ta reda på det återskapade teamet mutationen i humana celler och i museuroner och följde sedan hur APP styckades i sina många fragment. De upptäckte att den mutanta APP producerar mycket mer amyloid beta (Aβ), den klibbiga peptid som länge förknippats med Alzheimer, än normal APP när nivåerna jämförs rättvist.
Två giftiga peptider istället för en
APP kan klippas på flera sätt, som en stock som skärs vid olika punkter. Den klassiska Alzheimersvägen genererar Aβ, men en annan klyvning ger ett mindre känt fragment kallat Aη. Tidigare arbete visade att Aη kan skada kopplingarna mellan nervceller och försvaga hjärnans förmåga att stärka minnen. I sina experiment fann forskarna att E590D-mutation inte bara ökar Aβ; den ökar också starkt Aη och ett upstream-fragment som matar in i båda vägarna. Det innebär att mutationen skjuter APP-processningen mot en dubbel träff av skadliga peptider, vilket potentiellt stör hjärnkretsar redan innan de klassiska amyloida placken förväntas dyka upp.
Hur mutationen snabbar upp cellulär trafik
För att förstå varför fler giftiga fragment bildas studerade teamet var APP sitter och rör sig på cellens yta. Många av de klyvningar som skapar Aβ sker först efter att APP tagits in i cellen genom en process som kallas endocytos. Med bildteknik och biokemiska knep som märker proteiner vid ytan och sedan följer deras internalisering, visade forskarna att mutant APP är mindre förekommande på cellernas utsida och tas upp snabbare in i interna kompartment än normal APP. När den väl är inne i dessa tidiga endosomer möter APP enzymerna som genererar Aβ, och den förändrade trafiken verkar ge dessa enzymer större möjlighet att verka. Samtidigt ökar även klyvning vid η-stället på ytan, vilket förklarar ökningen av Aη.
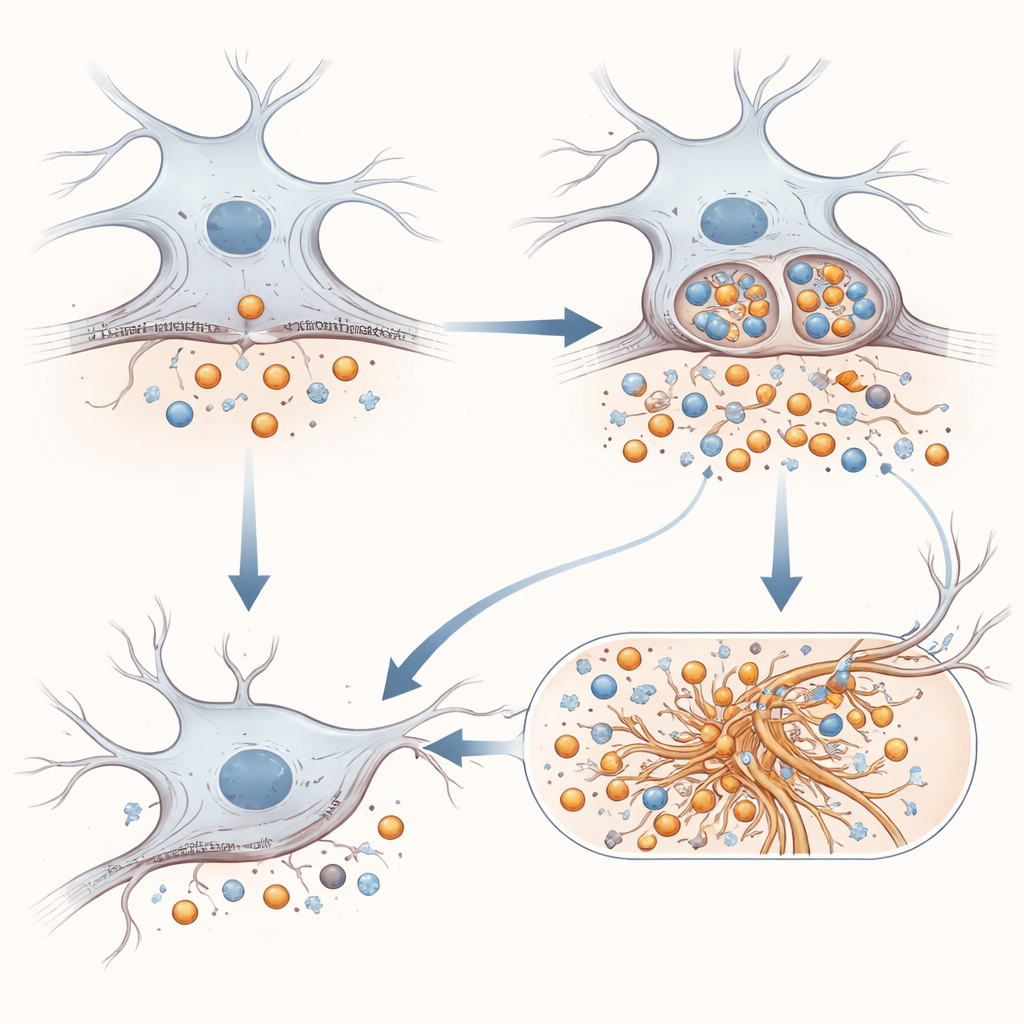
Från proteinfragment till trassligt tau och hjärnans inflammation
Berättelsen slutar inte med amyloidrelaterade fragment. Forskarna testade om mutant APP skulle påverka tau, det strukturella proteinet som bildar vridna fibrer i många demenser. I cellmodeller som lyser upp när tau-frön får nya tau-klumpar att bildas ledde närvaron av E590D-APP till starkare aggregat än antingen normal APP eller ingen APP. I en musemodell redan benägen för tau-problem förvärrade injektion av ett virus som producerar den mutanta APP i hippocampus tau-nystan och utlöstes starkare aktivering av astrocyter och mikroglia, hjärnans stöd- och immunceller. Intressant nog var standardlösliga amyloidbitar svåra att upptäcka i dessa mushjärnor, men ett distinkt APP-deriverat fragment dök bara upp när mutationen var närvarande, vilket tyder på förändrad processning i levande vävnad.
Vad detta betyder för förståelsen av Alzheimer
Tillsammans visar fynden att denna sällsynta APP-mutation inte är godartad. Den driver APP mot att generera mer än en giftig peptid, snabbar upp internaliseringsstegen som gynnar skadliga klyvningar och förstärker tau-trassel och inflammation i hjärnan. För icke-specialister är huvudbudskapet att Alzheimersbiologin inte drivs av en enda bov utan av ett nätverk av interagerande proteinfragment och cellresponser. Att studera sådana kraftfulla men ovanliga genetiska varianter ger en förstärkt vy av det nätverket. I detta fall tyder det på att behandlingar kanske behöver ta hänsyn till både amyloid och alternativa APP-deriverade peptider som Aη, samt deras samlade påverkan på tau, snarare än att rikta in sig på en väg isolerat.
Citering: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
Nyckelord: Alzheimers sjukdom, amyloidprekursorprotein, tau-nystan, neuroinflammation, genetisk mutation