Clear Sky Science · sv
15 år av longitudinella genetiska, kliniska, kognitiva, bild- och biokemiska mått i DIAN
Varför detta betyder något för familjer och Alzheimerbehandlingens framtid
De flesta tänker på Alzheimers sjukdom som något som dyker upp sent i livet, ofta utan varning. Men i ett litet antal familjer innebär specifika ärftliga genförändringar nästan garantier för att en person kommer att utveckla Alzheimers i relativt ung ålder. Dominantly Inherited Alzheimer Network (DIAN) Observational Study har under 15 år noggrant följt dessa familjer över hela världen. Genom att iaktta hur sjukdomen utvecklas långt innan minnesproblemen uppstår, avslöjar DIAN en detaljerad tidslinje av hjärnförändringar som kan hjälpa läkare att upptäcka, förebygga eller fördröja Alzheimers hos många fler människor.
En global insats som följer hög-riskfamiljer
DIAN följer vuxna från familjer som bär på sällsynta mutationer i tre gener kopplade till en ärftlig form av Alzheimers sjukdom. Vissa deltagare har mutationen och andra inte, men ingen får sin status upplyst av studien om de inte väljer separat klinisk testning. Projektet startade 2008 med 10 centra i tre länder och har vuxit till 23 centra i 11 länder, med arbete på sju språk. Över 660 personer har rekryterats, varav mer än 300 fortfarande aktivt deltar. Vid regelbundna besök genomgår volontärer medicinska och minnestester, hjärnavbildning, ryggvätske- och blodprov samt, för dem som samtycker, hjärnobefordran efter döden. Icke-bärande släktingar fungerar som en ovanligt välmatchad referensgrupp, vilket hjälper forskare att skilja normala åldersförändringar från sjukdomsrelaterade förändringar.
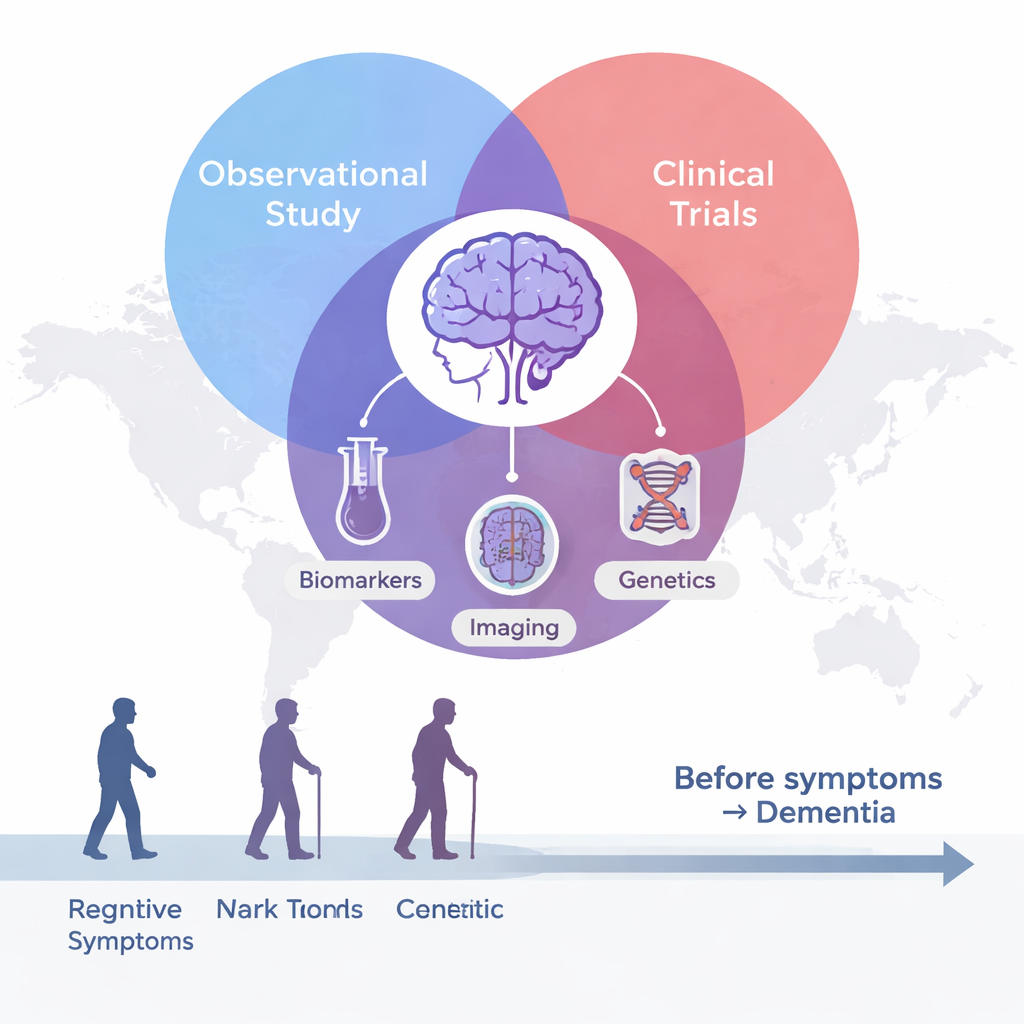
Att se sjukdomen decennier före symtom
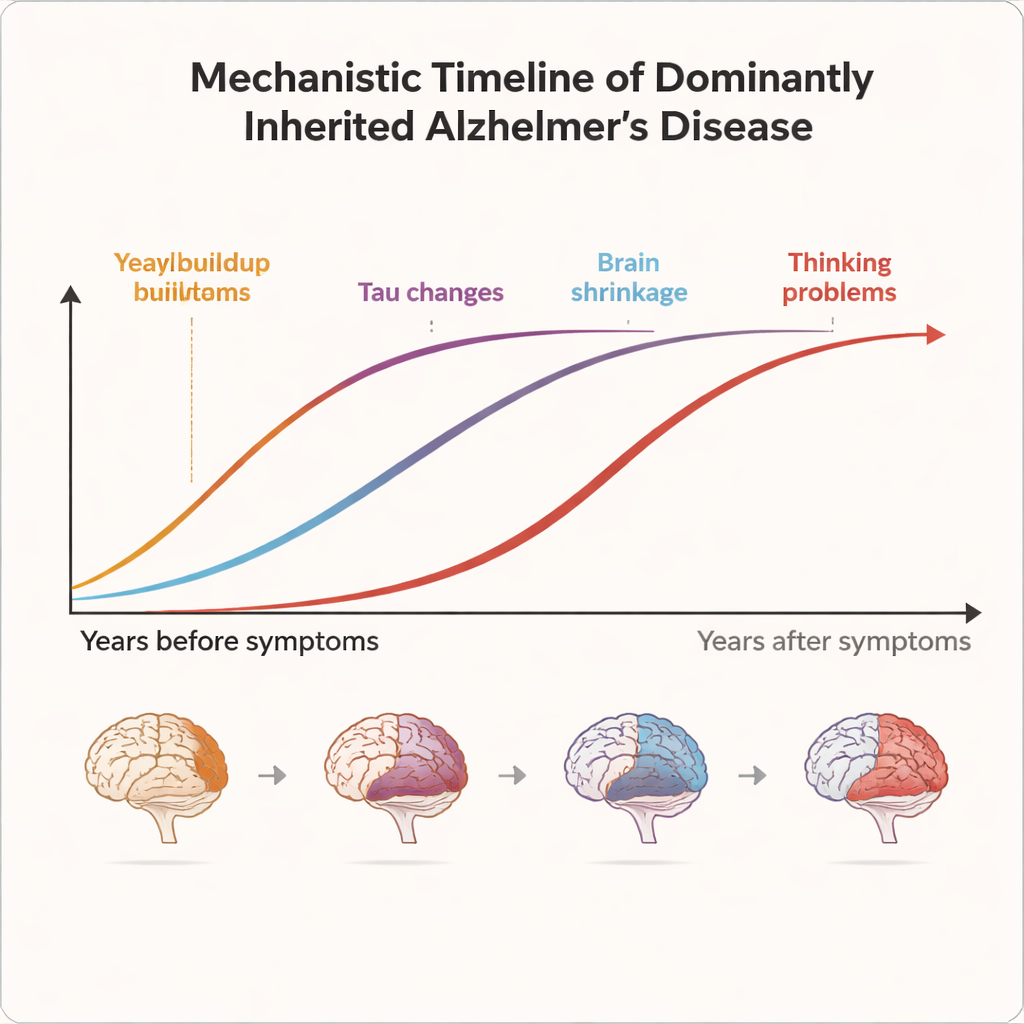
Eftersom åldern när symtom vanligtvis börjar är relativt förutsägbar inom varje familj, kan forskare uppskatta hur många år varje bärare ligger från sannolik debut. Det gör att de kan ordna personer längs en ”sjukdomsklocka”, från mer än 20 år före problemens början till många år därefter. DIAN:s resultat visar att Alzheimers inte är en plötslig händelse utan en lång process. Klibbiga proteinansamlingar kallade amyloida plack börjar bygga upp i hjärnan 15–20 år före symtom, synliga på specialiserade PET-skanningar och återspeglade av sjunkande nivåer av en form av amyloid i ryggvätskan. Cirka 10–15 år före förväntad debut framträder andra varningstecken: onormala tau-proteiner stiger i ryggvätskan, hjärnans ämnesomsättning saktar ner och subtilt tunt cortex syns på MR-bilder. Först flera år senare blir förändringar i tänkande och daglig funktion mätbara i detaljerade kognitiva tester.
Ett levande bibliotek av mätningar och prov
För att omvandla dessa observationer till allmängiltig vetenskap har DIAN byggt upp en av världens rikaste samlingar av data och vävnader relaterade till Alzheimers. Åtta specialiserade enheter hanterar klinisk information, kognitiva tester, hjärnavbildning, vätskebiomarkörer, genetik, hjärnpatologi, statistik och övergripande administration. Blod- och ryggvätskeprover bearbetas i ett centralt biobank, där avancerade verktyg mäter dussintals proteiner kopplade till amyloid, tau, inflammation och nervcellsskada. Genetiska och ”multi-omiska” analyser undersöker DNA, RNA, proteiner, fetter och andra molekyler i blod, hjärnvävnad och cellmodeller härledda från deltagare. Ett växande neuropatologiskt program undersöker noggrant donerade hjärnor för att bekräfta diagnoser och stadiera sjukdomen. All denna information rengörs, kvalitetskontrolleras och fryses ner i årsvisa dataset som externa forskare kan begära under strikta integritetsskydd.
Drivkraft för prövningar och nästa generations verktyg
DIAN är inte bara en studie av vad som händer naturligt; det är också ryggraden i ett kompletterande kliniskt prövningsprogram som testar läkemedel avsedda att bromsa eller förebygga ärftlig Alzheimers. Eftersom observations- och behandlingsstudier använder harmoniserade procedurer kan deras resultat kombineras och jämföras. Den detaljerade DIAN-tidslinjen för hjärnförändringar har redan bidragit till att forma internationella kriterier för att definiera Alzheimers biologiskt, baserat på amyloid, tau och neurodegenerationsmarkörer snarare än enbart symtom. Framöver expanderar nätverket till fjärrbedömningar via smartphoneappar, hembesök av vårdpersonal och bärbara enheter för att upptäcka mycket tidiga kognitiva förändringar och följa daglig funktion. Det satsas också kraftigt på blodbaserade tester och djupare molekylär profilering för att hitta nya behandlingsmål och förstå varför sjukdomsförloppet skiljer sig mellan individer och populationer.
Vad detta betyder för personer som oroar sig för Alzheimers
DIAN-studien visar att i ärftlig Alzheimers börjar hjärnan förändras många år innan minnet sviktar — och att dessa dolda skift kan mätas i blod, ryggvätska och avbildningar. Även om de studerade mutationerna är sällsynta, tycks den underliggande sjukdomsprocessen likna den hos den mycket vanligare sena debutformen av Alzheimers. Detta gör DIAN till en stark modell för hela fältet. Genom att kartlägga steg-för-steg-resan från frisk hjärna till demens, och genom att globalt dela sina noggrant insamlade resurser, hjälper DIAN forskare att utforma tidigare och mer precisa insatser. För familjer som står inför ärftlig risk, och för de miljoner som påverkas av Alzheimers mer generellt, erbjuder dessa insikter en tydligare väg mot tidigare upptäckt, bättre övervakning och i förlängningen mer effektiva förebyggande åtgärder och behandlingar.
Citering: Daniels, A.J., McDade, E., Llibre-Guerra, J.J. et al. 15 years of longitudinal genetic, clinical, cognitive, imaging, and biochemical measures in DIAN. npj Dement. 2, 13 (2026). https://doi.org/10.1038/s44400-025-00047-7
Nyckelord: Alzheimers sjukdom, genetisk demens, hjärnbiomarkörer, longitudinell studie, tidig upptäckt