Clear Sky Science · sv
Kodning av funktionella kanter i grafer för att modellera rumsligt varierande relationer i tumörmikromiljön
Varför det spelar roll att kartlägga cancers grannskap
Cancer växer inte i isolering. Tumörceller lever i ett livligt grannskap av immunceller, stödjeceller, blodkärl och kemiska signaler — alla trängda tillsammans i rummet. Hur dessa grannar är ordnade och hur starkt de påverkar varandra kan avgöra om en cancer sprider sig, svarar på behandling eller hålls i schack. Denna artikel introducerar SPIFEE, ett nytt artificiellt intelligensramverk som förvandlar mikroskopbilder och molekylära kartor av tumörer till nätverk, vilket hjälper forskare att peka ut vilka cell- och väginteraktioner som är mest kopplade till sjukdomstyp och patientutfall.
Att förvandla vävnad till en nätverkskarta
Moderna cancerstudier kan mäta mycket mer än hur en tumör ser ut i mikroskopet. Vissa metoder markerar dussintals proteiner på enskilda celler, andra ger detaljerade färgade snitt av vävnadsstruktur, och nyare verktyg registrerar vilka gener som är aktiva på tusentals punkter över ett tumörsnitt. SPIFEE behandlar allt detta som olika vyer av samma grannskap. Det representerar varje prov som en graf: noder står för nyckelentiteter i tumörmikromiljön — såsom celltyper, visuella vävnadsmönster eller molekylära signalvägar — medan kanter fångar hur dessa entiteter interagerar i rummet. Avgörande är att SPIFEE inte reducerar en interaktion till ett enda tal som “avstånd”. Istället lagrar varje kant en liten kurva som beskriver hur starkt två entiteter blandar sig eller stöter bort varandra över ett avståndsspann, och bevarar därigenom mycket rikare rumslig detalj.
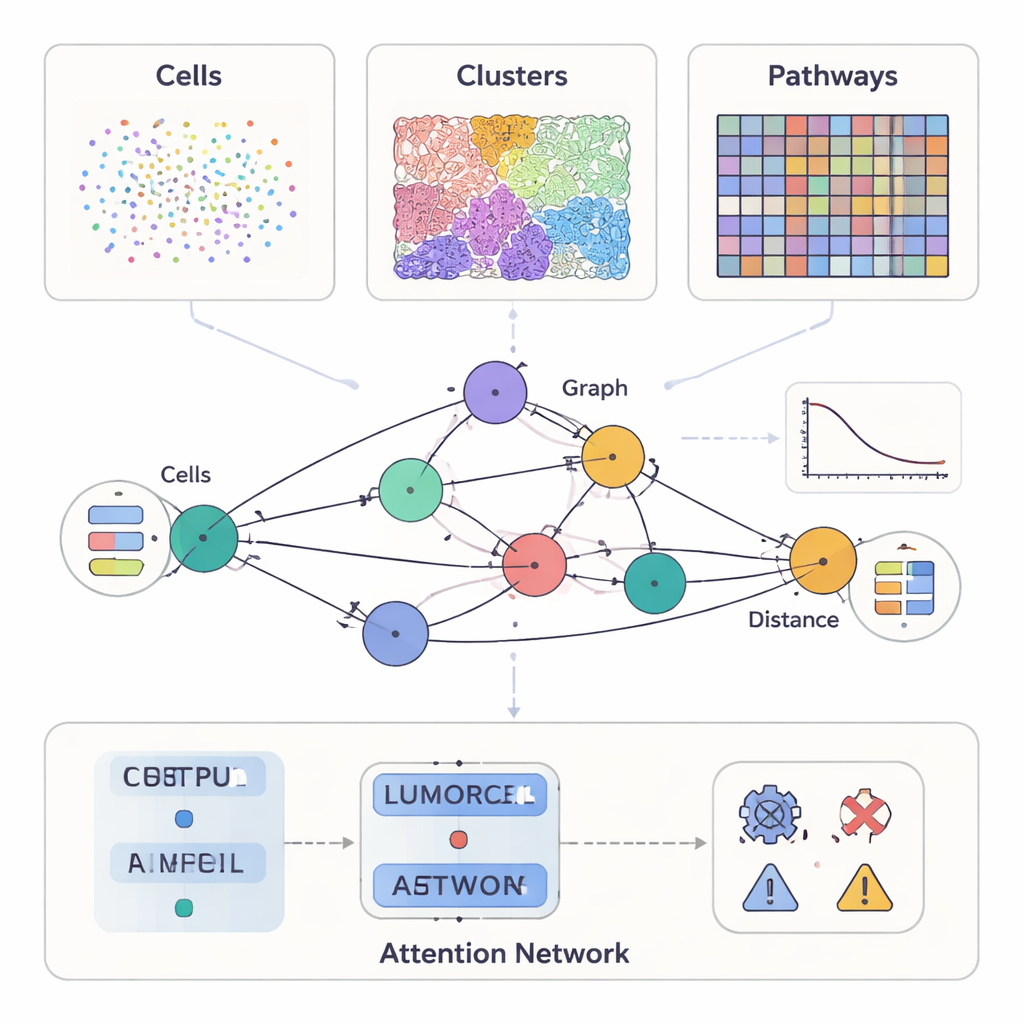
En flexibel lins för många typer av cancerdata
Författarna testade SPIFEE på flera stora, oberoende canceruppsättningar som täcker olika teknologier och skalor. I pankreassjukdomsprov märkta med multiplex immunofluorescens representerade varje nod en celltyp, och nodernas egenskaper kom från single-cell RNA-sekvensering som sammanfattade hur dessa celler tenderar att kommunicera. I lungcancerpreparat färgade med den rutinmässiga hematoxylin–eosin-metoden representerade noder återkommande visuella vävnadsmönster, upptäckta automatiskt av ett självövervakat inlärningssystem. I en tredje kontext konverterades standardlungpreparat av ett djupinlärningsverktyg till virtuella rumsliga transkriptomikdata, och SPIFEE-noder representerade molekylära signalvägar såsom hypoxi, östrogen eller JAK–STAT-signalering, med egenskaper härledda från genaktivitet. I samtliga dessa inställningar kunde samma ramverk ta in olika nodtyper och ändå bygga jämförbara rumsliga grafer.
Att hitta interaktionerna som skiljer hälsoutfall åt
När SPIFEE har byggt en graf skickas den genom ett grafattentionnätverk, en typ av neuralt nätverk som lär sig inte bara att förutsäga ett utfall — såsom cancergenotyp, överlevnadsrisk eller sjukdom kontra icke-cancerös inflammation — utan också att belysa vilka kanter som var viktigast för den förutsägelsen. I pankreasvävnad skilde SPIFEE kronisk pankreatit från pankreascancer (pancreatic ductal adenocarcinoma) med högre noggrannhet än tidigare grafbaserade metoder. Modellen fokuserade konsekvent på interaktioner som involverade epiteliala (tumörlika) celler och regulatoriska T‑celler, antigenpresenterande celler och hjälpar‑T‑celler, vilket pekar mot ett immunosuppressivt grannskap som är mer framträdande i cancer än vid inflammation. I lungadenocarcinompreparat identifierade SPIFEE särskilda stromal–tumörmönster vars interaktioner korrelerade med bättre eller sämre överlevnad, vilket antyder att ”gränszonerna” mellan tumör och stödjevävnad bär viktiga prognostiska ledtrådar som standardanalyser kan missa.
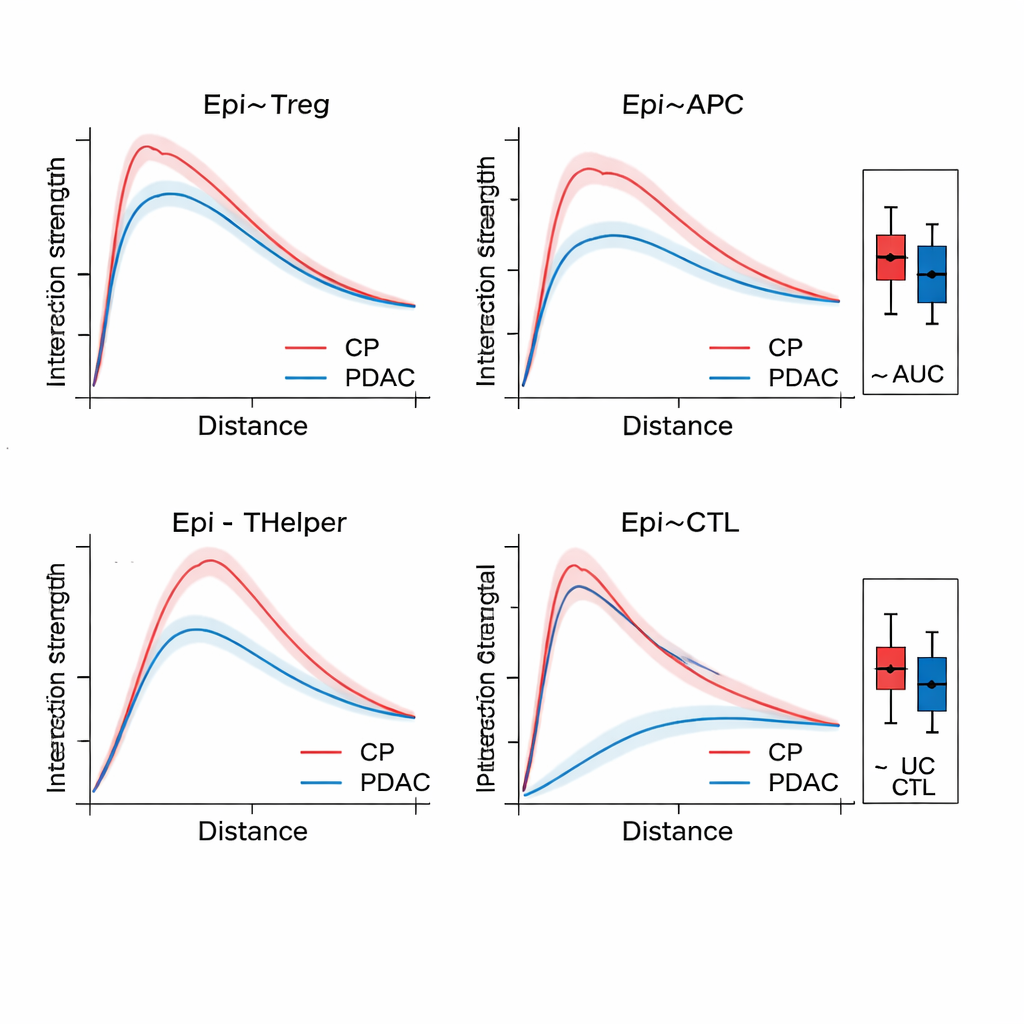
Att läsa molekylär korsprat från rutinpreparat
Kanske mest slående var att SPIFEE kunde härleda meningsfulla väginteraktioner från vanliga patologibilder när dessa översattes till predikterade genaktivitetskartor. Genom att behandla signalvägar som noder och deras rumsliga samsynkronisering som funktionella kanter framhävde metoden par såsom hypoxi med EGFR eller JAK–STAT med PI3K — kombinationer som redan är kända för att driva immunundvikande och läkemedelsresistens i lungcancer. Den lyfte också fram östrogenrelaterade vägar i lungadenocarcinom och vissa immuna och stressrelaterade vägar i skivepitelstumörer, fynd som stämde överens med mönster observerade i bulk-RNA‑sekvensering och i en oberoende, verklig rumslig transkriptomikdataset. Detta tyder på att även när molekylära mätningar är approximativa, bär rumsliga mönster i rutinpreparat fortfarande återvinningsbara signaler om hur nyckelvägar interagerar i levande tumörer.
Vad detta betyder för framtida cancerbehandling
För en icke-specialist är huvudbudskapet att SPIFEE erbjuder ett nytt sätt att läsa cancercellers ”sociala liv” direkt från bilder och molekylära kartor. Genom att koda hur relationer förändras med avstånd istället för att platta till dem till ensiffriga poäng, och genom att använda attention‑baserade neurala nätverk för att rangordna vilka interaktioner som är viktigast, kan ramverket avslöja kombinationer av celler, vävnadsmönster och signalvägar som särskiljer cancertyper och förutsäger överlevnad. Även om dessa fynd fortfarande behöver biologisk och klinisk validering, pekar tillvägagångssätt som SPIFEE mot en framtid där rutinprov från tumörer kan ge inte bara statiska bilder, utan dynamiska kartor över interaktionshotspots som hjälper till vid diagnostik, riskklassificering och så småningom val av individualiserad behandling.
Citering: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
Nyckelord: tumörmikromiljö, rumslig transkriptomik, grafneurala nätverk, cancerpatologi, cell–cell-interaktioner