Clear Sky Science · sv
AI-drivet 3D-subcellulärt RPE-karta upptäcker celltillståndsövergångar vid etablering av apikalt-basal polaritet
Varför ögats stödjeceller är viktiga
Den skarpa syn vi uppskattar varje dag bygger på ett tunt lager stödjeceller längst bak i ögat, kallat retinalt pigmentepitel (RPE). När dessa celler förlorar sin ordnade interna struktur kan synstörande sjukdomar, såsom åldersrelaterad makuladegeneration, följa efter. Denna studie kombinerar stamcellsbiologi, avancerad mikroskopi, artificiell intelligens och matematisk modellering för att bygga en detaljerad tredimensionell ”digital tvilling” av en RPE-cell, och visar hur dess inre delar omarrangeras när den mognar och vad som går fel när den processen störs.
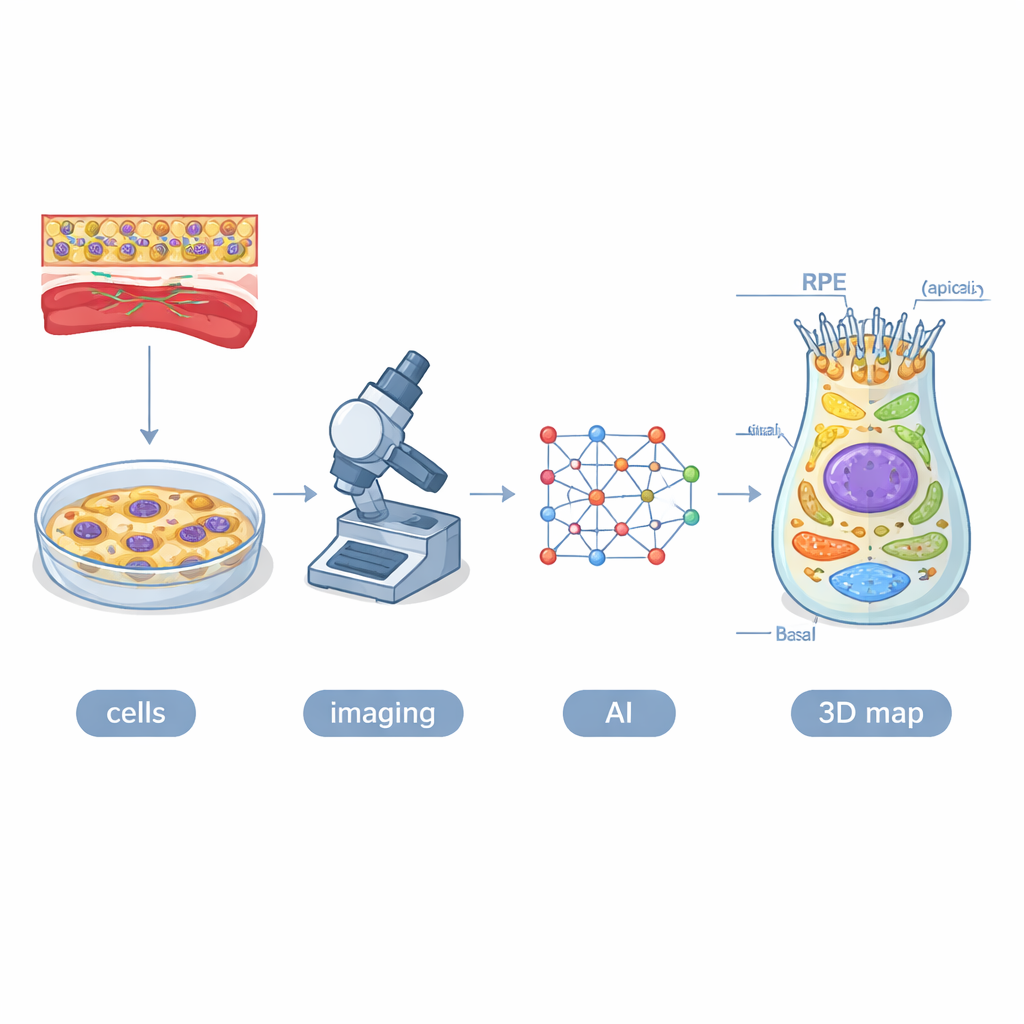
Att bygga en digital tvilling av ögonceller
Forskarna började med humana inducerade pluripotenta stamceller — celler omprogrammerade att bete sig som embryonala celler — och styrde dem att bli RPE. De använde 16 konstruerade cellinjer där olika cellulära strukturer, såsom mitokondrier, lysosomer och cellens yttre skelett, lyste grönt i mikroskopet. Under fyra veckor avbildade de ungefär 1,3 miljoner celler i 3D med höginnehålls konfokalmikroskopi. För att förstå denna enorma datamängd skapade de ett AI-system kallat POLARIS, baserat på en typ av neuralt nätverk som automatiskt kan rita upp varje cell, dess kärna och de märkta organellerna i varje bildskiva. Människliga experter kontrollerade och förfinade maskinens arbete, varefter teamet kombinerade resultaten till en genomsnittlig tredimensionell modell — en digital tvilling — av en typisk RPE-cell i varje stadium.
Två vägar: frisk mognad vs. blockerad polaritet
RPE-celler måste bli ”polariserade”, med distinkta topp- (apikala) och botten- (basala) sidor, för att transportera näringsämnen, rensa avfall och kommunicera både med näthinnan och blodtillförseln. För att främja detta behandlade teamet vissa kulturer med en molekyl som kallas PGE2, som främjar bildningen av en liten sensorisk struktur kallad primär cilie och förbättrar polaritet. Andra kulturer fick HPI4, vilket stör cilier och förhindrar korrekt polarisation. Med hjälp av POLARIS-baserade mätningar visade forskarna att i den friska vägen växte cellerna högre och smalare och deras kärnor blev mer kompakta och rundade. Under HPI4 förblev cellerna plattare och bredare med mer oregelbundna former. Statistiska modeller visade att i framgångsrikt polariserande celler följde dessa formförändringar en förutsägbar, icke-slumpmässig sekvens, medan blockerade celler drev in i mer varierade, oordnade tillstånd.
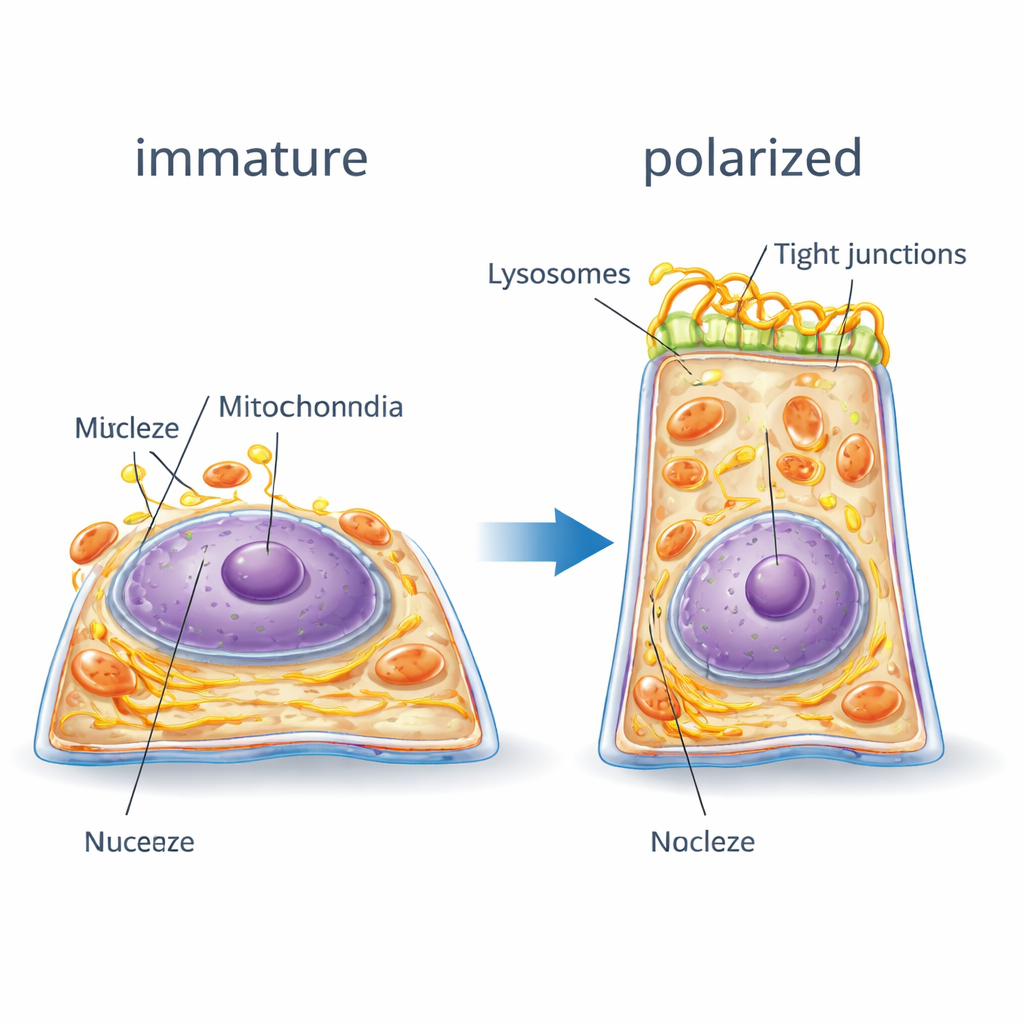
Hur cellens inre omorganiseras
Den digitala tvillingen gjorde det möjligt att följa hur cellens interna arkitektur omorganiseras. När RPE-celler polariserades skiftade deras interna stödjande nätverk av aktin- och myosinfiber från många små fragment till färre, tjockare band som ringade cellkanterna — som att dra åt ett bälte — för att stödja den nya höga formen. Kärnmembranet utvecklade djupa veck, och cellerna tenderade att sluta med färre nukleoler, tecken på ett mer moget och stabilt genuttrycksprogram. Junction-proteiner som binder samman närliggande celler flyttade från utspridda platser inne i cellen till väl definierade band längs sidoväggarna, vilket stärkte barriären. Samtidigt förstornades och migrerade mitokondrier och endoplasmatiskt retikulum, som hjälper till att bearbeta proteiner och lipider, mot kärnan och bildade mer sammanhängande nätverk. Lysosomer, cellens återvinningscentraler, försköts mot den centrala, övre regionen av cellen. När polariteten blockerades var många av dessa omplaceringar ofullständiga eller helt frånvarande, och organellerna förblev mer slumpmässigt spridda.
Samtal mellan organeller
Teamet undersökte också vilka organeller som tenderar att befinna sig i samma områden inne i cellen, ett tecken på att de kan interagera funktionellt. Genom att överlagra organellkartor på genomsnittscellen och beräkna hur starkt deras positioner korrelerade fann de att i välpolariserade celler grupperade strukturerna sig i koordinerade kluster. Till exempel bildade peroxisomer, mitokondrier, endoplasmatiskt retikulum, vissa junctions och delar av cytoskelettet ett tätt sammankopplat nätverk kopplat till energianvändning och membranombyggnad. Lysosomer placerade sig nära cellens centrala organiseringsnav, centriolen, vilket tyder på en roll i kontroll av cilier och ytförnyelse. I kontrast försvagades dessa rumsliga relationer när polarisationen blockerades, och det övergripande ”samtalet” mellan organeller verkade fragmenterat. Maskininlärningsklassificerare tränade på dessa egenskaper visade att den laterala fördelningen av mitokondrier och den vertikala placeringen av täta junctions var särskilt starka markörer för om en cell var korrekt polariserad.
Varför detta är viktigt för syn och sjukdom
Genom att förena AI, storskalig avbildning och matematisk analys levererar detta arbete en rikt detaljerad 3D-referens för hur friska humana RPE-celler organiserar sig i rum och tid, och hur den organisationen bryts ned när polarisationen misslyckas. För icke-specialister är slutsatsen att näthinnans hälsa inte bara beror på vilka molekyler som finns, utan på var och när cellulära komponenter är ordnade inne i varje stödjecell. Den digitala tvillingen som tagits fram här erbjuder ett kvantitativt mått för att upptäcka subtila defekter i patienthärledda RPE-celler och öppnar nya möjligheter för att diagnostisera tidiga cellulära problem i näthinnesjukdomar samt för att testa behandlingar som syftar till att återställa korrekt cellstruktur innan synen oåterkalleligt går förlorad.
Citering: Ortolan, D., Sathe, P., Volkov, A. et al. AI driven 3D subcellular RPE map discovers cell state transitions in establishment of apical-basal polarity. npj Artif. Intell. 2, 20 (2026). https://doi.org/10.1038/s44387-026-00074-6
Nyckelord: retinal pigmentepitel, cellpolaritet, artificiell intelligens, 3D cellkartering, åldersrelaterad makuladegeneration