Clear Sky Science · sv
En ämnesomsättningsinformerad neuronnätmodell identifierar vägar som påverkar effektivitet och toxicitet hos antimikrobiella kombinationer
Varför detta är viktigt för vardagshälsan
När fler infektioner slutar svara på våra standardantibiotika vänder sig läkare allt oftare till kombinationer av läkemedel. Men att blanda mediciner kan vara ett tveeggat svärd: rätt par kan utrota envisa bakterier, medan fel mix kan skada organ som njurar och lever. Denna studie presenterar en ny datorbaserad metod, kallad CALMA, utformad för att hjälpa forskare och kliniker att hitta läkemedelskombinationer som både är effektiva mot mikrober och skonsamma för patienter.
Bekämpa bakterier utan ren prov-och-fel
Traditionellt har upptäckten av bra antibiotikakombinationer inneburit att testa enorma antal läkemedelspaar eller trioer i labb och hos patienter. Antalet möjliga blandningar växer explosionsartat med varje tillsatt läkemedel, vilket gör fullständig experimentell testning orealistisk. Dessutom fokuserar de flesta befintliga verktyg endast på hur starkt kombinationerna dödar bakterier och bortser från hur de kan skada mänsklig vävnad. Författarna menar att för att utforma bättre behandlingar måste vi beakta båda sidorna av ekvationen: effektivitet mot patogener och säkerhet för människor.
En smart modell som förstår cellens kemi
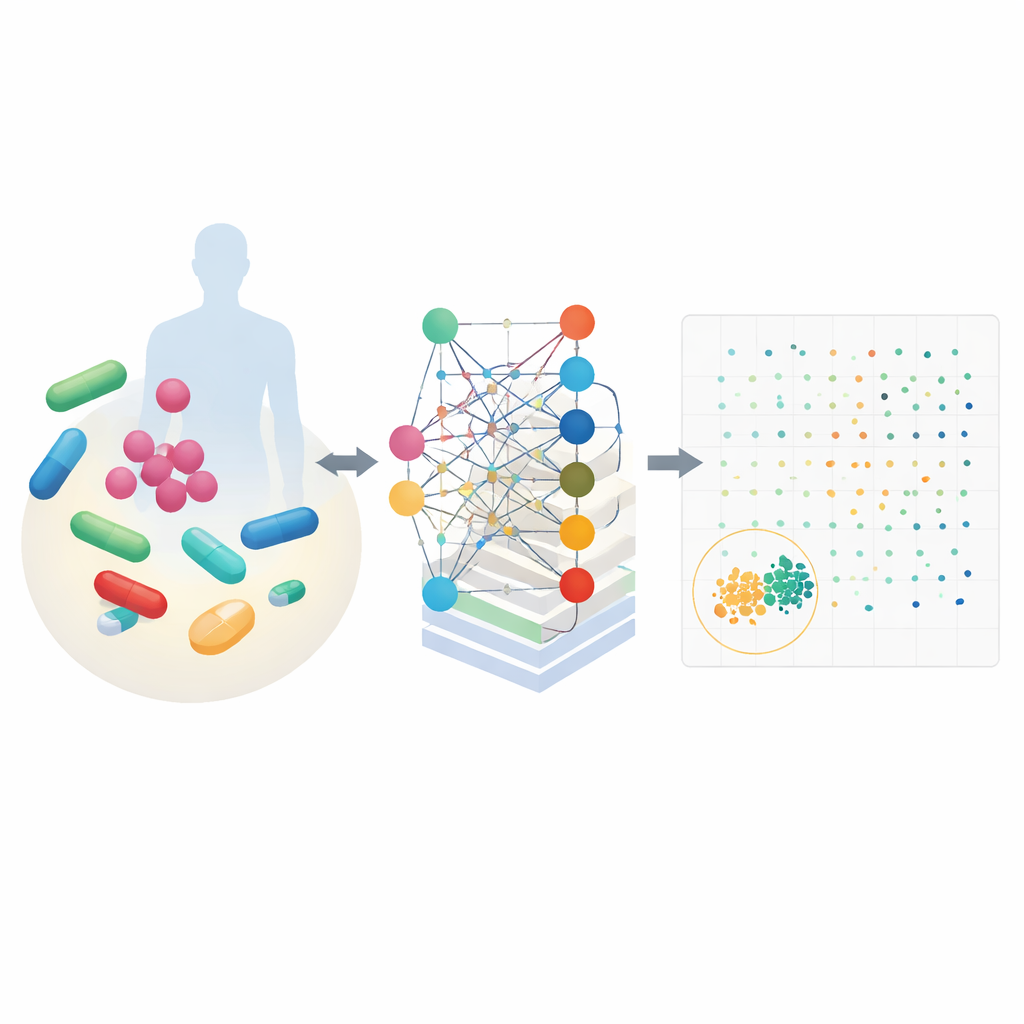
CALMA kombinerar två kraftfulla idéer. För det första använder den detaljerade kartor över cellulär metabolism som beskriver hur organismer omvandlar näring till energi och byggstenar. Dessa kartor, framtagna för bakterier som Escherichia coli och tuberkulosbakterien, simulerar hur tusentals kemiska reaktioner förändras när ett läkemedel är närvarande. För det andra matar CALMA dessa simuleringar till ett artificiellt neuralt nätverk vars struktur speglar metaboliska vägar. Genom att gruppera information enligt kända biologiska rutter—såsom energiproduktion eller återvinning av nukleotider—lär sig modellen samband som kopplar specifika vägar till antingen effektiv bakteriedödning eller skadliga biverkningar i mänskliga celler.
Skanna landskapet av läkemedelsblandningar
Med hjälp av data från tidigare experiment och stora säkerhetsdatabaser tränade forskarna CALMA att tilldela varje läkemedelskombination två poäng: en för hur starkt den angriper bakterier och en annan för hur sannolikt det är att den är toxisk för människor. Genom att plotta dessa poäng skapas ett landskap där de bästa kandidaterna hamnar i det nedre vänstra hörnet—starka mot mikrober och milda mot mänskliga celler. När de tillämpade CALMA på 35 kliniskt relevanta läkemedel förminskade verktyget nästan 600 möjliga par till en liten uppsättning lovande alternativ, vilket krympte det experimentella sökutrymmet med cirka 97 procent. Bland de främsta förslagen fanns kombinationer som involverade vanliga antibiotika som azithromycin, vancomycin, isoniazid och trimetoprim.
Från datorprediktioner till labbtester och verkliga patienter
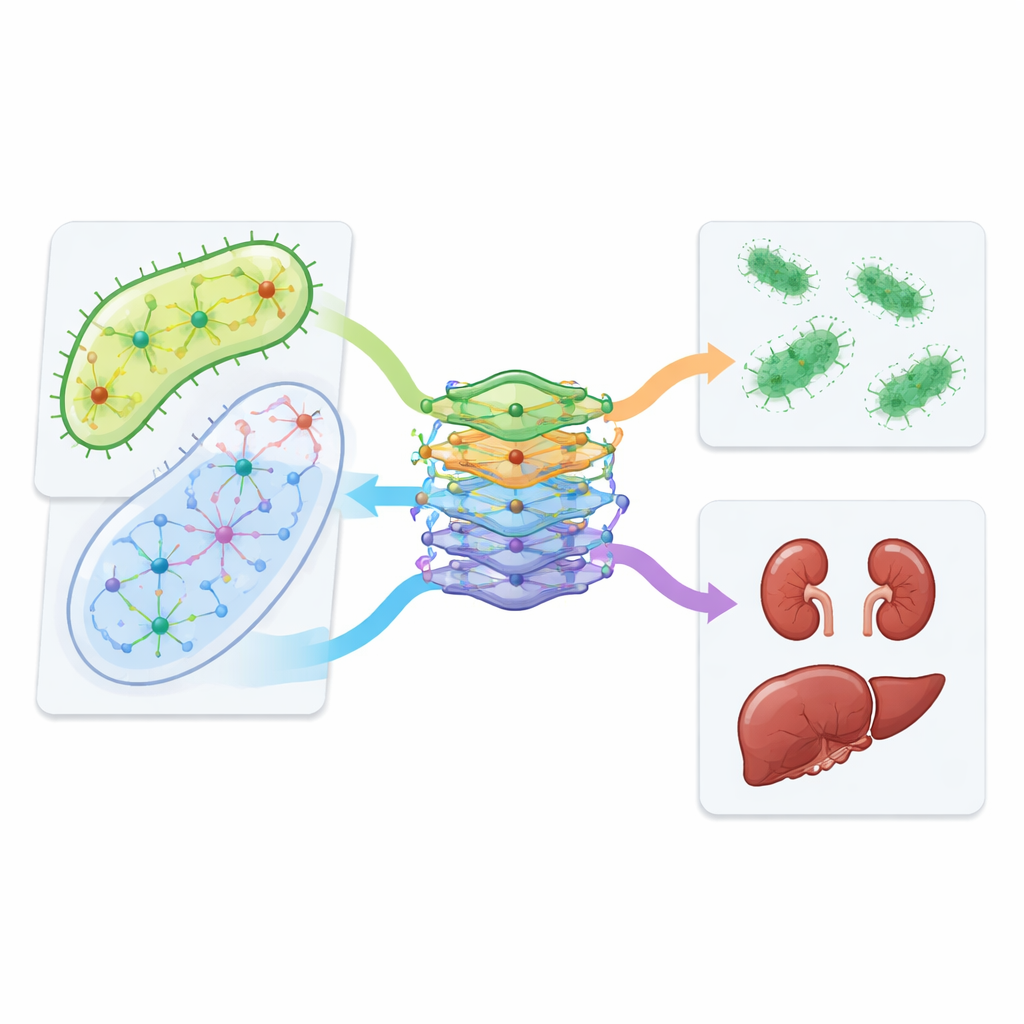
Teamet gick vidare från simuleringar för att testa flera förutsagda kombinationer i njur- och levercellinjer. De fann att vissa par, inklusive azithromycin med vancomycin och isoniazid med trimetoprim, var mindre toxiska för mänskliga celler än de enskilda läkemedlen, samtidigt som de behöll aktivitet mot E. coli. CALMAs design gjorde det också möjligt för forskarna att undersöka vilka metaboliska vägar som driver toxicitet. En väg som återvinner DNA-byggstenar, känd som nukleotidåtervinning (nucleotide salvage), framträdde som en nyckelfaktor: att justera den i cellexperiment förändrade hur skadliga vissa kombinationer var. Slutligen granskade författarna journaldata från hundratusentals patienter och observerade att personer som fick azithromycin tillsammans med vancomycin hade färre dokumenterade njurproblem än liknande patienter som endast behandlades med vancomycin, vilket ekar fynden från labbet.
Vad detta betyder för framtida behandlingar
För en icke-specialist kan CALMA betraktas som ett intelligent filter som förstår tillräckligt med biologi för att föreslå vilka läkemedelsblandningar som är värda att testa först. Istället för att blint blanda antibiotika och hoppas på det bästa kan forskare fokusera på kombinationer som modellerna förutspår kommer att träffa bakteriers svaga punkter samtidigt som sårbara mänskliga vägar skonas. Även om metoden är beroende av tillgängliga data och inte är perfekt erbjuder den en mer rationell väg för att utforma kombinationsterapier. Med tiden skulle verktyg som CALMA kunna hjälpa läkare att behandla resistenta infektioner mer säkert, minska prov-och-fel i läkemedelsutveckling och till och med anpassas till andra sjukdomar där kombinationsbehandlingar och biverkningar är stora utmaningar.
Citering: Arora, H.S., Lev, K., Robida, A. et al. A Metabolism-Informed Neural Network Identifies Pathways Influencing the Potency and Toxicity of Antimicrobial Combinations. npj Drug Discov. 3, 11 (2026). https://doi.org/10.1038/s44386-026-00042-9
Nyckelord: antibiotikakombinationer, Läkemedelstoxicitet, artificiella neurala nätverk, metabolism, antimikrobiell resistens