Clear Sky Science · sv
Sluta sig om avvikelser i signalvägar från histopatologiska bilder via logikbegränsad gen-väg heterogen kunskapsgraf
Att se dolda cellulära signaler i cancerpreparat
När läkare undersöker cancer i mikroskop ser de främst former och färger, inte de komplexa molekylära samtal som pågår inne i cellerna. Dessa osynliga signal"samtal" mellan gener och vägar bestämmer ofta hur en tumör växer och hur den kan reagera på behandling. Denna studie presenterar ett nytt artificiellt intelligenssystem som läser rutinmässiga patologibilder och härleder vilka cellulära kommunikationsvägar, eller signalvägar, som fungerar fel—vilket erbjuder ett sätt att skymta molekylärt beteende utan extra laboratorietester.
Från ledtrådar om enskilda gener till den större bilden
Traditionella angreppssätt försöker förutsäga status för enskilda gener från vävnadsbilder: är en viss gen muterad eller inte? Det är användbart, men cancer beror sällan på en enda felaktig gen. Istället samarbetar grupper av gener för att störa hela signalvägar som styr tillväxt, överlevnad och immunitet. Författarna menar att fokus på enskilda gener missar detta samverkande beteende och kan misslyckas med att förklara varför tumörer ser ut och beter sig som de gör i mikroskopet.
Att bygga en karta mellan bilder, gener och vägar
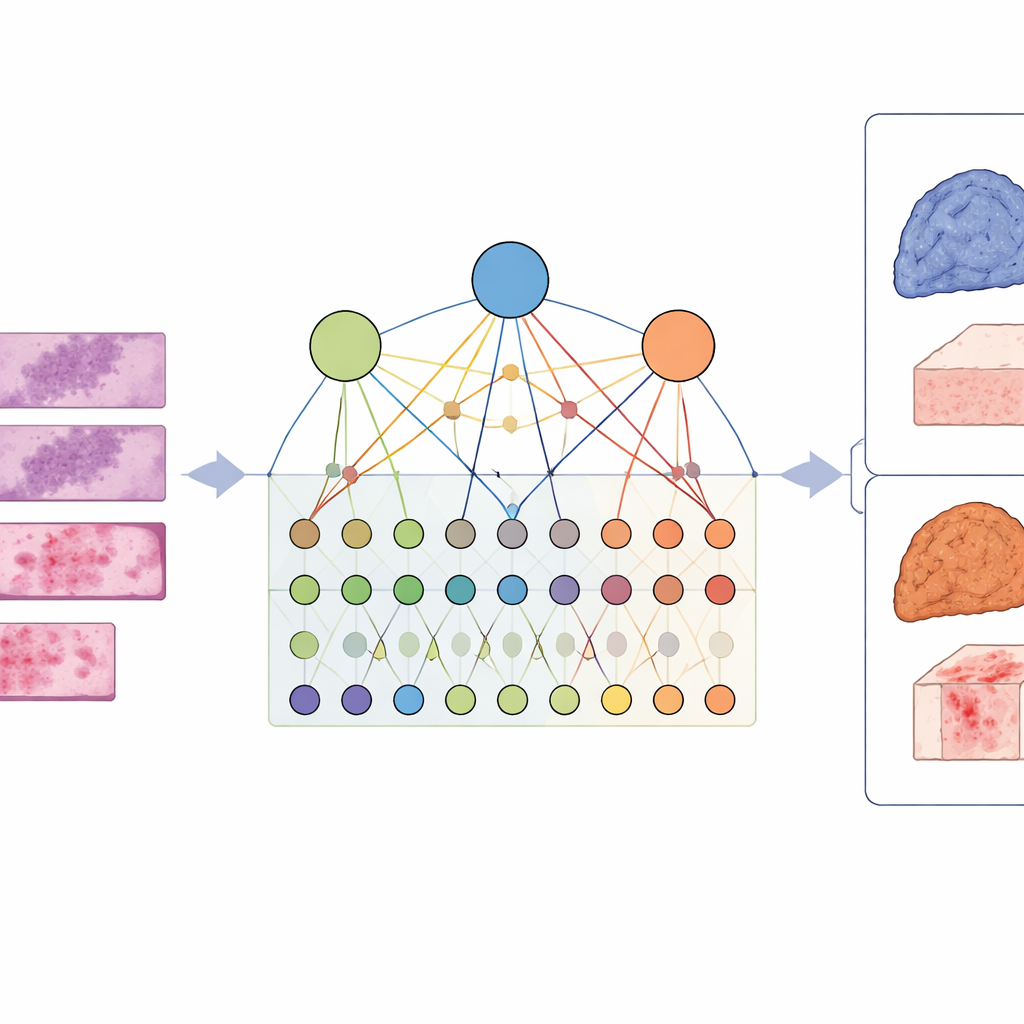
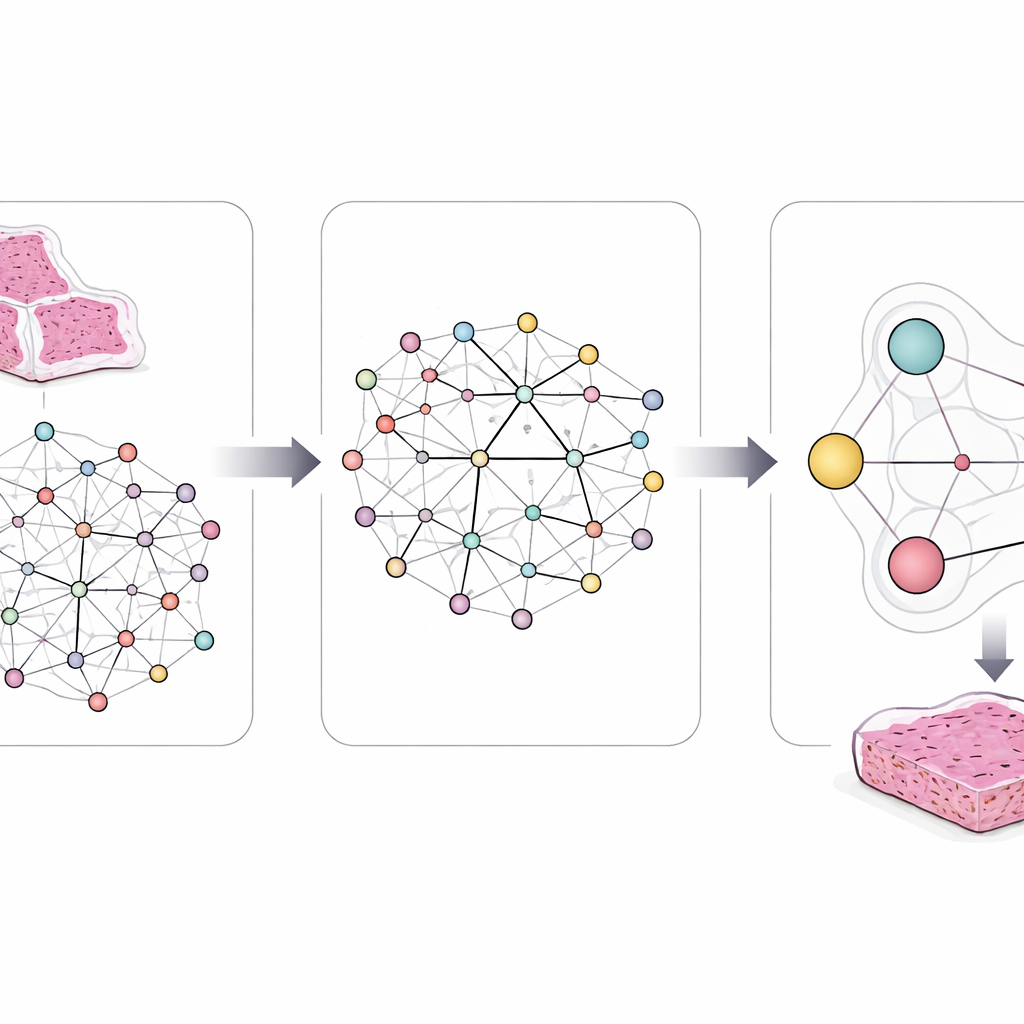
För att fånga denna komplexitet utformade forskarna en ram kallad LCG-HGNN som länkar tre informationslager. Först delar de varje helbild av lungadenokarcinom i många små fält och representerar dessa fält som en graf, där närbelägna eller liknande regioner är förbundna. För det andra kopplar de genmarkörer till signalvägar med hjälp av etablerade biologiska databaser och bygger en andra graf som kodar vilka gener som tillhör vilka vägar. Slutligen låter de en AI-modell föra information genom denna kombinerade graf, så att bildmönster, gener och vägar påverkar varandra istället för att behandlas isolerat.
Att lära systemet känd biologi
En viktig nyhet är att modellen inte tillåts lära fritt utan vägledning. Författarna inbäddar tydliga, regel-liknande uttalanden härledda från årtionden av cancerforskning. Till exempel förekommer vissa mutationer nästan aldrig tillsammans i samma tumör, och vissa vägar ligger uppströms eller nedströms om andra. De kodar sådana regler som logiska begränsningar som försiktigt styr AI:ns interna samband och prediktioner. Om modellen föreslår en kombination av gen- och vägförändringar som strider mot känd biologi eller mot likheter mellan patienternas bilder, trycker dessa regler den mot mer realistiska alternativ.
Testa noggrannheten mot befintliga metoder
Teamet utvärderade sitt system på över 1 600 lungcancerpreparat kopplade till genetiska data. De jämförde det med standard djupa inlärningsmodeller som fokuserar på enskilda gener och med mer avancerade metoder som hanterar många gener samtidigt men ignorerar vägstruktur. Över flera viktiga vägar, inklusive de som involverar celltillväxtsignaler och vävnadens stödstruktur, förutsade den nya modellen förändringar i gengrupper och avvikelser i vägar mer korrekt. Den producerade också bildfält vars utseende nära matchade verkliga kliniska exempel som är kända för att vara associerade med specifika mutationer, vilket tyder på att den fokuserade på meningsfulla mikroskopiska mönster snarare än slumpmässiga bildbrisyrer.
Varför detta spelar roll för patienter
För en icke-specialist är huvudresultatet att detta tillvägagångssätt förvandlar ett rutinmässigt patologipreparat till en rik källa till molekylär insikt. Istället för att beställa separata, ofta kostsamma genetiska tester för varje möjligt mål, skulle läkare så småningom kunna använda sådana modeller för att screena efter störda vägar direkt från de bilder de redan samlar in. Metoden behöver fortfarande större, verkliga valideringar och ersätter ännu inte genomiska tester, men den pekar mot en framtid där mikroskopvyn dubblas som ett fönster in i tumörens inre kopplingar—hjälpande till att vägleda mer precis och biologiskt informerad cancerbehandling.
Citering: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
Nyckelord: cancervägar, histopatologi AI, grafneurala nätverk, lungadenokarcinom, digital patologi