Clear Sky Science · sv
Användning av in vitro samexponeringsmodeller för att informera bakterieingenjörskonst vid behandling av solida tumörer
Varför bakterier i cancer kan vara viktiga för dig
Behandlingar mot cancer som operation, kemoterapi och strålbehandling räddar liv men medför ofta svåra biverkningar och alltför ofta behandlingar som misslyckas. En intressant ny idé är att använda levande bakterier som precisa verktyg som kan hitta och angripa solida tumörer inifrån. Den här artikeln förklarar hur forskare bygger laboratorietestsystem—där mänskliga celler och bakterier växer tillsammans—för att utforma säkrare, smartare bakterieterapier innan de når patienterna.
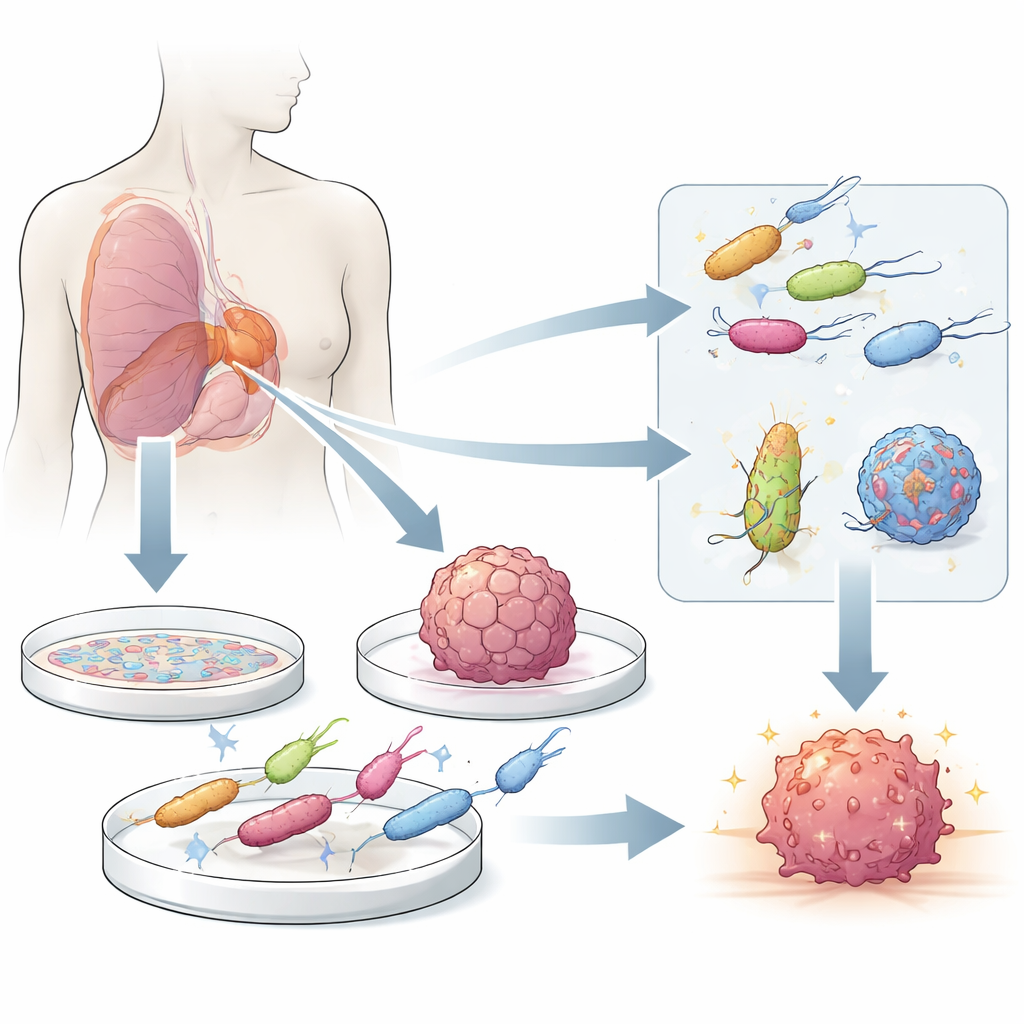
Små hjälpare som söker upp tumörer
Vissa bakterier föredrar naturligt den hårda, syrefattiga miljön inne i solida tumörer framför frisk vävnad. Efter att ha smugit igenom läckande tumörblodkärl eller åkt med immunceller rör sig dessa mikrober mot döende och döda celler i tumörens kärna, där de kan växa och ibland utlösa cancercelldöd och lokala immunsvar. Modern genteknik förvandlar dessa naturliga ”tumörsökande” stammar till levande transportörer som kan släppa ut läkemedel, immunstimulerande ämnen eller andra laster precis där de behövs som mest, samtidigt som ansträngningar att försvaga deras skadliga egenskaper ökar säkerheten.
Bygga realistiska laboratorie-mini-tumörer
För att förstå och förbättra dessa levande läkemedel behöver forskare testbäddar som efterliknar vad som händer i människokroppen så nära som möjligt. Enkla plana cellager är lätta att odla och nyttiga för snabb screening, men de missar tumörers komplexa struktur och syregradienter. Tredimensionella modeller, såsom sfäroider gjorda av cancercellinjer och organoider odlade från patientvävnad, återskapar bättre nyckelfunktioner som ett levande yttre skal, en tyst inre zon och en död kärna. När bakterier blandas direkt med dessa mini-tumörer kan forskare se hur de invaderar, var de ackumuleras och hur väl konstruerade läkecirklar fungerar i förhållanden som liknar en patients tumör.
Separera celler för att studera signaler
Andra samexponeringsdesigner fokuserar mindre på fysisk kontakt och mer på de osynliga kemiska utbytena mellan bakterier och mänskliga celler. I transwell-system delar ett poröst membran två kammare så att små molekyler passerar medan celler stannar kvar. Detta låter forskare testa till exempel hur en bakteriell stam omvandlat en ofarlig förening till en tumördödande gas som diffunderat över till närliggande cancerceller. Mikrofluidiska chips—små enheter med kanaler och fack—lägger till ytterligare en nivå av realism. De kan kontrollera vätskeflöde, syrenivåer och tidpunkter, vilket tillåter att konstruerade bakterier växer, brister i synkroniserade cykler och upprepade gånger badar cancerceller i terapeutiska molekyler, samtidigt som man noggrant följer hur båda parter svarar över tid.
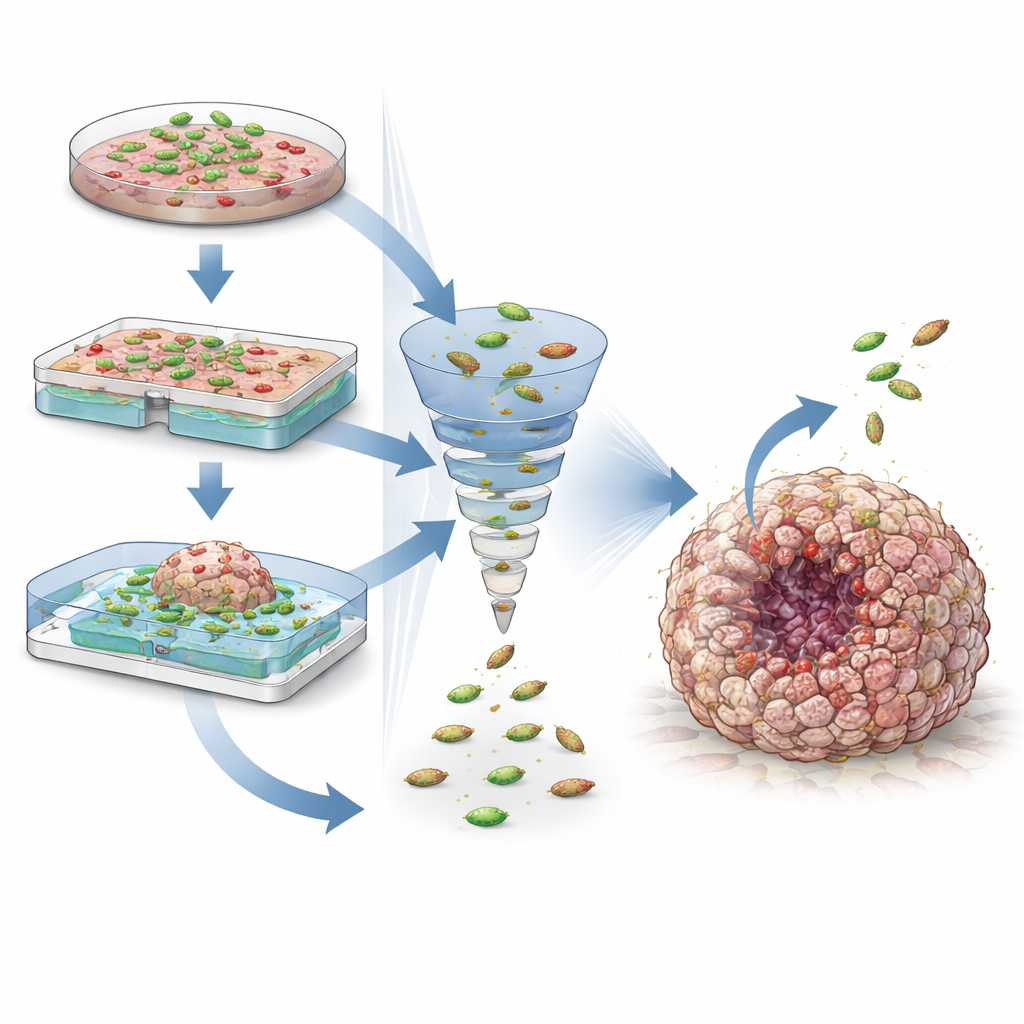
Insyn i tumörekosystemet
Samexponeringsmodeller används också för att studera hur bakterier interagerar med det bredare tumörekosystemet. Organoider härledda från enskilda patienter kan bevara många av de genetiska särdragen och läkemedelsresponserna hos sina ursprungliga tumörer, vilket öppnar dörren för personligt anpassade tester av bakterieterapier. Att lägga till immunceller i dessa kulturer visar hur bakterier kan förstärka eller dämpa antitumörimmunitet och hur de kan kombineras med läkemedel som checkpoint-hämmare. Samtidigt varnar dessa modeller för säkerhetsproblem, såsom bakteriella toxiner som skadar DNA och potentiellt kan bidra till att utlösa cancer. Genom att justera odlingsförhållanden, syrenivåer och mätmetoder—från levande avbildning till DNA-sekvensering—kan forskare systematiskt utforska dessa fördelar och risker.
Från labbbänk till vårdrum
Trots lovande resultat i djurstudier har mycket få bakteriebaserade cancerterapier visat tydliga fördelar i mänskliga studier. Författarna menar att smartare användning av samexponeringssystem kan överbrygga detta gap. Genom att bättre fånga patient-till-patient-variation, tumörkomplexitet och tidigare behandlingar kan dessa modeller identifiera vilka konstruerade stammar som är mest lovande, hur de bör kombineras med befintliga läkemedel och var de kan misslyckas. De betonar också behovet av gemensamma standarder så att laboratorier över hela världen kan jämföra resultat och så att tillsynsmyndigheter tryggare kan bedöma säkerhet och effektivitet. Med enkla ord erbjuder noggrant designade laboratorie-mini-tumörer odlade sida vid sida med bakterier ett kraftfullt sätt att finslipa dessa ”smarta buggar”, vilket ökar chansen att framtida patienter får bakterieterapier som är både säkrare och mer effektiva.
Citering: Foschini, S., Wright, J.A., Woods, S.L. et al. Use of in vitro co-culture models to inform bacterial engineering for the treatment of solid tumours. npj Biomed. Innov. 3, 21 (2026). https://doi.org/10.1038/s44385-026-00075-9
Nyckelord: bakteriell cancerterapi, tumororganoider, samexponeringsmodeller, syntetisk biologi, tumörmikromiljö