Clear Sky Science · sv
3D-biofabricerade in vitro-modeller som nya metodologier för alternativ till djurförsök
Ompröva hur vi testar nya läkemedel
I nästan ett sekel har de flesta nya läkemedel testats på djur innan de når mänskliga prövningar. Ändå misslyckas mer än 9 av 10 läkemedelskandidater som verkar säkra i djur när de provas på människor. Den här artikeln undersöker hur en ny generation 3D–"bioprintade" humana vävnader kan förändra den berättelsen—genom att erbjuda mer exakta, humana sätt att förutsäga hur våra kroppar reagerar på läkemedel, och potentiellt skynda på säkrare behandlingar till patienter.

Från försöksdjur till människocentrerad testning
Ny lagstiftning i USA, känd som FDA Modernization Act 2.0, har tagit bort det automatiska kravet att varje nytt läkemedel måste testas på djur. Istället kan tillsynsmyndigheter nu godta "New Approach Methodologies"—testsystem relevanta för människor som är utformade för att bättre förutsäga verkliga patientreaktioner. Bland dessa sticker 3D-bioprinting ut. Metoden använder specialiserade skrivare för att placera levande mänskliga celler och mjuka, geléaktiga material i intrikata former som efterliknar riktiga vävnader och mini‑organ. Processen börjar ofta med medicinska bilder som CT- eller MR-undersökningar, som ger en ritning. Forskare väljer sedan lämpliga biomaterial, blandar in rätt celltyper för att skapa en utskrivbar "bioink" och skriver ut lager- eller volymstrukturer som mognar till funktionella vävnadsmodeller i bioreaktorer.
Hur 3D-bioprinting bygger levande vävnader
Bioprinting är inte en enda teknik utan en familj av metoder. Bläckstråleliknande skrivare sprutar ut små droppar av cellinnehållande vätska för att bygga tunna lager med fin detaljrikedom, vilket gör dem användbara för miniatyrvävnader såsom hudlappar eller lungbarriärer. Extrusionsskrivare pressar ut kontinuerliga strängar av tjockare bioinks, som kan innehålla många celler och stödjande fibrer, vilket möjliggör konstruktion av större, mer robusta strukturer som hjärtklaffar, levertumörmodeller eller kärlnätverk. En nyare klass, kallad vat-fotopolymerisation, riktar mönstrat ljus in i en vätska för att härda komplexa former utan att klämma celler genom munstycken. Varianter av denna metod kan skulptera funktioner i mikrometerskala, skriva ut ett helt litet organ på sekunder eller till och med forma vävnader inuti ett transparent bad, samtidigt som cellerna håller sig vid liv.
Byta ut och förfina läkemedelstester
Dessa utskrivna vävnader används redan för att ompröva läkemedelsprocessen. I tidig upptäckt tillåter patient- eller sjukdomsspecifika konstruktioner—som bioprintade tumörmodeller—forskare att testa många läkemedelskandidater i realistiska 3D‑miljöer som bättre liknar mänsklig sjukdom än platta cellager i en skål. I prekliniskt testande visar tryckt hud, lunga och levervävnad sig mer träffsäkra än djur för att upptäcka människospecifik toxicitet eller biverkningar. Några studier går längre genom att skriva ut "kliniska prövningar på ett chip", där vävnader gjorda av celler från olika donatorer exponeras för ett läkemedel parallellt, och avslöjar vem som kan dra nytta av eller skadas av behandlingen. Tillsynsmyndigheter uppmuntrar nu företag att lämna in data från dessa modeller tillsammans med djurstudier, för att bygga upp den evidens som behövs för bredare acceptans.
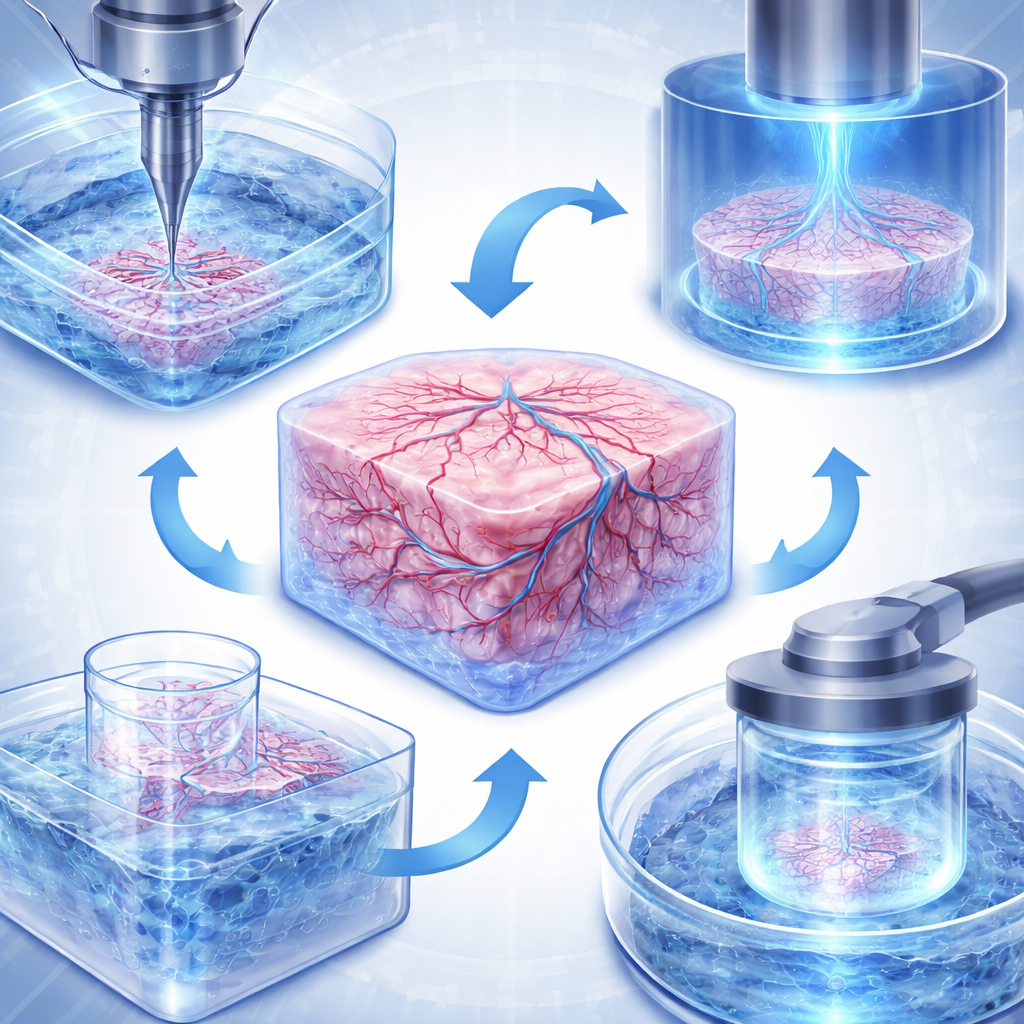
Konstruera organ utan en kropp
Trots snabb utveckling återstår flera hinder innan bioprintade vävnader rutinmässigt kan ersätta djurtester. En stor utmaning är blodförsörjning: riktiga organ innehåller kärlnät som varierar från stora artärer ner till hårfina kapillärer, medan tryckta konstruktioner måste övervinna en naturlig gräns för hur långt syre och näringsämnen kan diffundera. Forskare angriper detta med nya printstrategier som skapar förgrenade kanaler, med stödbad som håller mjuka vävnader på plats medan små kärl bildas, och med blixtsnabba volymetriska skrivare som tillverkar tjocka, celldensiva strukturer innan cellerna börjar lida. En annan utmaning är realism: levande vävnader är blandningar av många celltyper badande i komplexa kemiska signaler och ofta påverkade av mikrobiomet och avlägsna organ. Avancerade modeller kombinerar nu flera cellpopulationer, kontrollerade gradienter av syre och pH, och till och med sammankopplade "multi‑organ"-system som förbinder tarm, lever, immunsystem och hjärnvävnad genom flödande vätska för att efterlikna helkroppsreaktioner.
En humanare, prediktiv framtid för läkemedelsutveckling
Tillsammans tyder dessa framsteg på en framtid där högfidelitets, människobaserade vävnadsmodeller blir centrala för hur vi utvärderar läkemedel. Artikeln slår fast att 3D-bioprinting rör sig från en nischlaboratorieteknik till ett kärnverktyg för att bygga standardiserade, regulatoriskt godkännande provsystem. För att fullfölja detta löfte måste forskare och tillsynsmyndigheter enas om var och hur dessa modeller bör användas, bevisa att de pålitligt förutsäger mänskliga utfall och lösa kvarstående tekniska utmaningar såsom att bygga stabil vaskulatur och anatomiskt komplexa organ. Om detta lyckas kan skiftet minska beroendet av djurförsök, kapa kostsamma sena läkemedelsmisslyckanden och leverera säkrare, mer effektiva terapier samtidigt som det bättre speglar den biologi som betyder mest: vår egen.
Citering: Hua, W., Gaharwar, A.K. 3D biofabricated in vitro models as new approach methodologies for animal alternatives. npj Biomed. Innov. 3, 20 (2026). https://doi.org/10.1038/s44385-026-00073-x
Nyckelord: 3D-bioprinting, alternativ till djurtester, Läkemedelsutveckling, vävnadsmodeller, volumetrisk bioprinting