Clear Sky Science · sv
Ingenjörsmässigt utformade makrofager för cancerimmunterapi: nya insikter och terapeutisk potential
Att förvandla kroppens städpatrull till cancerbekämpare
Våra kroppar är fulla av makrofager — vandrande "städ"-celler som slukar bakterier och död vävnad. Denna översiktsartikel undersöker hur forskare lär sig omdirigera dessa celler mot cancer. Eftersom makrofager är rikliga i tumörer, även i sådana som är resistenta mot dagens ledande immunterapier, kan förståelse och ingenjörskonst kring dem öppna nya alternativ för patienter med svårt behandlade cancerformer.
En cells många ansikten
Makrofager är inte en enhetlig, fast celltyp; de förändrar sig. De kan komma från blodet eller redan finnas i vävnader, och när de väl etablerat sig svarar de på lokala signaler. I tumörer kan dessa tumörassocierade makrofager antingen hjälpa till att döda cancerceller eller, förvirrande nog, främja tumörtillväxt och spridning. Tidigare försökte forskare pressa in dem i två fack — ”M1” (attackläge) och ”M2” (reparations- eller stödjande läge). Nya genetiska och spatiala kartläggningsverktyg visar nu ett mycket rikare spektrum av tillstånd, med flera undergrupper och beteenden som varierar mellan tumörer och platser. Även celler som tidigare ansågs vara entydigt ”pro-tumör” kan i vissa sammanhang mobilisera T‑celler och stödja antitumoral immunitet.
Känna av omgivningen och äta cancerceller
Makrofager lyssnar inte bara på kemiska signaler; de känner också av den fysiska omgivningen. När de kryper genom en tumörs täta proteinmatris, pressar sig mellan celler och utsätts för vätskekrafter, uppfattar de styvhet och dragkrafter via specialiserade receptorer som Piezo1. Dessa mekaniska signaler, tillsammans med klassiska immunsignaler, kan luta makrofager mot mer inflammatoriska eller mer dämpande roller. Funktionellt kan makrofager omsluta cancerceller, sönderdela dem och visa upp fragment (antigener) för T‑celler, vilket kopplar samman medfödd och adaptiv immunitet. Cancerceller försvarar sig genom att skicka "ät mig inte"-signaler, särskilt via en ytmolekyl kallad CD47 som binder en broms på makrofager. Läkemedel som blockerar denna interaktion finns i många kliniska studier och ökar rensningen av cancerceller, men kräver noggrann avvägning för att undvika skada på friska celler.
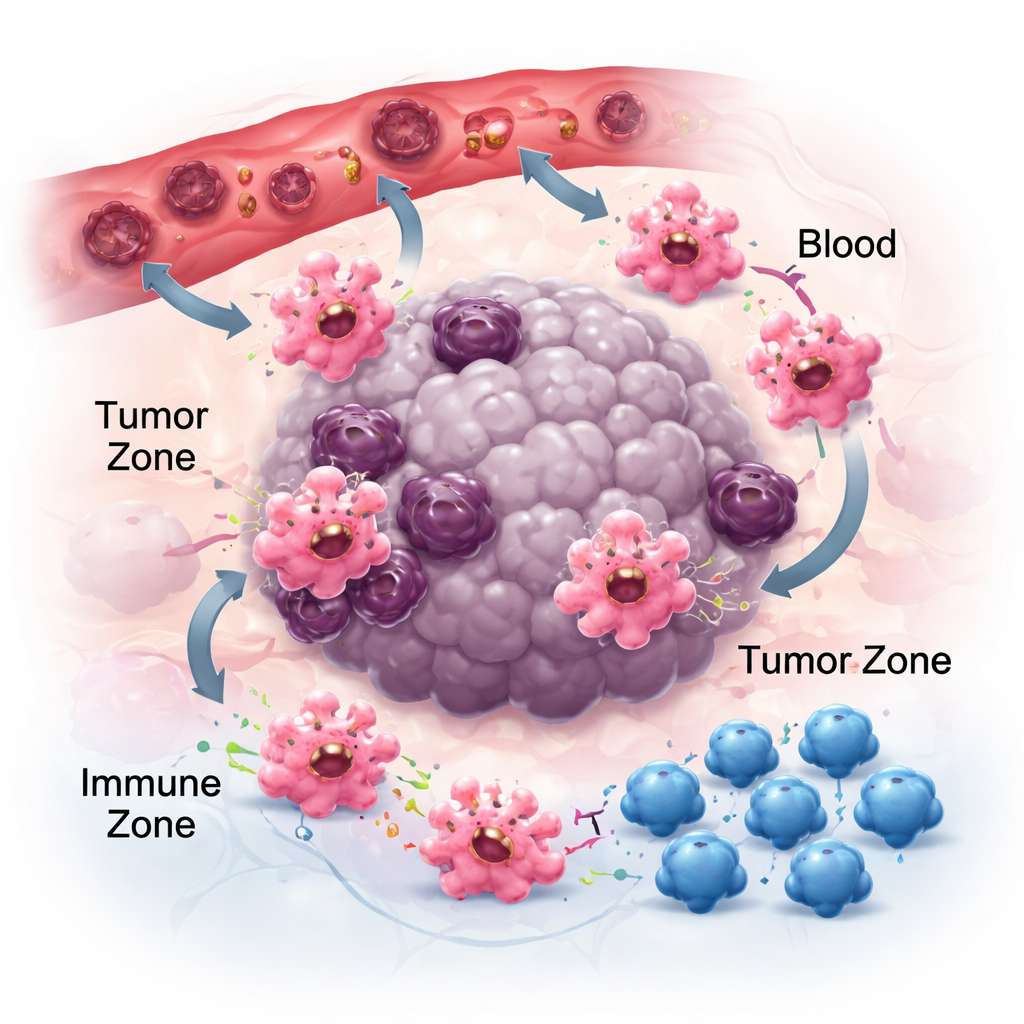
Röra sig, fästa och kommunicera i tumöromgivningen
För att vara verksamma i cancer måste makrofager först nå tumörer och sedan positionera sig i rätt nischer. De följer kemiska spår — kemokiner och tillväxtfaktorer — som frisätts av cancer- och omgivande celler. Par som CCR2–CCL2 hjälper till att locka in dem i tumörer, och läkemedel som blockerar dessa signaler kan minska makrofagansamling, om än inte helt, vilket pekar på andra attraktanter som CSF‑1 och VEGF. När de väl är på plats formar också hur makrofager fäster i den lokala matrisen deras beteende. Deras adhesionsreceptorer, så kallade integriner, fungerar inte bara som lim; de förstärker inflammatoriska signaler och kan styra celler mot mer tumörbekämpande tillstånd. Samtidigt avger makrofager små paket kallade extracellulära vesiklar som bär RNA och proteiner till närliggande celler. Beroende på tumörtyp kan dessa vesiklar antingen dämpa immuniteten och underlätta spridning eller stärka antitumorala svar, vilket framhäver den kontextberoende naturen i makrofagkommunikation.
Omkodning av makrofager med gener och material
Eftersom makrofager naturligt infiltrerar solida tumörer bättre än många T‑celler, omformar forskare dem nu till levande läkemedel. En genetisk strategi lånar från chimeric antigen receptor (CAR) T‑cellsterapi: man lägger till en syntetisk receptor för att skapa CAR‑makrofager (CAR‑M). Dessa designer-celler känner igen tumörmarkörer, omsluter cancerceller mer effektivt, bryter ner den omgivande matrisen, släpper inflammatoriska signaler och aktiverar T‑celler genom att presentera tumörantigener. Tidiga mänskliga prövningar av HER2‑inriktade CAR‑M visar uppmuntrande säkerhetsdata och biologisk aktivitet, även om mer arbete behövs för att visa starka, bestående fördelar. Parallellt använder icke‑genetiska metoder partiklar och ”ryggsäckar” gjorda av lipider eller polymerer. Makrofager kan sluka läkemedelsladdade nanopartiklar och bära dem djupt in i tumörer som trojanska hästar, eller bära ytfästa patchar som långsamt frisätter immunstimulerande signaler, vilket hjälper dem behålla en tumörbekämpande identitet utan att överbelasta sitt inre. Vesiklar härledda från makrofager testas också som naturliga, cellfria leveranssystem.
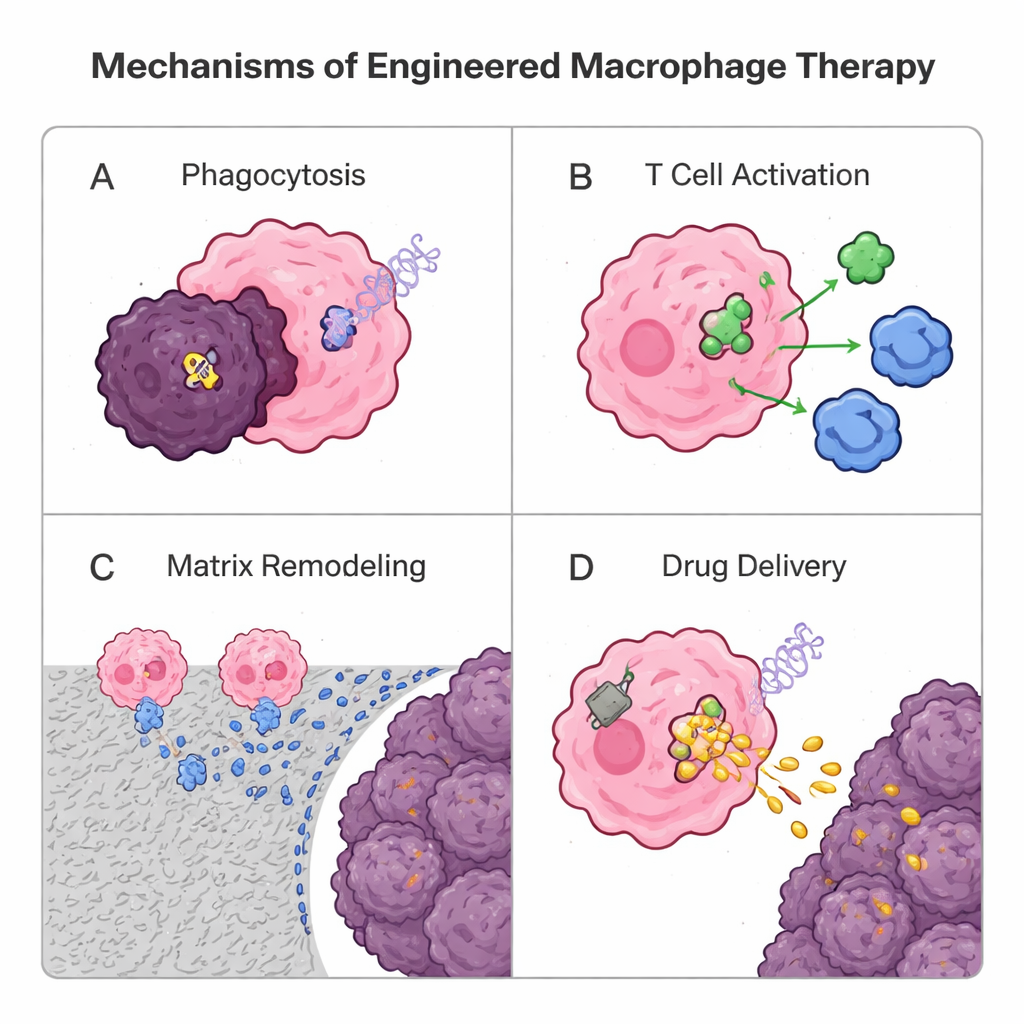
Framtida utmaningar och skäl till hopp
Trots löftena måste makrofagterapier övervinna praktiska hinder. Det tar tid och är kostsamt att framställa tillräckligt många konsekventa celler från patienter, och när de väl infunderats lever eller förökar sig inte dessa celler oändligt. Deras inneboende flexibilitet, samtidigt biologiskt användbar, kan göra det svårt att hålla dem låsta i ett antitumoralt läge i en komplex, hämmande tumörmikromiljö. Författarna menar att avancerade bioingenjörsmodeller — 3D‑kulturer, organoider och organ‑on‑a‑chip‑system som efterliknar verklig vävnadsmekanik — blir avgörande för att förstå och förutse hur ingenjörsberedda makrofager beter sig hos patienter. Ändå, deras naturliga förmåga att tränga in i solida tumörer, äta cancerceller och väcka T‑celler, i kombination med en tidig säkerhetsprofil, antyder att makrofagbaserade terapier kan bli ett viktigt nytt vapen, särskilt mot ”kalla” tumörer som i dag är resistenta mot de flesta immunbehandlingar.
Citering: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
Nyckelord: makrofagimmunterapi, tumörmikromiljö, CAR-makrofager, fagocytos, nanopartikelleverans av läkemedel