Clear Sky Science · sv
Nukleinsyra-baserade terapier för att återställa ledens homeostas vid åldersrelaterad och posttraumatisk artrit
Varför värkande leder behöver nya typer av mediciner
Artros, den vanligaste formen av artrit, avfärdas ofta som enkel ”slitage”, men är i själva verket en komplex sjukdom där ledens naturliga balans mellan skada och reparation rubbas. Eftersom människor lever längre och är aktiva högre upp i åldrarna blir smärtsamma, stela leder en allt större orsak till funktionsnedsättning, och dagens behandlingar dämpar mest symtom eller slutar i kostsamma ledprotesoperationer. Denna översiktsartikel utforskar en ny klass av behandlingar byggda på genetiska instruktioner — små RNA-trådar — som syftar till att inte bara lindra smärta utan att återställa en hälsosam balans inne i skadade leder.
Från nedsliten brosk till genomgripande ledsammanbrott
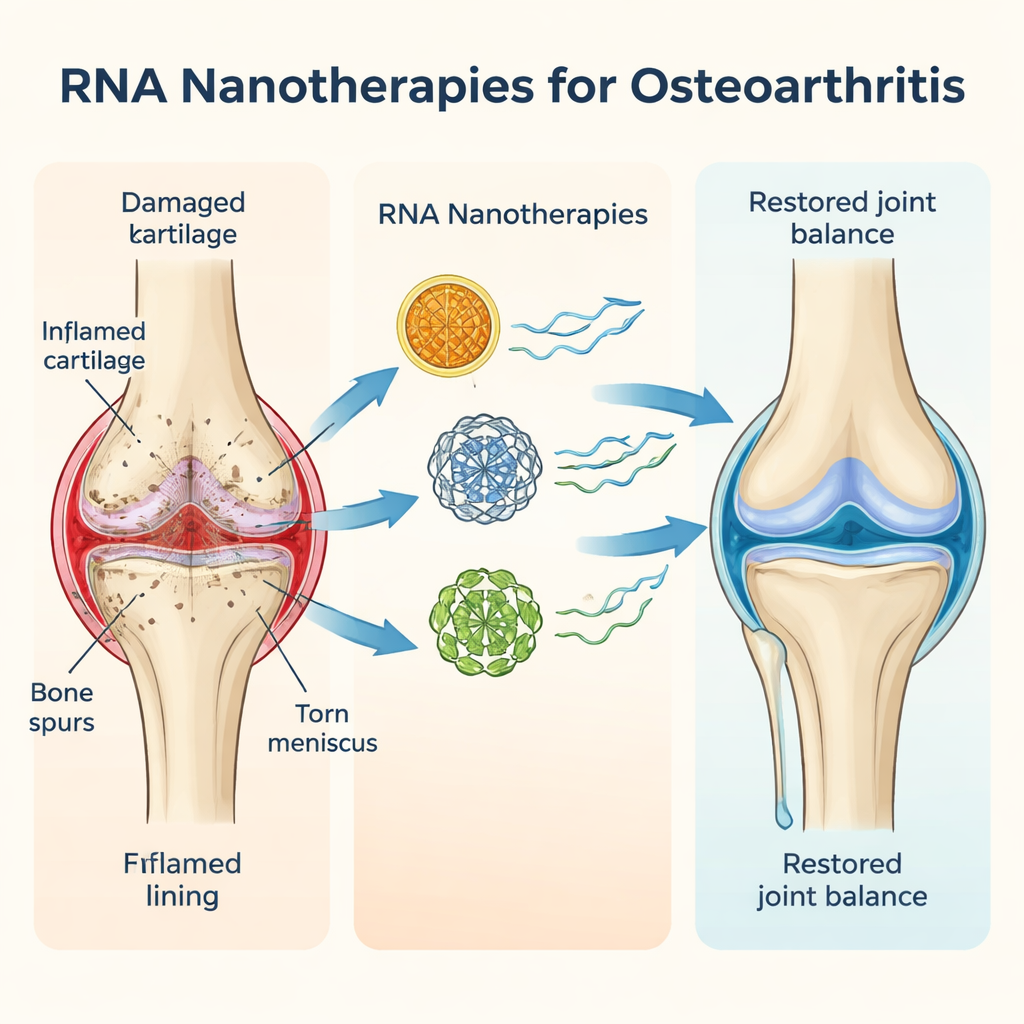
Artros betraktas nu som en helledssjukdom, inte bara ett problem med tunnare brosk. I ett artroseramt knä slits till exempel det släta brosket som dämpar benen bort, menisken kan fransas, underliggande ben förtjockas och ledkapseln blir inflammerad. Denna låggradiga, kroniska inflammation göder tyst sjukdomen under åratal. Författarna beskriver hur ålder, skada, övervikt och genetik samverkar för att välta balansen mot katabola processer som bryter ner vävnad och överväldigar de anabola processer som reparerar den. Eftersom varje patients sjukdom drivs av en något annorlunda mix av faktorer varierar svaren på vanliga behandlingar som smärtstillande, injektioner eller kirurgi stort, och i dag finns ingen läkemedel som verkligen kan stoppa eller vända artros.
Varför traditionella behandlingar inte räcker till
Översikten redogör för många nuvarande alternativ — från receptfria smärtstillande och kortisoninjektioner till sjukgymnastik, ortoser och avancerade ingrepp som broskimplantat. Var och en har fördelar men också tydliga nackdelar. Smärtstillande kan irritera mage eller hjärta, steroider kan skada brosk vid upprepad användning, och regenerativa metoder som plasma med rikligt antal blodplättar eller stamceller är dyra och saknar långsiktiga bevis. Viktigast är att nästan alla befintliga läkemedel bara angriper ena sidan av problemet: antingen försöker de dämpa inflammation och bromsa nedbrytning, eller så försöker de öka reparation. Få metoder angriper båda sidor samtidigt, vilket sannolikt förklarar varför de har svårt att ändra sjukdomens förlopp.
RNA-läkemedel: Omformulera ledens inre manus
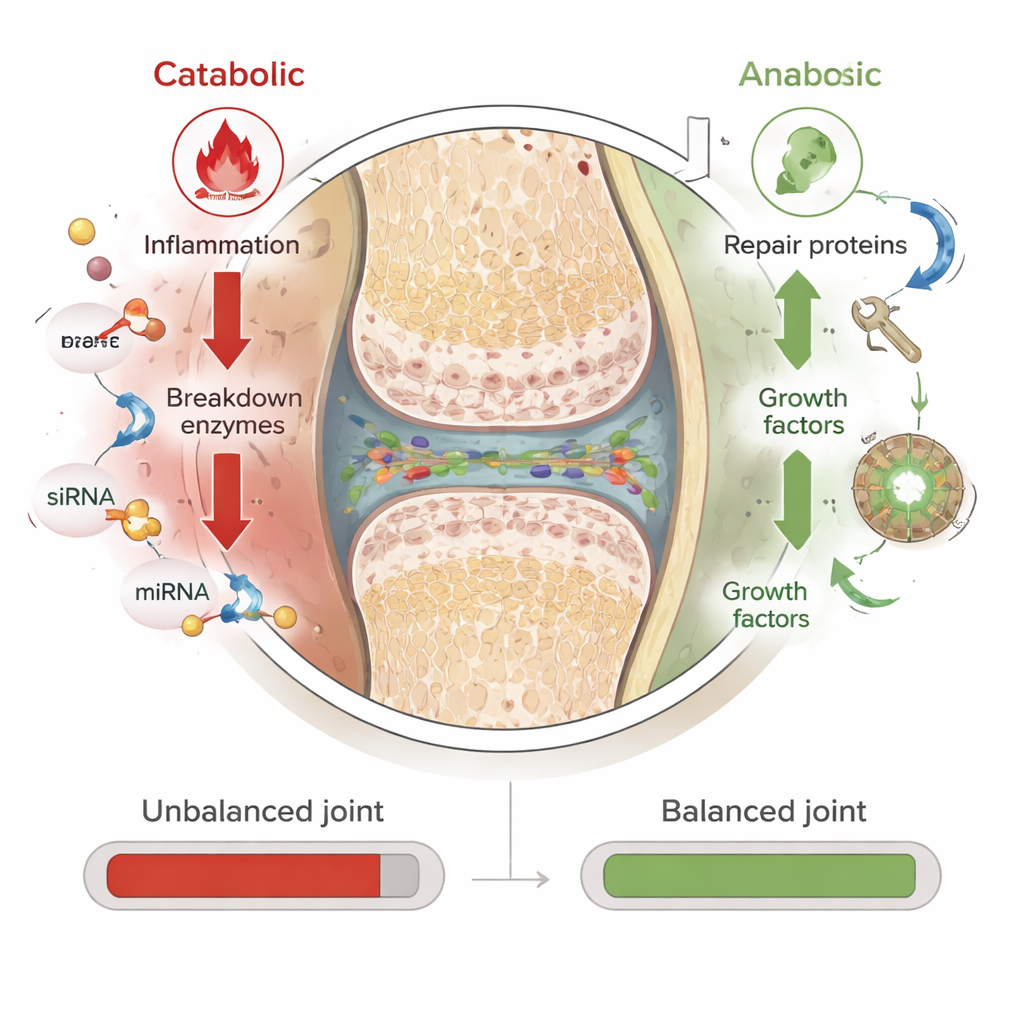
RNA-baserade terapier verkar på en annan nivå. I stället för att rikta in sig på proteiner efter att de bildats, verkar de på de kortlivade genetiska meddelanden som talar om för celler vilka proteiner de ska bygga. Författarna fokuserar på tre typer. Small interfering RNA (siRNA) kan tysta ett enda skadligt gen med hög precision. MicroRNA (miRNA) kan fint justera hela gen-nätverk och dämpa flera skadliga vägar samtidigt. Messenger-RNA (mRNA) gör motsatsen: det tillför instruktioner för att göra hjälpsamma proteiner, såsom tillväxtfaktorer som stimulerar broskreparation eller molekyler som blockerar inflammatoriska signaler. Eftersom RNA verkar temporärt och inte ändrar DNA är dess effekter reversibla och i princip säkrare än permanent genredigering. Byggt på framgångarna med COVID-19 mRNA-vacciner testas nu liknande idéer i djurmodeller av artrit.
Nanopartiklar: få sköra budskap till rätt celler
En stor utmaning är att naken RNA är bräcklig och har svårt att ta sig in i celler. Översikten beskriver hur forskare paketerar RNA i skyddande ”nanoplattformar” — små bärare gjorda av fetter, polymerer eller korta peptider. Dessa nanopartiklar skyddar RNA från nedbrytning, hjälper det att passera genom den täta broskmatrixen och uppmuntrar celler i ledkapseln och brosket att ta upp det. I prekliniska studier har partklar laddade med siRNA använts för att stänga ner gener som driver inflammation, oxidativ stress och vävnadsnedbrytning, medan mRNA-laddade partiklar har ökat skyddande proteiner som främjar smörjning och reparation. Tidiga experiment visar mindre broskskada och mindre smärta i djurmodeller, vilket tyder på att genomtänkta kombinationer av anti-nedbrytande och pro-reparerande RNA en dag kan fungera som verkliga sjukdomsmodifierande behandlingar.
Hinder på vägen mot kliniken
Trots sina löften står RNA-nanomediciner för artros fortfarande inför viktiga hinder. Immunsystemet kan missta både RNA och dess bärare för inkräktare och utlösa oönskad inflammation i redan irriterade leder. Injektioner i leden rensas bort inom dagar till veckor, så långvariga fördelar kommer sannolikt att kräva smartare system för långsam frisättning eller upprepade doser. Tillverkning av RNA och nanopartiklar av hög kvalitet i stor skala är kostsamt, och regulatorer har begränsad erfarenhet av att utvärdera sådana läkemedel för långsamt progredierande ledsjukdomar. Slutligen, eftersom artros är så varierande från person till person, kommer läkare behöva bättre sätt att matcha specifika RNA-koktailer till varje patients unika mönster av ledspecifik skada och inflammation.
Vad detta betyder för personer med artrit
Enkelt uttryckt hävdar artikeln att för att verkligen hjälpa personer med artros måste framtida behandlingar göra mer än att dämpa smärta — de måste återställa ledens förlorade balans genom att sänka aktiviteten hos de gener som driver skada och höja de gener som stödjer reparation. RNA-baserade läkemedel, levererade med sofistikerade nanopartikelbärare, erbjuder ett flexibelt verktyg för att göra just detta. Även om de ännu inte är redo för klinisk användning och viktiga frågor om säkerhet, hållbarhet, kostnad och reglering återstår, ser författarna dem som en realistisk väg mot personligt anpassade, minimalt invasiva terapier som skulle kunna fördröja eller till och med förhindra behovet av ledbyte vid åldersrelaterad och skaderelaterad artrit.
Citering: Rai, M.F., Pham, C.T., Hou, K. et al. Nucleic acid-based therapeutics to restore joint homeostasis in age-related and post-traumatic arthritis. npj Biomed. Innov. 3, 17 (2026). https://doi.org/10.1038/s44385-026-00068-8
Nyckelord: artros, RNA-terapier, nanomedicin, ledregenerering, siRNA mRNA miRNA