Clear Sky Science · sv
Accelerera individualiserad medicin: miniatiserad patient‑härledd organoid‑läkemedelsscreening för att förutsäga cancerbehandlingssvar och mer därtill
Ta laboratoriet snabbare till sängen
För många med avancerad cancer kan det kännas plågsamt att vänta i veckor för att få veta om en kemoterapi fungerar. Denna studie undersöker ett sätt att snabba upp den tidslinjen genom att använda pyttesmå, laboratorieodlade kopior av patientens tumör — så kallade organoider — för att testa läkemedel i förväg. Genom att krympa och automatisera testprocessen siktar forskarna på att förutsäga vilka behandlingar som sannolikt hjälper, med avsevärt mindre vävnad och tid än vad nuvarande metoder kräver.
Mini‑tumörer i en skål
Patient‑härledda organoider är tredimensionella cellkluster odlade från en persons egen tumör. Till skillnad från traditionella tvådimensionella cellkulturer bevarar dessa mini‑tumörer mycket av originalcancerns genetiska mångfald och beteende. Tidigare arbete har visat att när organoider svarar — eller inte svarar — på ett läkemedel i labbet, får patienter ofta en liknande effekt i kliniken. Problemet är att standardtester med organoider använder hundratals organoider per brunn, vilket kräver mycket biopsimaterial och tar många veckor att slutföra, vilket begränsar deras användbarhet i verklig klinisk praxis där behandling måste starta snabbt.
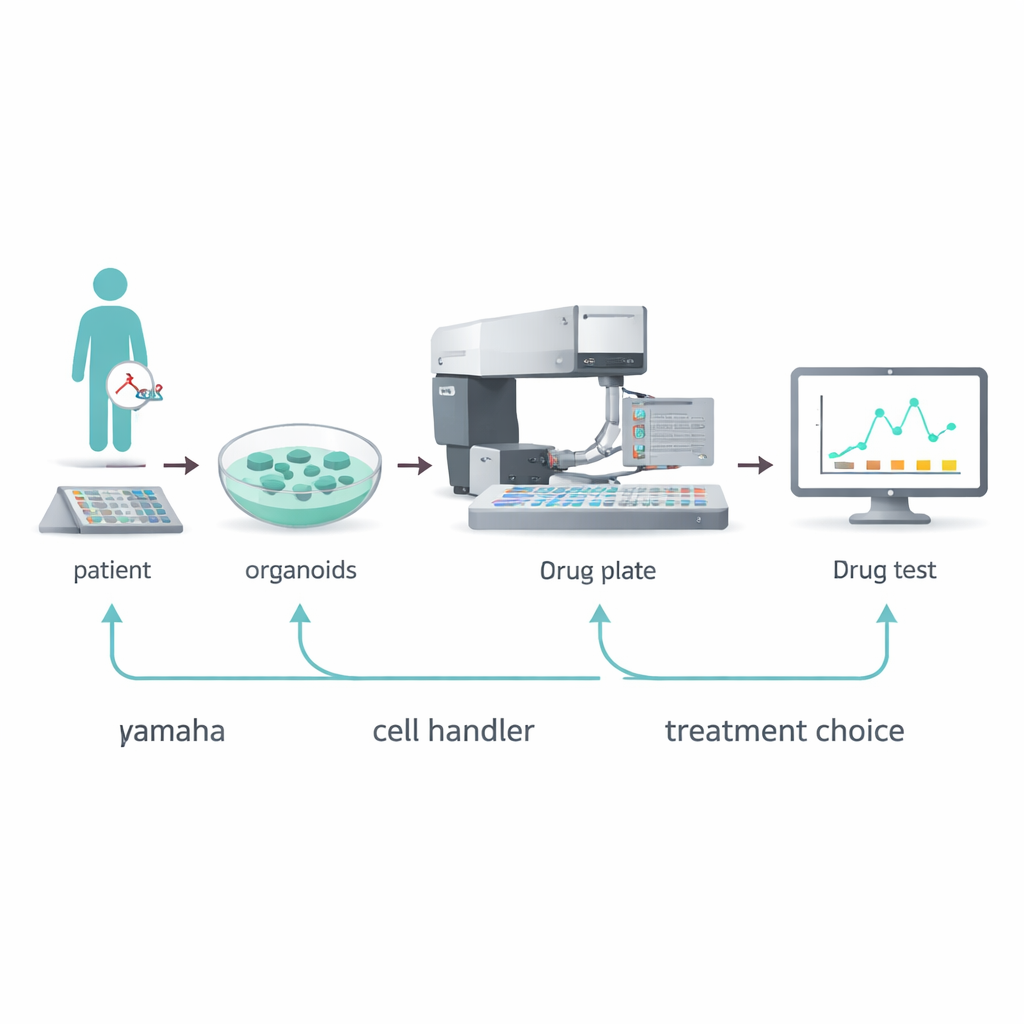
En robotplockare för pyttesmå tumörer
Forskargruppen vände sig till en automatiserad enhet, Yamaha Cell Handler, för att åtgärda dessa flaskhalsar. Denna robot använder en kamera för att hitta enskilda organoider i en källplatta, analyserar deras storlek och form, plockar sedan försiktigt upp utvalda organoider och fördelar dem i de små brunnarna i en 384‑brunnsplatta. Genom att finjustera hur många organoider som såddes, hur de stöddes i en gel‑liknande matris och vilka färgämnen och mätmetoder som användes, visade forskarna att bara 5 till 10 organoider per brunn räckte för tillförlitlig läkemedelsprovning. De optimerade också en DNA‑baserad fluorescensanalys som rapporterar hur många celler som förblir livskraftiga efter läkemedelsexponering och undviker därmed vissa fallgropar hos äldre energibaserade tester.
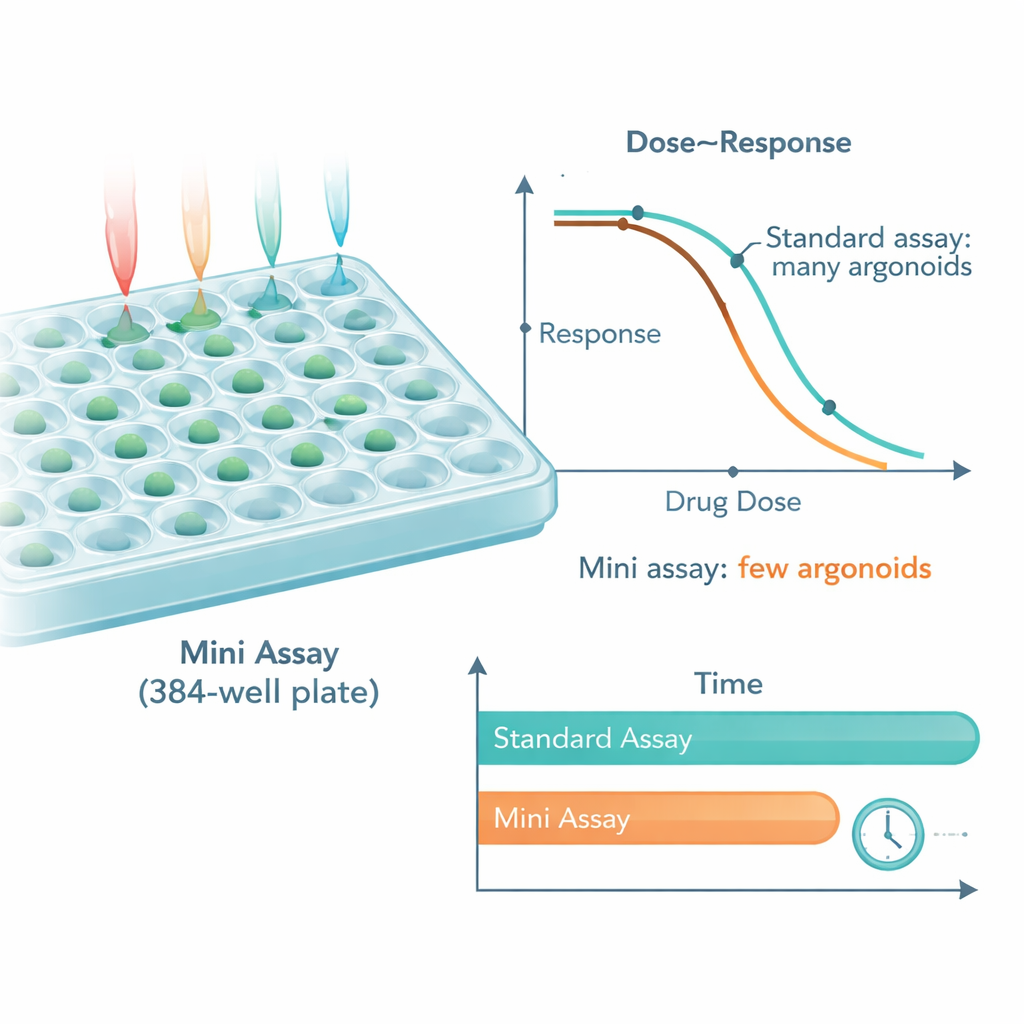
Göra mer med långt färre celler
Efter optimering använde det miniatiserade systemet så lite som 0,5 % till cirka 5 % av det material som krävs för konventionella screeningar, vilket minskade organoidbehovet med ungefär 25 gånger. Trots den drastiska nedskalningen matchade mönstren av läkemedelskänslighet mätta med 10 organoider per brunn väl de som sågs med 250 organoider per brunn. Plattformen kunde till och med avslöja dolda skillnader inom en enskild patients tumörmodell, såsom subgrupper av organoider som var känsliga eller resistenta mot en vanlig cytostatika. I ett exempel med en riktad antikroppsbehandling uppträdde organoider från tumörer med en känd resistensmutation som förväntat — de svarade inte — medan organoider utan den mutationen hämmades starkt, oavsett om de testades i standardformatet eller i det miniatiserade formatet.
Från laboratoriesignaler till patientutfall
Forskarna frågade därefter om detta mer slimmade test fortfarande speglade verkliga patientupplevelser. De testade organoider från personer med metastaserande kolorektal cancer som hade fått standardkemoterapi i kliniken. För både 5‑fluorouracil och oxaliplatin överensstämde läkemedelsresponser mätta i de miniatiserade analyserna (med endast 5–10 organoider per brunn och färre läkemedelskoncentrationer) väl med resultaten från större, traditionella screeningar. Viktigare för patienterna korrelerade organoidernas känslighet i miniassayet med hur länge patienternas cancer hölls under kontroll och i många fall med total överlevnad. Att reducera antalet organoider försvagade inte dessa samband, vilket tyder på att den strömlinjeformade metoden förblir kliniskt informativ.
Vad detta kan betyda för patienter
Genom att visa att precisa läkemedelsresponstester är möjliga med betydligt färre organoider och ett snabbare arbetsflöde förflyttar denna studie organoid‑baserad precisionsmedicin närmare rutinmässig klinisk användning. Den nya automatiserade plattformen minskar både antalet celler som krävs och ledtiden med ungefär hälften, vilket gör det mer realistiskt att odla organoider från en biopsi, testa flera terapier och ge resultat i tid för att vägleda behandlingsbeslut. Medan ytterligare validering över fler cancerformer behövs, erbjuder denna miniatiserade organoid‑screeningstrategi en praktisk väg mot att välja cancerläkemedel baserat på hur en individs egen tumör beter sig i labbet, snarare än att enbart förlita sig på populationsmedelvärden.
Citering: Abouleila, Y., Smabers, L.P., Voskuilen, T. et al. Accelerating personalized medicine: miniaturized patient-derived organoid drug screening for predicting cancer treatment responses and beyond. npj Biomed. Innov. 3, 16 (2026). https://doi.org/10.1038/s44385-026-00067-9
Nyckelord: cancerorganoider, individualiserad medicin, läkemedelsscreening, kolorektal cancer, automation inom onkologi