Clear Sky Science · sv
Ikvilibrium kemomekanisk omvandling av ATP-driven proteinutvikling i 26S-proteasomen
Hur en mikromaskin håller våra proteiner i schack
Inuti varje cell finns en mikroskopisk kvarn, 26S-proteasomen, som ständigt bryter ner skadade eller onödiga proteiner och därigenom håller cellen frisk. I centrum av denna maskin sitter en ringformad motor som förbrukar kemisk bränsle (ATP) för att greppa, veckla ut och dra in proteiner i ett centralt kammare där de mals sönder. Denna artikel använder avancerade datorsimuleringar för att visa hur motorn omvandlar kemisk energi till mekanisk rörelse och ger en detaljerad, kvantitativ bild av en process som ligger till grund för åldrande, hjärnsjukdom, immunitet och cancer.
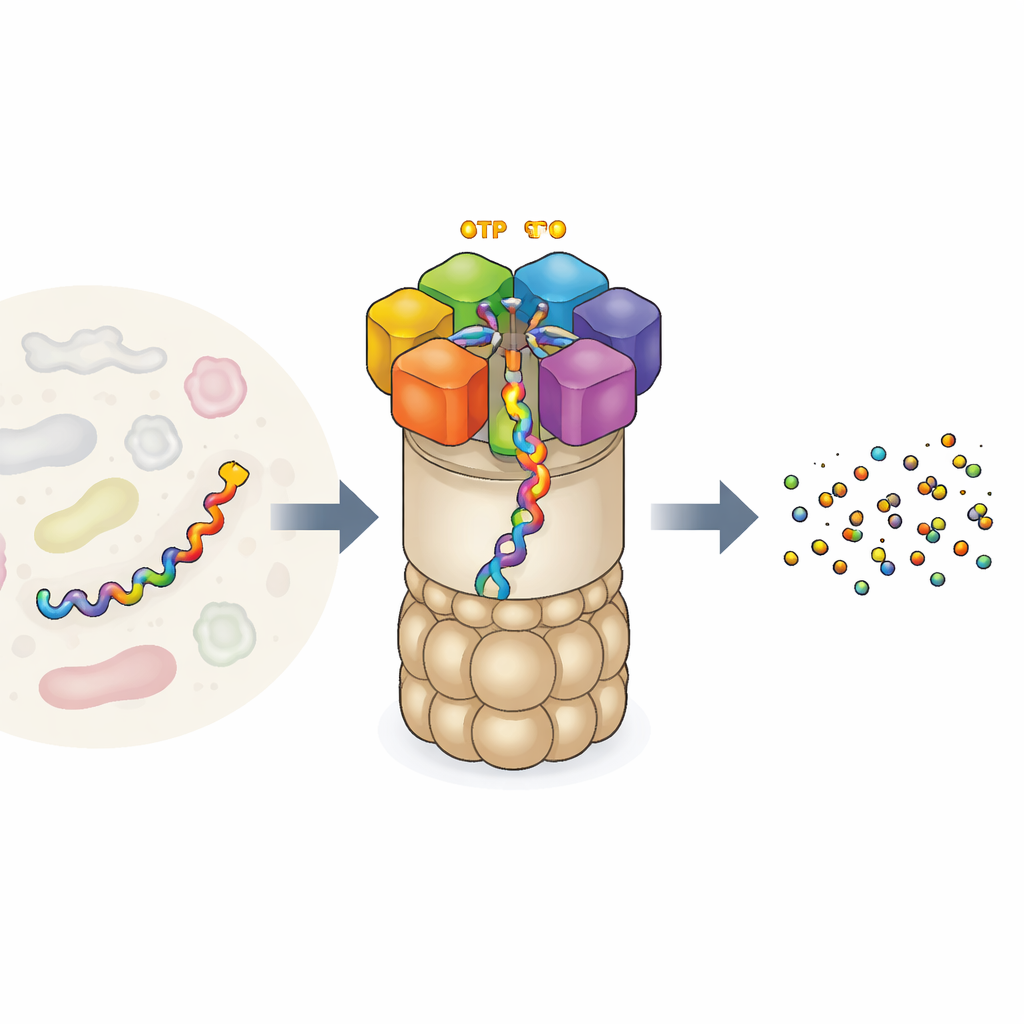
Cellens fabrik för proteinsamling
26S-proteasomen är en av de största och mest intrikata proteinmaskinerna i våra celler. Den består av en tunnliknande kärna som skär proteiner och ett regulatoriskt lock som känner igen vilka proteiner som ska förstöras. Vid ingången sitter en ring av sex olika motorenheter. Varje enhet kan binda ATP, cellens universella energivaluta, och använder den energin för att greppa en proteinkedja och dra in den i kärnan för nedbrytning. Motorn agerar inte slumpmässigt: tidigare experiment föreslog att de sex enheterna arbetar i en koordinerad ”hand-över-hand”-rörelse och skickar proteinet vidare som klättrare på ett rep. Men experimenten fångade bara några ögonblicksbilder av denna handling, vilket lämnade frågetecken kring hela rörelsesekvensen och hur exakt bränsleförbrukningen kopplas till mekaniskt arbete.
Att simulera ett molekylärt dragkamp
Författarna byggde en probabilistisk datormodell som behandlar motorn som ett system som hoppar mellan många möjliga former medan ATP-molekyler och deras nedbrytningsprodukter binder och släpper. De definierade 30 huvudkonformationer av ringen där en, två eller tre motorsubenheter tappar greppet om proteinet, plus ett särskilt tätt stängt tillstånd där alla sex håller kvar. Med en standardalgoritm för att simulera slumpmässiga kemiska händelser följde de hundratusentals steg där ATP-bindning, ATP-nedbrytning och motorns formförändringar inträffar. Från dessa körningar kunde de förutsäga hur snabbt ett protein dras igenom under olika villkor, såsom varierande mängder ATP, dess förbrukade form ADP, och en icke‑brytbar ATP-mimic som ofta används i experiment.
När för mycket bränsle bromsar motorn
Simuleringarna återskapade flera förbryllande experimentella fynd. När ATP-nivåerna stiger från låga värden drar motorn proteiner snabbare, eftersom bränslebindningen är det långsammaste steget. Men efter ungefär 1 millimolar ATP når hastigheten en topp och faller sedan: ringen tillbringar mer tid i en fastlåst, icke‑translokaterande konformation där alla sex subenheter är ockuperade av ATP men proteinet inte förflyttas. Tillsats av ADP eller den icke‑brytbara ATP-analogen saktar ständigt ner motorn, eftersom dessa molekyler konkurrerar med ATP om bindningsfickorna men inte kan fullfölja hela kraftslaget. Modellen förutsäger också hur motorn beter sig när den möter mycket tätt veckade regioner i ett protein som fungerar som trafikstopp. I de fallen tillbringar motorn mer tid med att kämpa mot motstånd, och den övergripande nedbrytningshastigheten minskar, vilket stämmer överens med mätningar på artificiellt stabiliserade proteindomäner.
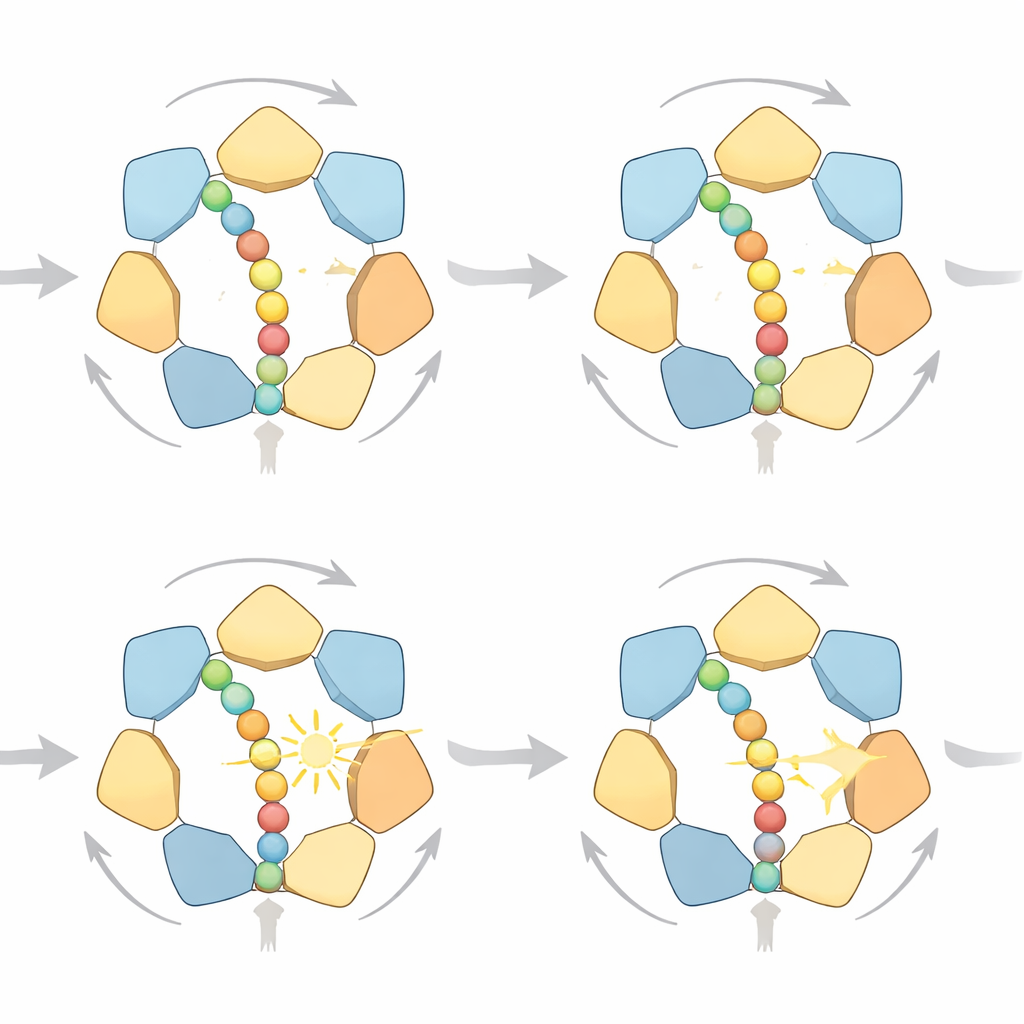
Många sätt att ta ett steg
Genom att granska de simulerade banorna i detalj fann forskarna att ringen inte följer en enda stel cykel. Istället finns flera högprobabilitetsvägar som alla respekterar samma riktade ”hand‑över‑hand”-regel: subenheter nära ringens utgång släpper proteinet efter ATP‑nedbrytning, rör sig till toppen av en spiraltrappa av subenheter och greppar kedjan längre upp. Ibland avancerar proteinet med ett litet steg, ibland med två, beroende på hur många subenheter som släpper samtidigt. Vid rikligt bränsle dominerar ettstegsrörelser eftersom de slösar mindre arbete mot motverkande krafter; när bränslet är knappt förutspår modellen fler frekventa tvåstegshopp. Simuleringarna kopplar också mekanisk belastning till motorns kemiska tillstånd: när motståndet ökar och proteinet stannar tenderar ADP att ackumuleras i fler av de sex bindningsfickorna — precis det som högupplösta strukturella studier observerar.
Energianvändning och gemensamma designregler
Modellen gör det möjligt för författarna att kartlägga hur motorns energi ökar när ATP bryts ner och faller när den energin omvandlas till rörelse. De beräknar en verkningsgradskurva som visar att motorn fungerar bäst vid en mellanliggande motkraft: för lite motstånd och den förbrukar ATP slösaktigt; för mycket och den stannar nästan. När teamet jämförde sina förutsägelser med data från besläktade proteinnedbrytande maskiner i bakterier och jäst fann de mycket liknande trender i hur en icke‑brytbar ATP-mimic saktar ner dessa motorer. Det tyder på att många medlemmar av samma familj av ringformade enzymer sannolikt delar en gemensam, konservativ mekanism för att dra i proteiner.
Varför detta är viktigt för hälsa och sjukdom
Genom att omvandla spridda strukturella ögonblicksbilder och biokemiska mätningar till ett enhetligt, testbart ramverk visar detta arbete i kvantitativ detalj hur en liten molekylär motor omsätter kemiskt bränsle till kraft för att återvinna cellens proteiner. Modellen förklarar inte bara ett brett spektrum av befintliga experiment utan ger även förutsägelser om hur förändringar i bränslenivåer, mekanisk belastning eller motormutationer kan påverka proteinnedbrytningen. Eftersom liknande maskiner är verksamma i alla livsformer och är centrala i tillstånd från neurodegeneration till cancer, kan förståelsen av deras inre funktioner på denna nivå i slutändan vägleda designen av läkemedel som finjusterar, förstärker eller selektivt blockerar dessa mikroskopiska kvarnar.
Citering: Wu, D., Ouyang, Q., Wang, H. et al. Nonequilibrium chemomechanical transduction of ATP-driven protein unfolding in the 26S proteasome. npj Biol. Phys. Mech. 3, 4 (2026). https://doi.org/10.1038/s44341-026-00034-w
Nyckelord: proteasom, AAA+ ATPas-motor, proteinnedbrytning, molekylära maskiner, kemomekanisk koppling