Clear Sky Science · sv
Ultrakänslig icke‑enzymatisk proteinidentifiering med proximetsimmunanalys och fotonisk resonatorabsorptionsmikroskopi
Varför det spelar roll att hitta mycket små spår av proteiner
Läkare och forskare förlitar sig i allt större utsträckning på proteiner i blodet för att varna för cancer, hjärtsjukdom, infektioner eller skadlig inflammation långt innan symtomen blir allvarliga. Men många av dessa molekylära varningssignaler förekommer i ytterst låga nivåer som dagens standardlabbar ofta har svårt att upptäcka snabbt eller billigt. Denna studie presenterar en ny testmetod, kallad PINATA, som kan upptäcka extremt små mängder av ett protein kopplat till inflammation samtidigt som den använder enkel utrustning och steg i rumstemperatur, vilket öppnar för mer tillgänglig och känslig diagnostik.
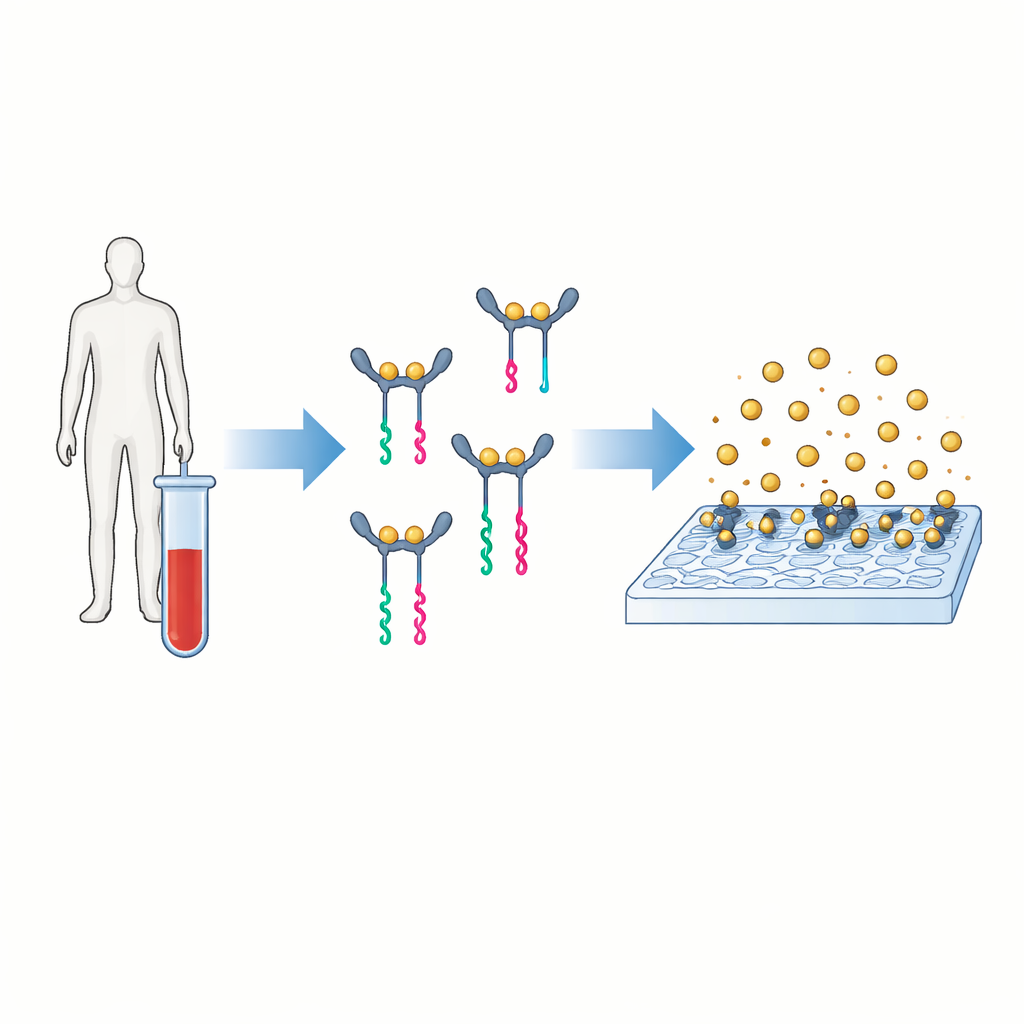
Ett nytt sätt att översätta proteiner till avläsbara signaler
Huvudidén bakom PINATA är att översätta närvaron av ett protein till en kort DNA‑bit som är lätt att amplifiera och räkna. Författarna fokuserar på interleukin‑6, ett signalprotein i blodet som ökar vid allt från infektion till cancer. I konventionella tester binder två antikroppar till proteinet och bär på ett enzym som genererar en färgad eller fluorescerande signal. PINATA behåller grundidén att två antikroppar känner igen samma protein, men istället för enzymer fästs korta DNA‑strängar vid varje antikropp. När båda antikropparna binder samma protein och förs nära varandra samarbetar deras DNA‑delar för att frigöra en separat DNA‑bit kallad reporter. Varje proteinklon kan därigenom utlösa frisättningen av många identiska DNA‑reportrar.
Använda DNA:s ”trafikregler” istället för enzymer
I hjärtat av metoden finns noggrant designade DNA‑kretsar som beter sig som molekylära trafiksystem och styr när strängar kan binda, släppa eller byta partner. Dessa kretsar är konstruerade så att reporter‑DNA:t förblir låst och ingen signal genereras om inte ett protein för ihop de antikroppsbundna DNA‑delarna. När proteinet är närvarande frigör dess brofunktion reportern. Denna frigjorda reporter deltar sedan i en sekundär förstärkningsprocess på en förberedd yta. Där engagerar den sig upprepade gånger i strängbytesreaktioner som gör att en enda reporter kan rekrytera många guldbeläggna nanopartiklar till ytan och skapa en stark digital signal utan att använda enzymer eller temperaturcykling.
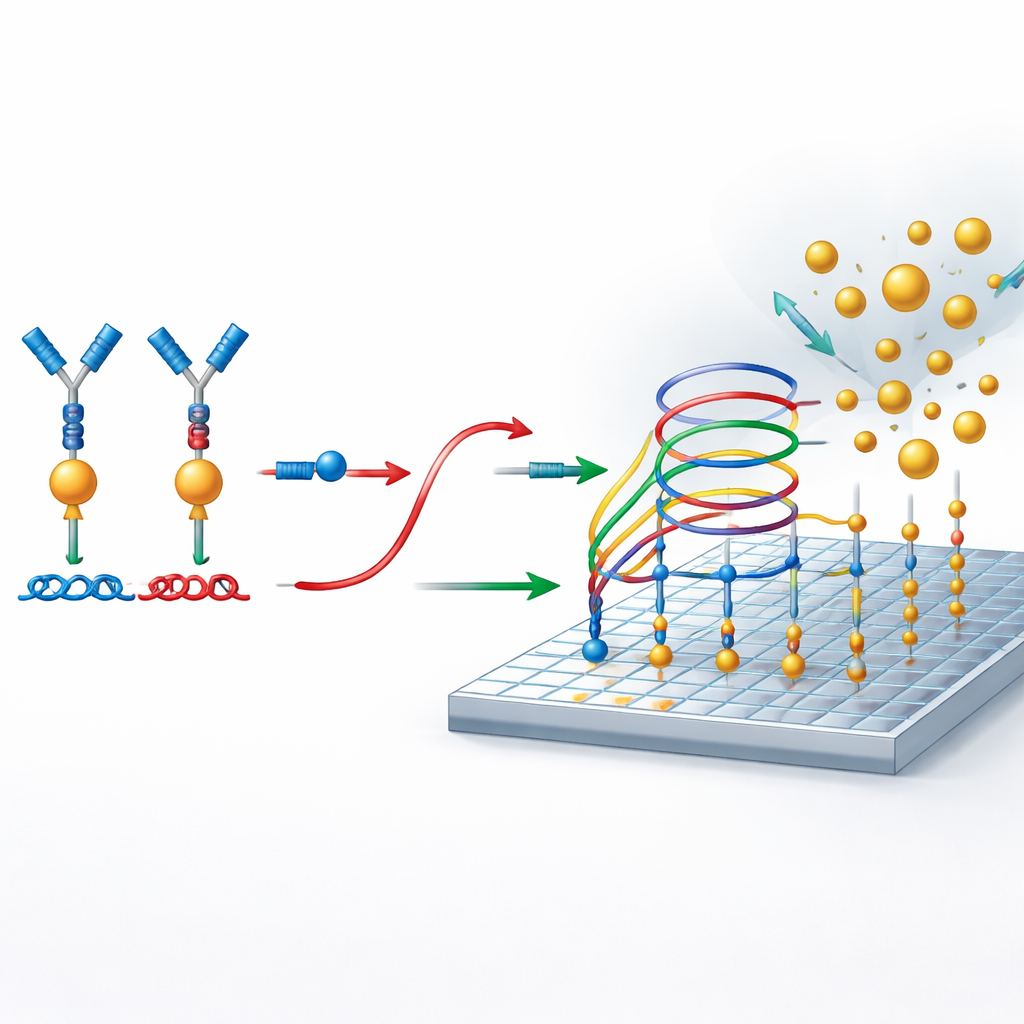
Räkna enstaka nanopartiklar som ja‑/nej‑händelser
För att läsa av resultatet använder forskarna fotonisk resonatorabsorptionsmikroskopi, PRAM. Detektionsytan är ett speciellt mönstrat material som starkt reflekterar ljus vid en viss våglängd. När guldbelagda nanopartiklar landar på denna yta absorberar de det ljuset och framträder som mörka prickar i mikroskopbilden. Eftersom systemet är designat så att nanopartiklar bara binder när reporter‑DNA finns närvarande, representerar varje mörk prick en lyckad detektionshändelse som kan kopplas tillbaka till en proteinklon. En enkel, lågkostnads optisk uppställning och bildbehandlingsprogramvara används sedan för att räkna dessa prickar över ytan, vilket omvandlar antalet nanopartiklar till en exakt mätning av proteinkoncentrationen.
Hur känsligt och selektivt är testet?
Med denna metod visar teamet att de kan detektera interleukin‑6 vid nivåer ner till 37 femtogram per milliliter—ungefär några tiotals molekyler i en droppe—över ett dynamiskt område som sträcker sig över sex storleksordningar. Analysen fungerar i ett enkelt tvåstegsprotokoll på 90 minuter som utförs helt i rumstemperatur. Författarna visar också att testet förblir korrekt även när interleukin‑6 blandas i komplexa prover som mänskligt serum och plasma, vilka annars ofta stör känsliga mätningar. De bekräftar vidare att antikropparna mot interleukin‑6 inte reagerar på andra, närbesläktade proteiner, vilket understryker analysens selektivitet.
Vad detta kan innebära för framtidens diagnostik
För en icke‑specialist är huvudpoängen att PINATA erbjuder ett sätt att upptäcka sjukdomsrelaterade proteiner på extremt låga nivåer med ett kompakt optiskt instrument i stället för skrymmande, kostsam labbutrustning. Genom att kombinera smart DNA‑logik med digital räkning av nanopartiklar undviker metoden ömtåliga enzymer och uppvärmningssteg, men når ändå eller överträffar känsligheten hos många avancerade proteinassays. Med vidare utveckling och anpassning till andra målmolekyler skulle denna strategi kunna möjliggöra tidigare diagnoser, tätare övervakning och punkt‑av‑vårdstester för ett brett spektrum av tillstånd där små förändringar i proteinnivåer har stor klinisk betydelse.
Citering: Shepherd, S., Bhaskar, S., Xu, H. et al. Ultrasensitive non-enzymatic protein detection using proximity immunoassay with photonic resonator absorption microscopy. npj Biosensing 3, 21 (2026). https://doi.org/10.1038/s44328-026-00090-1
Nyckelord: detektion av proteinbiomarkörer, ultrakänslig diagnostik, DNA‑strängförskjutning, interleukin‑6‑analys, digital biosensorik