Clear Sky Science · sv
Plasmonförstärkt bioanalys för amplifikationsfri detektion och kvantifiering av SARS-CoV-2 RNA
Varför snabbare, enklare virustester spelar roll
COVID-19-pandemin visade hur beroende vi är av laboratoriebaserade tester som är långsamma, dyra och svåra att skala upp när miljontals människor snabbt behöver svar. Det arbete som beskrivs här presenterar en ny typ av labbtest som kan upptäcka och räkna mycket små mängder koronavirusets genetiska material utan det vanligt förekommande amplifikationssteget som används i PCR. Denna metod syftar till att föra sjukhusnivåns noggrannhet närmare enkla, lågutkostningstester som kan användas mer brett vid framtida utbrott.
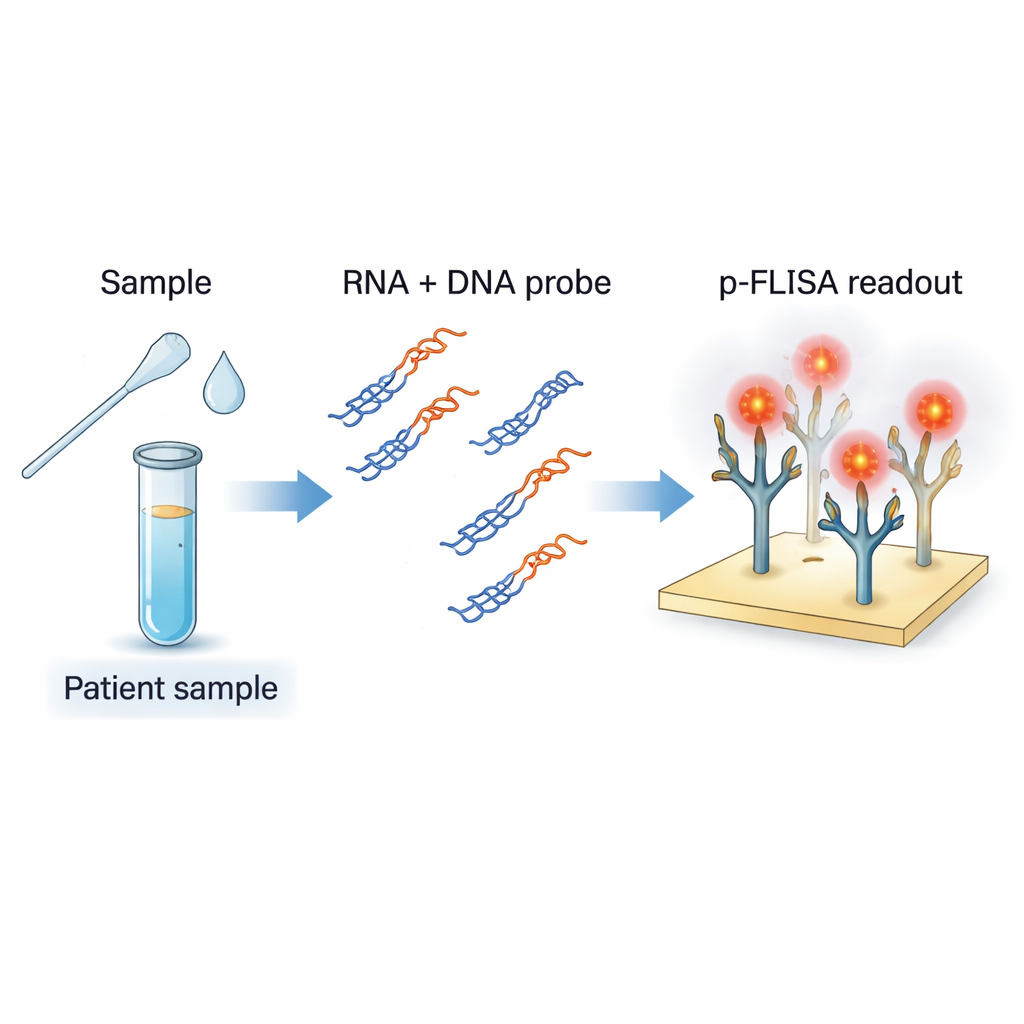
Ett nytt sätt att se virala genetiska spår
Standarddiagnostik för COVID-19 använder RT-PCR, som gör många kopior av fragment av virusets RNA så att de kan upptäckas. Även om PCR är mycket känsligt kräver det komplex utrustning, utbildad personal och tid, och ger oftast ett ”ja eller nej”-svar snarare än en exakt virusmängd. Författarna försökte bygga en analys som fungerar mer som en kraftigt uppgraderad ELISA: ett enkelt plattformat, men inställt på att detektera viral RNA direkt och kvantifiera hur mycket som finns. Deras metod riktar in sig på SARS-CoV-2 RNA i prover som nasala bomullspinnar och saliv, men är utformad för att lätt kunna anpassas till andra RNA-virus.
Att göra RNA till ett fångbart mål
Teamet använder korta DNA-bitar som är utformade för att matcha specifika regioner av SARS-CoV-2-genomet. När dessa blandas med RNA som extraherats från ett patientprov och försiktigt upphettas och kyls, parar sig DNA-proberna med matchande viralt RNA och bildar DNA–RNA-hybrider, som en liten dragkedja med en RNA-sträng och en DNA-sträng. Ett speciellt antikroppstyp kallad S9.6 fungerar som fångare: den känner igen och binder starkt till dessa hybrider, men inte till vanlig enkel- eller dubbelsträngad DNA eller till orelaterat RNA. Genom att belägga botten av en platta med S9.6 fångar analysen selektivt endast de hybrider som innehåller virusets genetiska sekvenser av intresse och filtrerar bort resten av provets genetiska störningar.
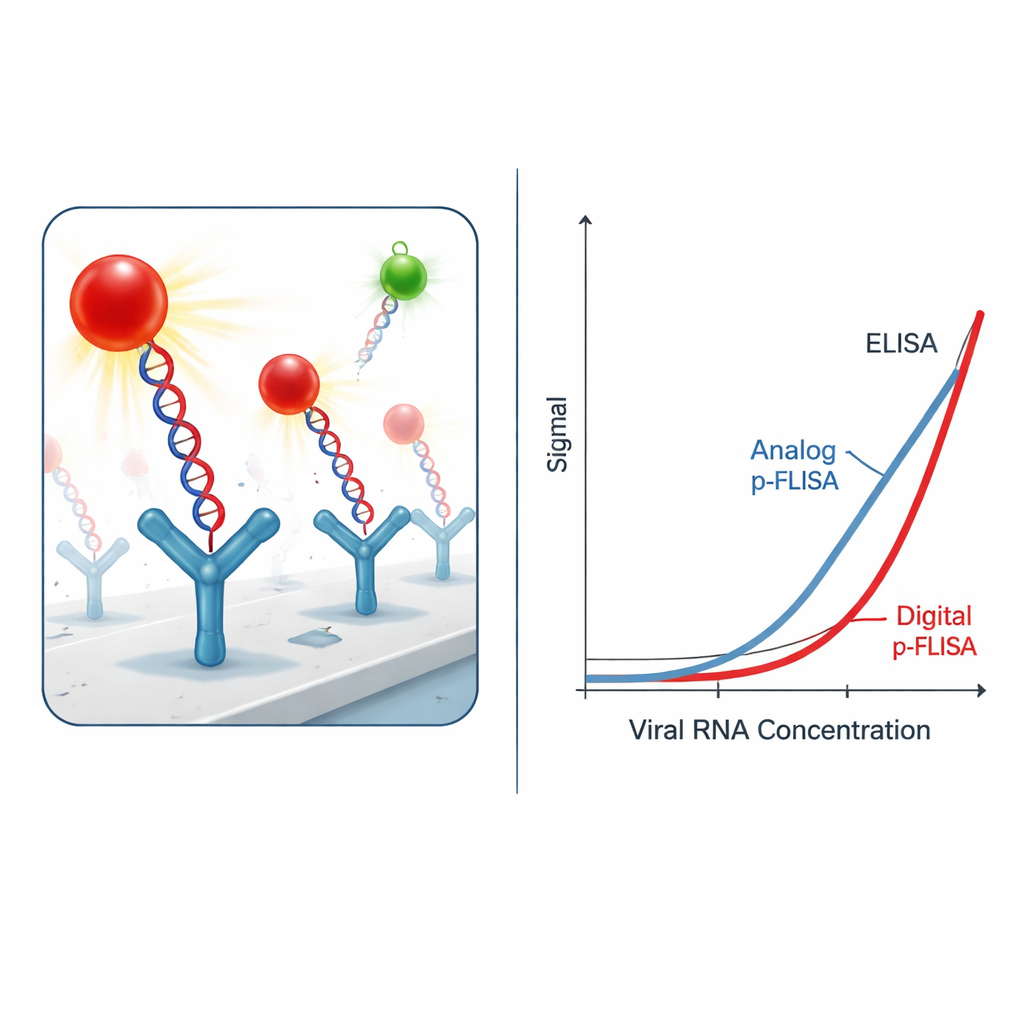
Göra signalen ultrastark
Att enbart fånga de virala hybriderna räcker inte; utmaningen är att se dem över bakgrundsbruset. Istället för konventionella fluorescerande färgämnen använder forskarna "plasmonic-fluor" nanomarkörer—konstruerade nanopartiklar som fungerar som små antenner för ljus. Varje markör kombinerar en metallnanostav med flera fluorescerande molekyler och en beläggning som gör att den kan fästa vid biotin-taggar på DNA eller antikroppar. Dessa plasmoniska markörer sänder ut ljus mer än tusen gånger starkare än standardfärgämnen under samma förhållanden. I praktiken innebär det att avsevärt färre virala hybrider behövs för att ge ett detekterbart sken, vilket dramatiskt förbättrar testets känslighet och sänker den lägsta virus-RNA-koncentration som kan mätas.
Från analogt sken till digital räkning
I sin enklaste "analoga" form mäter analysen den totala ljusstyrkan från varje brunn i plattan, ungefär som ett klassiskt fluorescensprov. Även i detta läge förbättrar det plasmonförstärkta systemet detektionsgränsen och den lägsta pålitligt kvantifierbara nivån av SARS-CoV-2 RNA med en till tre storleksordningar jämfört med en traditionell ELISA som använder enzymer eller standardfluoroforer. Författarna går sedan längre genom att byta till ett "digitalt" format: istället för att medelvärdesbilda ljuset över hela brunnen avbildar de ytan med ett fluorescensmikroskop och räknar individuella ljusstarka nanomarkörer med specialanpassad bildanalysprogramvara. Denna singelpartikelräkning ger ytterligare en tio- till trettiofaldig känslighetsvinst, vilket totalt leder till ungefär 2 300 gånger bättre detektionsgräns och 460 gånger bättre kvantifieringsgräns än ELISA.
Att prova testet på riktiga prover
För att se om metoden håller utanför kontrollerade laboratorieblandningar testade forskarna RNA extraherat från nasala provpinnar och saliv från patienter med COVID-19, inklusive infektioner från olika varianter såsom alfa/beta och delta, samt prover från personer med andra luftvägsvirus. Deras plasmonförstärkta analys detekterade SARS-CoV-2 RNA i alla PCR-positiva prover, med ingen signal över bakgrund i PCR-negativa prover eller de som innehöll andra virus, vilket visar utmärkt klinisk känslighet och specificitet jämförbar med RT-PCR. Dessutom visade de uppmätta RNA-koncentrationerna ett omvänt förhållande till PCR:s cykeltröskelvärden: prover som behövde färre PCR-cykler (vilket indikerar högre virusmängd) hade högre RNA-nivåer enligt den nya analysen, i överensstämmelse med biologiska förväntningar och vilket tyder på att den kan ge meningsfull kvantitativ information om virusbörda.
Vad detta kan innebära för framtida utbrott
För icke-specialister är huvudbudskapet att denna analys erbjuder ett sätt att läsa av hur mycket virus som finns utan det extra kopieringssteget som gör PCR långsamt och utrustningskrävande. Genom att kombinera en selektiv antikropp för RNA–DNA-hybrider med ultrastarka nanoskaliga ljuskällor och digital räkning närmar sig metoden PCR-liknande prestanda samtidigt som den behåller ett enkelt plattformat arbetsflöde. Med ytterligare validering och ingenjörsarbete skulle sådana plasmonförstärkta analyser kunna anpassas till många RNA-mål och eventuellt omformas till snabba tester vid vårdplatsen, vilket hjälper kliniker att inte bara diagnostisera infektioner utan också bedöma sjukdomsstadium och smittsamhet utifrån ett absolut mått på virus-RNA.
Citering: Liu, L., Seth, A., Liu, Y. et al. Plasmon-enhanced bioassay for amplification-free detection and quantification of SARS-CoV-2 RNA. npj Biosensing 3, 13 (2026). https://doi.org/10.1038/s44328-026-00078-x
Nyckelord: Detektion av SARS-CoV-2 RNA, plasmoniska nanomarkörer, digital immunoanalys, diagnostik utan amplifikation, kvantifiering av virusmängd