Clear Sky Science · sv
En mikrorgan-baserad mikrofluidisk biosensor för kontinuerlig övervakning av glukosnivåer in vivo
Varför detta betyder något för personer med diabetes
För personer med typ 1-diabetes kräver dagens ”artificiella bukspottkörtelsystem” fortfarande ständig uppmärksamhet—anmälning av måltider, hantering av larm och oro för lågt blodsocker nattetid. Denna studie undersöker en radikalt annorlunda typ av glukossensor som inte förlitar sig på ett enskilt enzym eller en datorformel, utan istället lånar en liten levande del av kroppens egna sockerreglerande maskineri: kluster av pankreasceller kallade öar. Genom att låta dessa mini-organ göra det evolutionen optimerat dem för, siktar forskarna på att bygga smartare, säkrare glukosmonitorer som en dag skulle kunna fungera mer självständigt i bakgrunden.
Ett litet organ som en levande sensor
De flesta nuvarande biosensorer upptäcker kemikalier med renade molekyler eller cellinjer. De reagerar på ett specifikt ämne och skickar sedan den råa signalen till programvara som försöker tolka den. Författarna menar att detta förbigår en kraftfull inbyggd ”dator”: mikro-organ, som pankreasöar, som naturligt känner av många signaler samtidigt och omvandlar dem till ett samordnat svar. Varje ö innehåller flera hormonproducerande celltyper som ständigt kommunicerar med varandra. Tillsammans håller de blodsockret inom ett smalt, säkert intervall och reagerar inte bara på glukos utan även på aminosyror, tarm- och stresshormoner samt kroppens nyliga historia av toppar och dalar. Denna inbyggda komplexitet, föreslår de, skulle kunna utnyttjas för att ge rikare och mer pålitlig information än en enkel glukosoxidas-sensor.
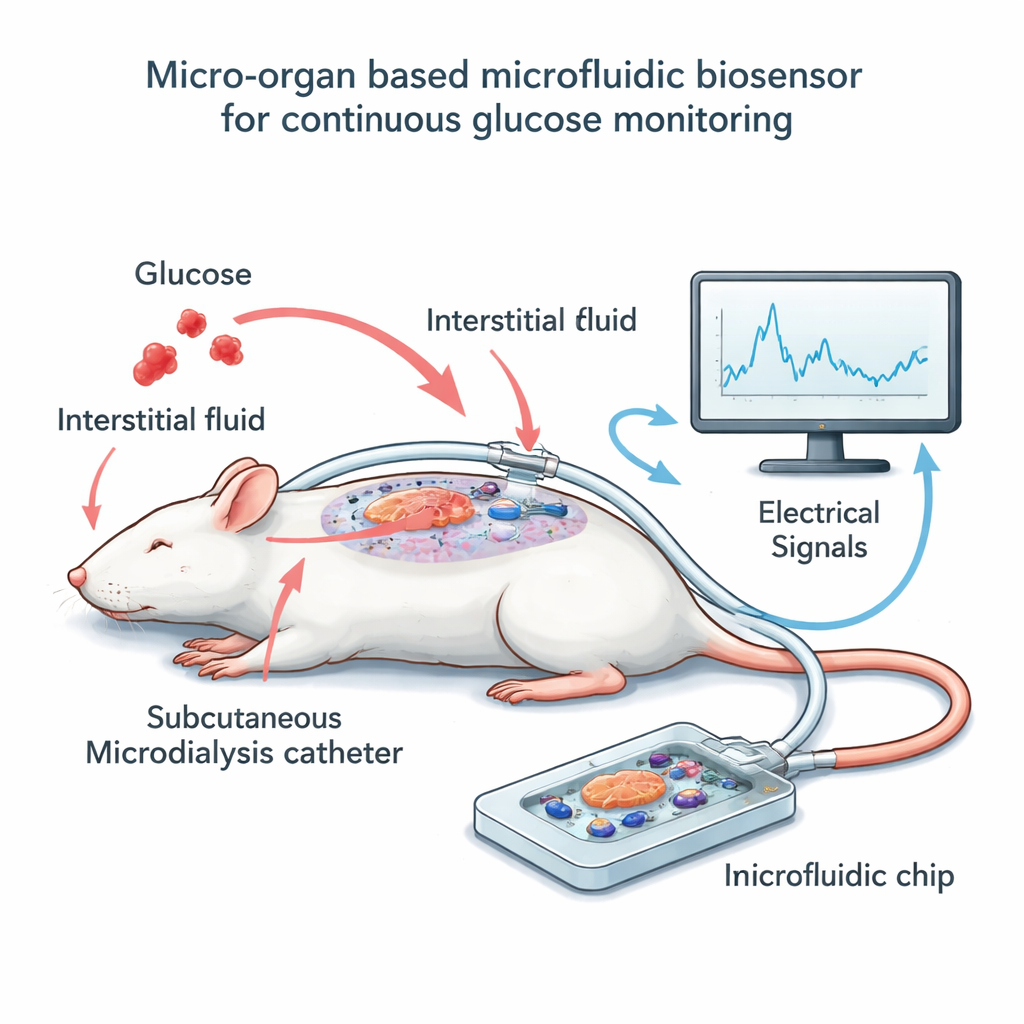
Bygga chip- och katetersystemet
För att testa idén byggde teamet en liten enhet utanför kroppen som rymmer några dussin musöar ovanpå ett galler av mikroskopiska elektroder. Istället för att bada dessa celler direkt i blod använde de en teknik kallad mikrodialys: en tunn flexibel kateter ligger precis under huden på bedövade råttor och samlar långsamt upp den omgivande vätskan i vävnaden, som följer blodsockret nära men med en kort fördröjning. Ett lågt, konstant flöde för denna vätska genom en smal kanal över öarna på chippet. När glukosnivåerna i dialysatet stiger och faller ändrar öarna sin elektriska aktivitet, vilket elektroderna fångar som långsamma, vågliknande signaler. Parallellt mätte forskarna med jämna mellanrum glukos i råttornas blod och i dialysatet, vilket gjorde det möjligt att ställa den elektriska avläsningen mot faktiska sockernivåer över tid.
Hur den levande sensorn svarade på förändrat socker
Först testade forskarna om öarna på elektroderna kunde reagera på verkliga blodkomponenter snarare än enkla labsystem. De exponerade dem för mänskligt och råttserum med olika glukosnivåer och såg tydliga, graderade förändringar i både frekvens och storlek på deras elektriska vågor. Responsen var tillräckligt stark för att skilja små steg i sockerkoncentration över det intervall som är relevant för diabetes. De gick sedan vidare till råttexperiment, gav en glukosinjektion för att höja blodsockret och senare injicerade insulin för att sänka det. Efter att ha kompenserat för tiden det tar för glukos att röra sig från blod till vätska i vävnaden och genom slangen fann de att frekvensen i öarnas långsamma elektriska signaler steg och föll nästan i takt med blodsockret. Statistiska analyser över flera djur visade en anmärkningsvärt tajt, upprepat förhållande mellan signalfrekvens och glukosnivå, medan signalamplitud, även om den var informativ, var något mer variabel.
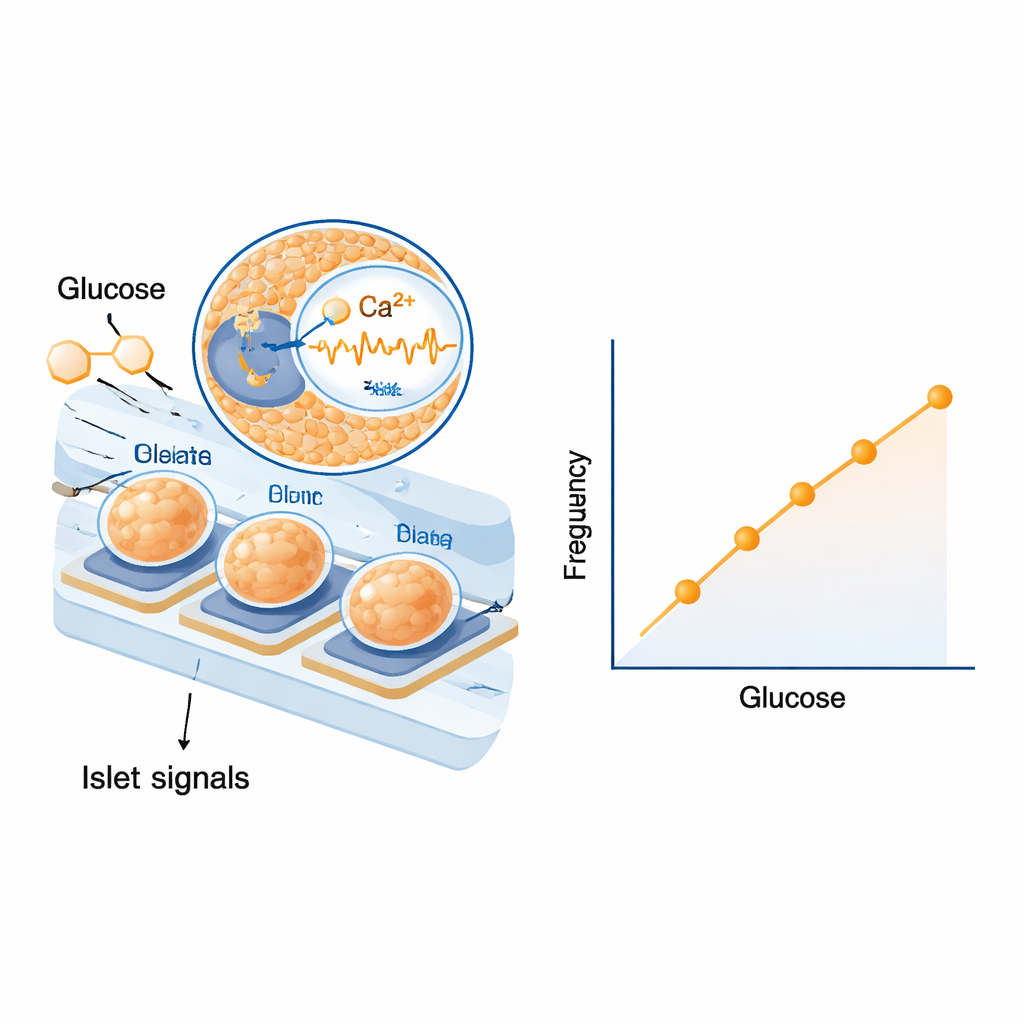
Inbyggda säkerhetsfunktioner från biologin
En viktig fördel med att använda hela öar snarare än en enda molekyl är att deras beteende redan inkluderar säkerhetsmekanismer formade av evolutionen. Tidigare arbete, och antydningar i denna studie, visar att öarna reagerar starkare när glukos sjunker än när det stiger—en form av ”hysteresis” som hjälper till att skydda mot farlig hypoglykemi. De elektriska mönstren formas också av närliggande celltyper som förstärker eller dämpar insulinfrisättning beroende på kroppens behov. Eftersom chippet helt enkelt lyssnar på dessa integrerade signaler utan att tillsätta färgämnen eller genetiska modifieringar kan det spela in i flera dagar utan att skada cellerna. Författarna noterar tekniska utmaningar framåt, såsom att undvika luftbubblor, säkerställa långsiktig mikrodialysfunktion och avgöra vilken typ av mänskliga eller stamcellsderiverade öar som slutligen bör användas. Ändå tyder datorsimuleringar med en etablerad diabetesmodell på att en sådan öbaserad sensor skulle kunna matcha eller till och med överträffa dagens glukosmonitorer under svåra förhållanden.
Vad detta kan betyda för framtidens diabetesvård
Detta arbete visar att ett fåtal pankreasmikro-organ, hållna vid liv på ett litet chipp och kopplade till kroppen via en tunn kateter, kan följa blodsockret kontinuerligt i levande djur genom deras naturliga elektriska sorl. För en icke-specialist är huvudbudskapet att istället för att be en enkel kemisk sensor att mäta glukos och sedan tvinga en dator att gissa vad det betyder för kroppen, lyssnar detta tillvägagångssätt direkt på samma typ av levande vävnad som normalt bestämmer hur mycket insulin som ska frisättas. Om det förfinas och görs praktiskt användbart för människor skulle sådana levande biosensorer kunna bli kärnan i verkligt autonoma artificiella bukspottkörtelsystem—enheter som tyst förutser kroppens behov och minskar den dagliga bördan av diabetesvård.
Citering: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
Nyckelord: kontinuerlig glukosövervakning, artificiell bukspottkörtel, pancreatiska öar, mikrofluidisk biosensor, typ 1-diabetes