Clear Sky Science · sv
En narrativ översikt över apolipoproteiners påverkan på aterosklerotiska kranskärlsplack
Varför fetterna i ditt blod fortfarande spelar roll
Hjärtinfarkter och stroke börjar ofta med tysta förändringar i blodkärlen som försörjer hjärtat. Denna artikel ser bortom det välbekanta begreppet "bra" och "dåligt" kolesterol till de proteinskalen som transporterar fetter i blodomloppet, så kallade apolipoproteiner. Genom att följa hur fyra av dessa proteiner formar tillväxten, sammansättningen och behandlingen av kranskärlsplack – de fettansamlingar som täpper till hjärtats artärer – visar författarna varför vissa personer fortsätter att ha hög risk för hjärtsjukdom även när deras kolesterolvärden ser idealiska ut.
De dolda aktörerna på kolesterolet
De flesta av oss hör talas om LDL- och HDL-kolesterol, men vart och ett av dessa partiklar är omslutet av en eller flera apolipoproteiner som hjälper till att bestämma vart partikeln tar vägen och hur farlig den är. Denna översikt fokuserar på fyra viktiga typer: apolipoprotein(a), apolipoprotein A‑I, apolipoprotein B och apolipoprotein C‑III. Tillsammans styr de hur fettpartiklar byggs upp, hur länge de cirkulerar och hur lätt de tar sig in i och skadar kärlväggen. Moderna avbildningsverktyg – ultraljud inuti kärlet, högupplösta ljusbilder och CT-angiografi – gör det nu möjligt för läkare att se inte bara hur trångt ett kärl är, utan om dess plack är mjuka och sprickbenägna eller täta och förkalkade. 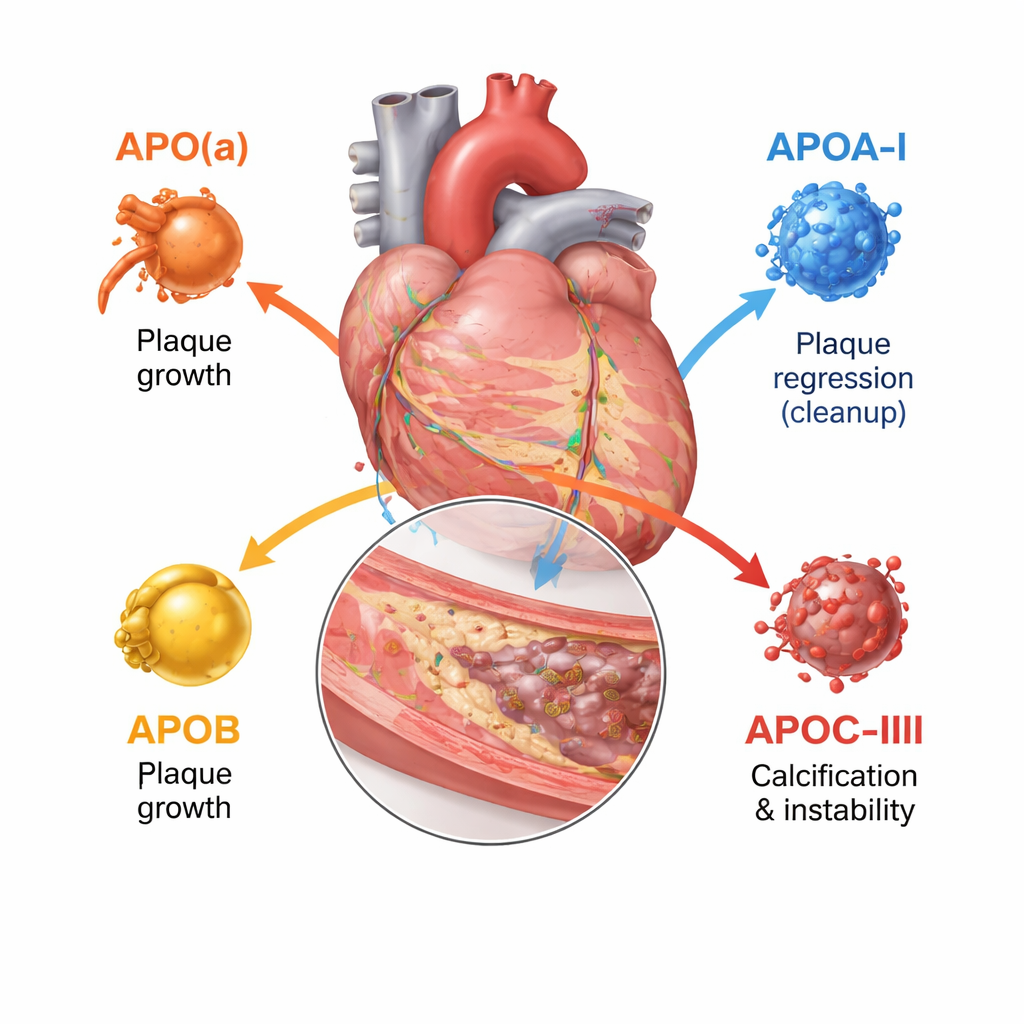
Hur fyra proteiner formar farliga plack
Apolipoprotein B sitter på varje LDL-liknande partikel och räknar i praktiken hur många aterogena – artärtilltäppande – partiklar som finns i blodet. Ju fler ApoB-bärande partiklar en person har och ju längre de cirkulerar, desto större blir den totala plackbördan i kranskärlen. Studier som använder avbildning inne i hjärtats artärer visar att högre ApoB-nivåer går hand i hand med större plack, längre lesioner, fler mjuka, nekrotiska kärnor och färre stabiliserande kalciumdepositioner. Däremot hjälper apolipoprotein A‑I, huvudproteinet på HDL, till att avlägsna kolesterol från plackceller och transportera det tillbaka till levern. Högre funktionell ApoA‑I-aktivitet och en gynnsam balans mellan HDL-kolesterol och ApoA‑I är kopplade till långsammare placktillväxt och mer fibrös, stabil vävnad, även om enbart en höjning av HDL-kolesterolet i blodet inte har resulterat i färre kliniska händelser.
Ett särskilt riskprotein och en främjare av förhårdnande
Apolipoprotein(a) bildar en partikel kallad lipoprotein(a), eller Lp(a), när det binder till en LDL-liknande kärna. Lp(a) bestäms nästan uteslutande av genetik och påverkas vanligtvis inte av kost. Avbildningsstudier på tusentals patienter visar att personer med högt Lp(a) har mer totalt plack, fler områden med låg densitet och lipidrika regioner samt fler fokala "högrisk"-plack som är benägna att brista, även när LDL-kolesterolet redan behandlas aggressivt. Översikten slutsatsen är att Lp(a) representerar en betydande "kvarstående risk" som standardbehandlingar för att sänka kolesterol inte fullt ut adresserar. Apolipoprotein C‑III, som mest finns på triglyceridrika partiklar, saktar ner deras utsöndring och väcker inflammation. Personer med högre ApoC‑III har mer koronarkalcium och mer komplexa, förkalkade noduler i placken, kännetecken kopplade till avancerad sjukdom och stelare artärer.
Nya läkemedel som riktar sig mot rätt mål
Där dessa proteiner spårar risk mer precist än kolesterol ensam håller de på att bli direkta läkemedelsmål. För Lp(a) kan flera injicerbara genetiska läkemedel – antisense- och små-interfererande RNA-läkemedel – sänka nivåerna med 80–95 % i tidiga studier, och en tablett som blockerar partikelns sammansättning visar också stora reduktioner. För ApoC‑III kan nyligen godkända terapier kraftigt sänka triglycerider och ApoC‑III själv, och tidiga data tyder på att de kan minska risken för pankreatit och potentiellt omforma plackförkalkning. 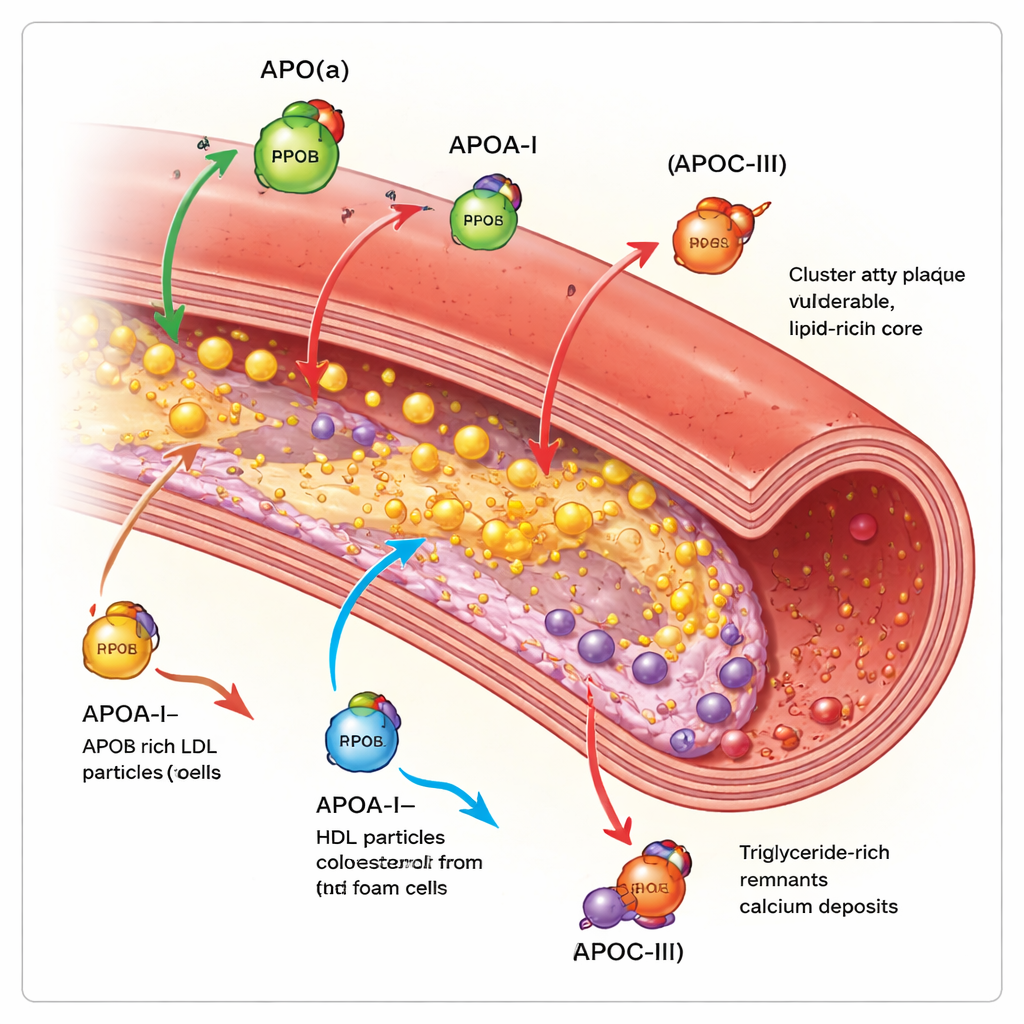
Vad detta betyder för att skydda ditt hjärta
Förenklat hävdar denna översikt att vem som drabbas av en hjärtinfarkt inte avgörs enbart av kolesterolnivåer, utan av blandningen och beteendet hos de proteinöverdragna partiklar som bär kolesterolet. ApoB speglar hur många "dåliga" partiklar som bombarderar kärlväggen, ApoA‑I speglar systemet som fraktar bort kolesterol, Lp(a) tillför en extra genetiskt bestämd risk och ApoC‑III favoriserar förhårdnade, inflammerade plack. Framväxande läkemedel som specifikt sänker Lp(a) och ApoC‑III, samt mer precis användning av ApoB och ApoA‑I i rutintester, skulle kunna göra det möjligt för läkare att skräddarsy prevention efter varje patients individuella plackbiologi och fånga upp dold risk som standardlipidpaneler missar.
Citering: Fukase, T., Dohi, T. A narrative review of impacts of apolipoproteins on atherosclerotic coronary plaques. npj Cardiovasc Health 3, 4 (2026). https://doi.org/10.1038/s44325-026-00104-x
Nyckelord: lipoprotein(a), apolipoprotein B, apolipoprotein A-I, apolipoprotein C-III, koronar plackavbildning