Clear Sky Science · sv
En enkelstegs radiomärkningsstrategi för PET, SPECT och terapeutiska radionuklider med nanopartiklar som en universell kelator
Varför små radioaktiva partiklar är viktiga
Modern cancerbehandling förlitar sig i allt högre grad på att upptäcka och behandla tumörer med radioaktiva läkemedel som gör dem synliga i skanningar och i vissa fall förstör dem inifrån. Att ta fram varje nytt radioaktivt läkemedel är dock tidskrävande och klurigt, eftersom de flesta konstruktioner måste skräddarsys för en viss radioaktiv metall. Denna studie utforskar en helt annan strategi: att använda en enda typ av järnbaserad nanopartikel som ett ”universellt uttag” som kan bära många olika medicinska isotoper för avbildning och terapi, vilket potentiellt kan snabba upp hur sådana läkemedel skapas och finjusteras.
Från många nycklar till ett lås
Dagens radioaktiva läkemedel bygger vanligtvis på kemiska klor i form av kelatorer som greppar metallatomer och fäster dem vid antikroppar eller andra målriktade molekyler. Varje radioaktiv metall tenderar att kräva sin egen kelator och sitt eget recept—förhållanden som temperatur, surhetsgrad och reaktionstid skiljer sig åt. För vissa medicinskt viktiga metaller, särskilt de som används för kraftfulla alfapartikelterapier, finns ännu ingen ideal kelator. Författarna menar att detta metall‑för‑metall‑tänkande har blivit en flaskhals: listan över användbara isotoper växer, men kemin för att hantera dem på ett säkert sätt kan inte hålla jämna steg.
Nanopartiklar som ett universellt uttag
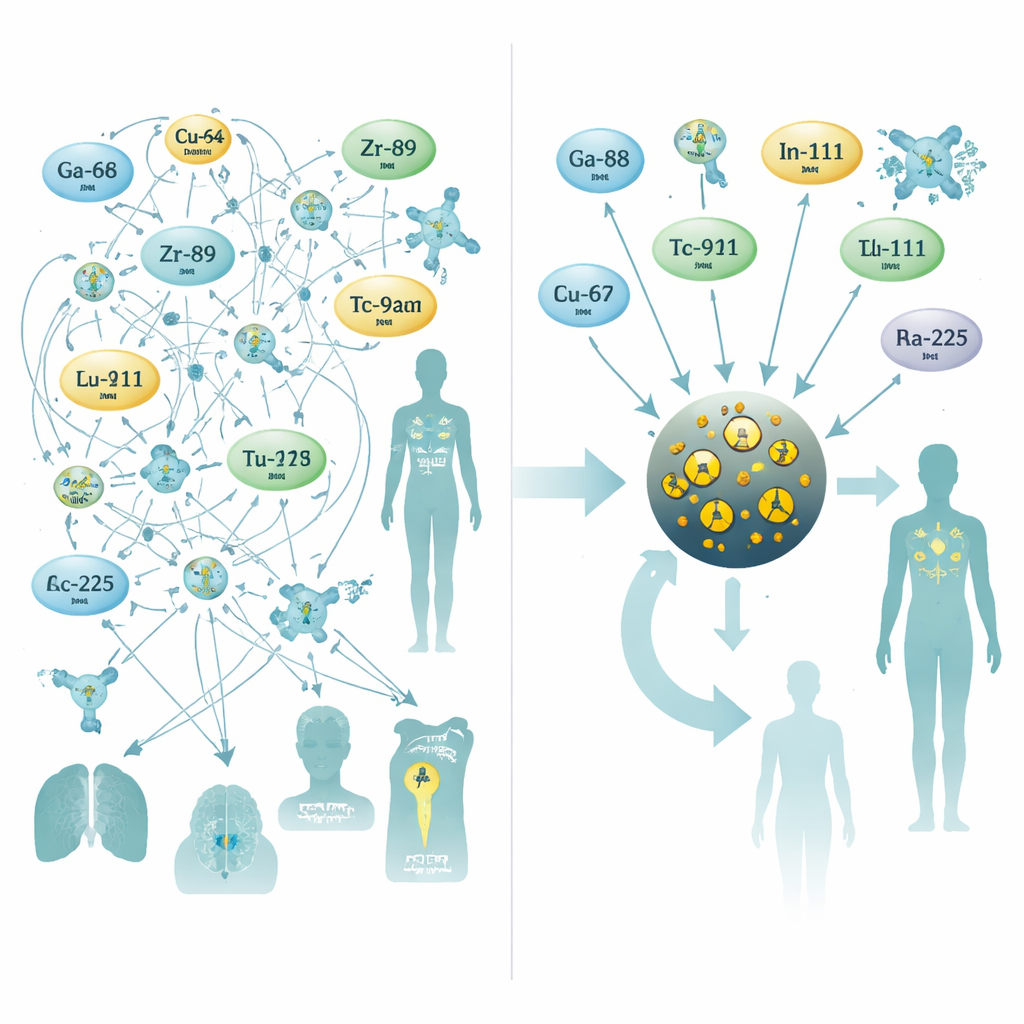
För att tackla detta använde forskarna mycket små järnoxidnanopartiklar, ett material som redan studerats för MR‑kontrast. De designade partiklar med en järnoxidkärna på omkring tre nanometer, omsluten av ett citratlager som håller dem stabila i blodbanan. Under ett enda 10‑minuters mikrovågsassisterat syntessteg dopade de kärnan med en av tio olika radioaktiva metaller som ofta används för PET‑skanningar, SPECT eller intern strålterapi. Denna enkelkärlsprocess gav partikelstorlekar med hög avkastning och, avgörande, utmärkt stabilitet i humant serum—även för utmanande terapeutiska isotoper som radium‑223 och aktinium‑225, vars sönderfallsprodukter ofta läcker ur traditionella kelatorer.
Avbildning av blodproppar och hjärntumörer
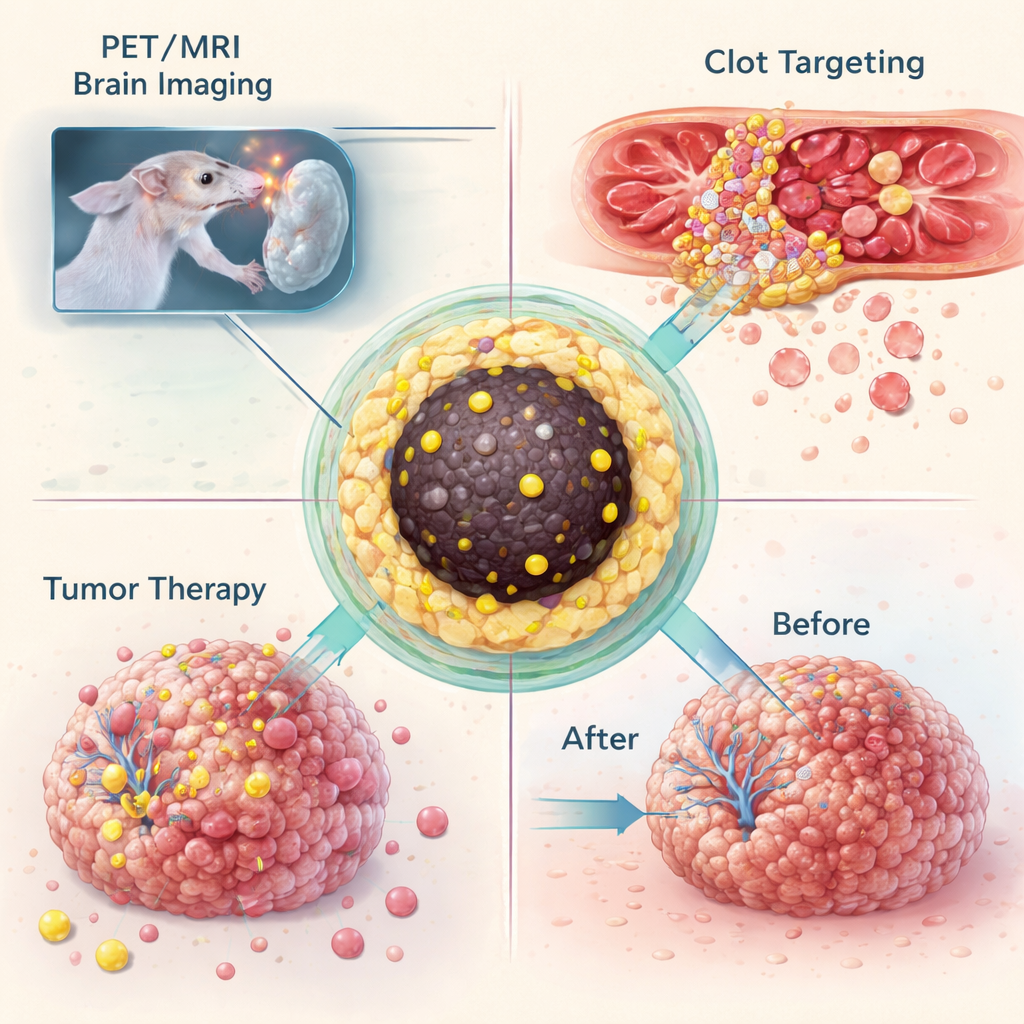
När de visat att de kunde fånga många olika isotoper i samma nanopartikeldesign testade teamet vad dessa ”nanotracers” kan göra i levande djur. I en musmodell för glioblastom, en dödlig hjärntumör, injicerades partiklar märkta med gallium‑68 i blodet och avbildades med kombinerad PET och MR. Partiklarna ackumulerades i tumörer som var tillräckligt stora för att störa blod‑hjärnbarriären, vilket gjorde att samma formulering gav både stark MR‑kontrast och en känslig PET‑signal. I ett separat experiment modifierades partiklarna kemiskt så att de kunde kopplas ihop, via en mycket selektiv click‑reaktion, med en antikropp som söker upp aktiverade blodplättar i blodproppar. I möss med skadad karotisartär gav denna tvåstegs ”pretargeting”‑strategi tydliga PET‑signaler vid proppplatsen, medan kontrollgrupper inte visade något sådant hetområde.
Från diagnos till behandling och säkrare utsöndring
Samma plattform användes också för att leverera behandling. När nanopartiklar laddade med lutetium‑177 injicerades direkt i glioblastomtumörer hos möss stannade partiklarna till stor del kvar i tumormassan i minst två veckor. Under den tiden växte obehandlade tumörer till flera gånger sin ursprungliga storlek, medan behandlade tumörer upphörde att växa, vilket tyder på att den lokaliserade stråldosen var tillräcklig för att stoppa progressionen. Med insikten att upprepade behandlingar kan överbelasta lever och mjälte med järn justerade teamet syntesförhållandena för att framställa ännu mindre partiklar—runt fyra till fem nanometer—som är tillräckligt små för att filtreras av njurarna. Dessa förminskade partiklar höll fortfarande sin radioaktiva last säkert men utsöndrades snabbt i urinblåsan, vilket minskade långsamt ackumulation i stora organ.
Vad detta kan innebära för framtida cancerbehandling
För icke‑specialister är huvudbudskapet att forskarna har byggt en enkel, flexibel nanopartikelplattform som kan kombineras med många olika radioaktiva metaller utan att kemin måste uppfinnas om varje gång. I djurmodeller kan samma grundpartikel hjälpa till att upptäcka hjärntumörer, framhäva blodproppar, leverera strålning direkt in i tumörer och till och med justeras för att lämna kroppen via njurarna. Även om mer arbete krävs innan denna metod når patienter erbjuder den en lovande väg för att designa familjer av diagnostiska och terapeutiska medel som uppvisar samma beteende i kroppen, där de bara skiljer sig åt i vilken typ av strålning de bär. Denna konsekvens kan förenkla utveckling, förbättra säkerhetstester och i slutändan göra avancerade nuklearmedicinska verktyg mer tillgängliga.
Citering: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
Nyckelord: radiotheranostik, nanopartiklar, PET-avbildning, glioblastom, målinriktad strålbehandling