Clear Sky Science · sv
Modeller med ordinära differentialekvationer för SARS-CoV-2:s replikationsdynamik och effekter av antivirala läkemedel
Varför siffror spelar roll för ett nytt virus
När COVID-19 dök upp kunde läkare se vad viruset gjorde mot patienter, men de kunde inte lätt förutsäga vem som skulle bli allvarligt sjuk eller när ett läkemedel borde ges för bästa effekt. Denna översiktsartikel visar hur forskare omvandlade virusmätningar från patienter, djur och cellodlingar till matematiska ”filmer” av infektionen inne i kroppen. Dessa modeller använder ekvationer för att följa hur viruset växer, hur våra celler och immunsystem reagerar samt hur antivirala läkemedel och vacciner kan tippa vågskålen till vår fördel.
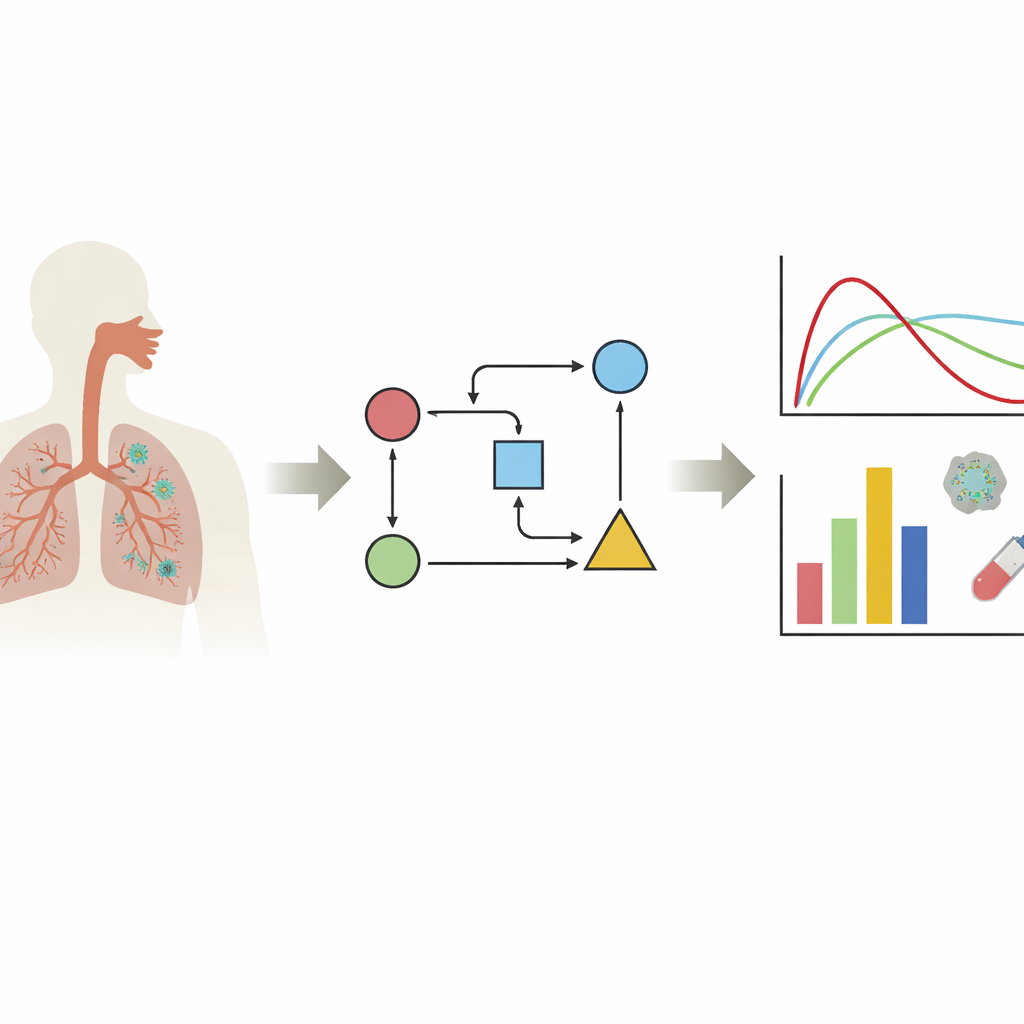
Att följa viruset inne i kroppen
Författarna fokuserar på en familj av modeller kallade målcellbegränsade modeller. Enkelt uttryckt följer dessa modeller tre huvudaktörer: friska celler som kan infekteras, redan infekterade celler och fria viruspartiklar. Genom att mata in verkliga data om virusnivåer i dessa ekvationer kan forskare uppskatta dolda egenskaper hos infektionen: hur snabbt viruset infekterar celler, hur länge en infekterad cell producerar virus och hur snabbt viruset rensas bort. Översikten visar att det mesta arbetet koncentreras till de vävnader som betyder mest för COVID-19—näsan samt övre och nedre luftvägarna—medan endast några få modeller undersöker andra organ. Ett viktigt budskap är att virusets beteende kan se mycket olika ut beroende på vilken vävnad, vilken virusvariant och vilken laboratoriecellsstam som studeras, så det finns ingen enskild "typisk" infektionskurva.
Vad vi lär oss om immunsystemet
Många modeller lägger till lager som representerar immunsystemets tidiga försvar och dess långsammare, mer riktade svar. Studier som fokuserar på första försvarslinjen antyder att snabb, välavvägd aktivitet från medfödda immunceller och signalmolekyler kan dämpa infektionen, men sällan rensa bort den helt på egen hand. Annat arbete belyser den avgörande rollen för T‑celler och antikroppar för slutligen få viruset under kontroll. Modellerna fångar också en mörkare sida: om det riktade immunsvaret kommer sent eller är felriktat kan samma verktyg som ska skydda oss driva fram skadliga ”cytokinstormar”, där överskott av inflammatoriska signaler skadar frisk vävnad. I dessa simuleringar avgörs ofta gränsen mellan hjälpsam och skadlig immunaktivitet om sjukdomen förblir lindrig eller blir livshotande.
När läkemedel och vacciner fungerar bäst
Där ekvationer kan köras om och om igen under olika antaganden blir de kraftfulla verktyg för att testa behandlingsstrategier i datorn innan man prövar dem på människor. I många studier enas modellerna om en central punkt: antivirala läkemedel fungerar bäst när de ges mycket tidigt, innan viruset nått sin topp och infekterat majoriteten av tillgängliga celler. Behandlingar som blockerar virusets kopiering av sitt genetiska material framstår som särskilt lovande, särskilt i kombination med andra läkemedel som verkar genom olika mekanismer. Sen behandling tenderar däremot att ha liten effekt i simuleringar om inte flera starka läkemedel används tillsammans. Vaccination förutsägs konsekvent att överträffa enbart läkemedel, främst genom att förbereda immunsystemet så att det känner igen viruset snabbt och håller höga virusnivåer kortvariga.
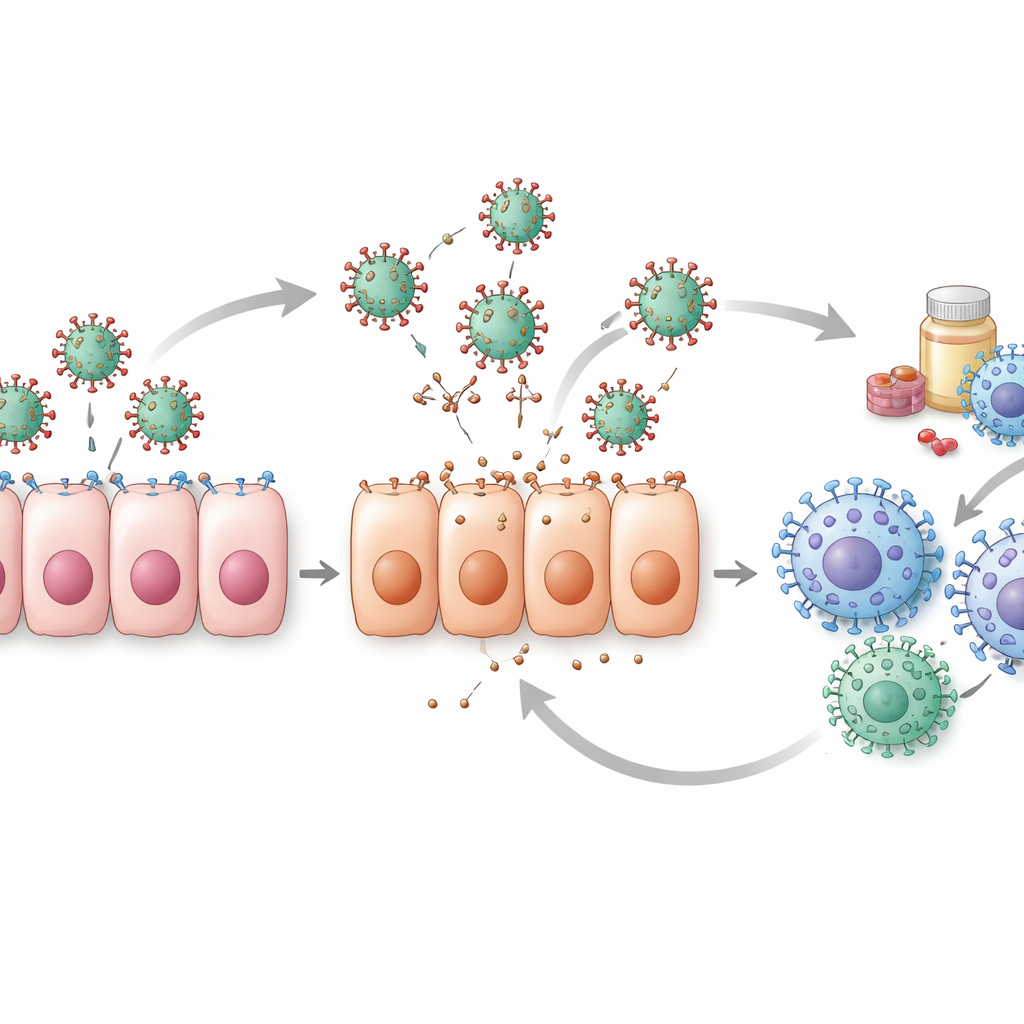
Dolda utmaningar i datan
Översikten belyser också svagheterna bakom siffrorna. De flesta kliniska dataset börjar först efter att människor redan känner sig sjuka, vilket innebär att modeller ofta missar de avgörande första dagarna av infektionen när virusnivåerna stiger snabbast. Utan dessa tidiga mätningar kan olika kombinationer av modellparametrar förklara samma data, vilket gör det svårt att veta vilken förklaring som är riktig. Endast en minoritet av studierna utför noggranna kontroller för att se om deras parameteruppskattningar verkligen är unika och tillförlitliga. Djursstudier och cellkulturförsök hjälper till att fylla vissa luckor, särskilt för tidiga tidpunkter, men skillnader mellan arter och laboratoriesystem begränsar hur direkt dessa resultat kan tillämpas på människor.
Vad detta betyder framöver
För icke-specialister är slutsatsen att noggrant byggda matematiska modeller i hög grad har förbättrat vår förståelse av hur SARS-CoV-2 beter sig inne i kroppen och hur tidpunkt, läkemedelskombinationer och tidigare vaccination formar utfallen. Modellerna är ense om att tidig, kraftfull intervention—särskilt genom vaccination och väl tajmade antivirala medel—ger immunsystemet bäst möjlighet att segra, medan fördröjda svar, vare sig från kroppen eller från behandling, kopplas till svårare sjukdom. Samtidigt betonar författarna att dessa verktyg bara är så bra som de data som matas in i dem. För att förbereda sig för framtida varianter eller nya virus efterlyser de rikare, tidigare kliniska provtagningar och bredare immunsmätningar, så att de "siffror som ligger bakom infektionen" kan vägleda snabbare och mer precisa beslut vid verkliga utbrott.
Citering: Kapischke, T., Herrmann, S.T., Bertzbach, L.D. et al. Ordinary differential equation models of SARS-CoV-2 replication dynamics and antiviral drug efficacies. npj Viruses 4, 17 (2026). https://doi.org/10.1038/s44298-026-00183-8
Nyckelord: SARS-CoV-2 viral dynamik, modellering inom värden, tidpunkt för antiviral behandling, immunsvar, COVID-19-vaccination