Clear Sky Science · sv
Olika roller för Hsp70-chaperoner i orthoflavivirus proteinssekretion och virionbildning
Varför små värmechockshjälpare spelar roll för hjärninfekterande virus
Virus som sprids av fästingar och myggor, såsom fästingburen encefalit och West Nile‑virus, kan tränga in i hjärnan och orsaka allvarlig sjukdom, ändå finns det fortfarande inga specifika läkemedel som stoppar dem. Denna studie undersöker hur dessa virus kapar en grupp av våra egna protein "hjälpare", kallade Hsp70‑chaperoner, för att bygga och släppa ut nya viruspartiklar. Eftersom Hsp70‑proteiner redan undersöks som läkemeddsmål vid cancer kan förståelsen av denna relation öppna nya vägar för att behandla farliga virusinfektioner utan att angripa virusen direkt.
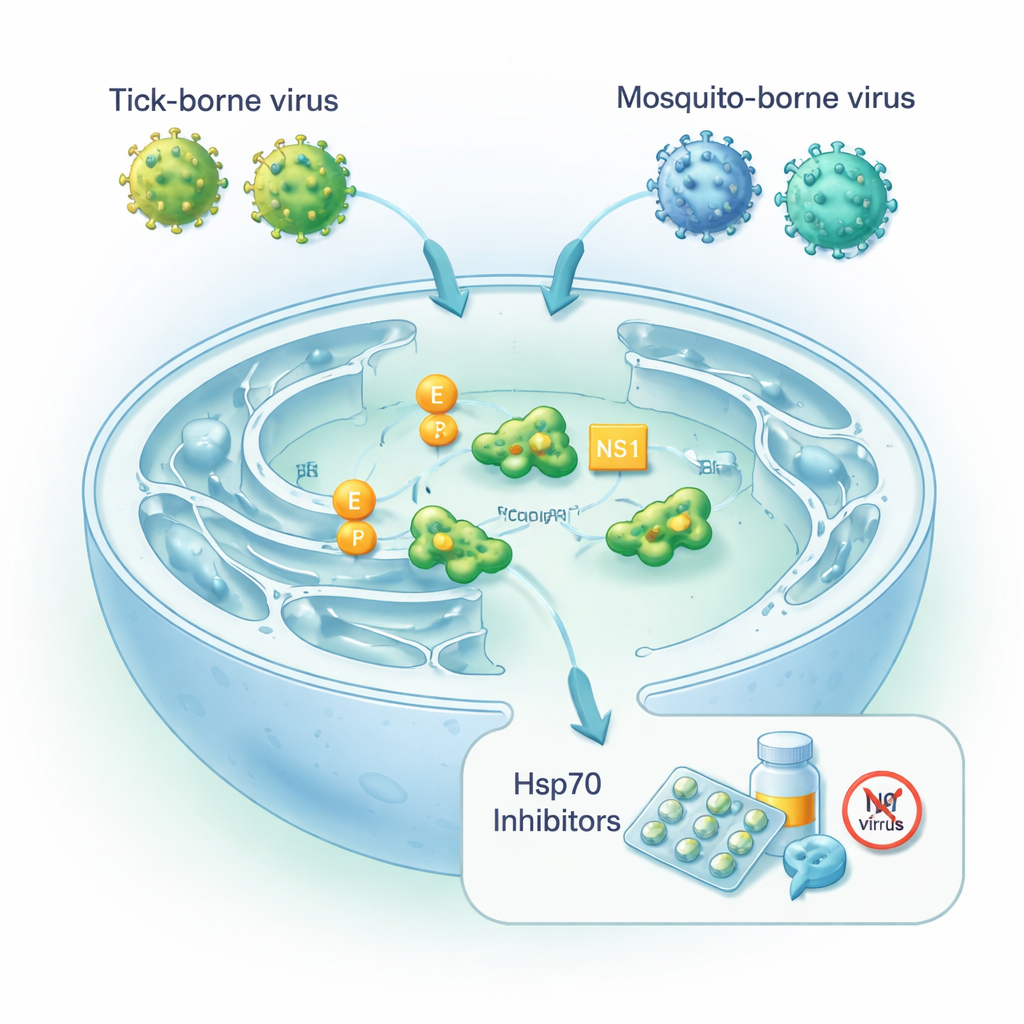
Virus som lutar sig mot cellens vikningsmaskineri
Orthoflavivirus är små RNA‑virus vars genetiska material kodar för ett långt polyprotein som måste klyvas och vikas till flera funktionella delar. Två viktiga virala komponenter är höljeproteinet E, som täcker viruspartikeln och möjliggör inträde i nya celler, och det icke‑strukturella proteinet NS1, som hjälper viruset kopiera sitt genom och kan sekreteras för att manipulera immunsystemet. Allt detta sker i det endoplasmatiska nätverket, den del av cellen där många proteiner viks och förbereds för export. Där förlitar sig cellen på Hsp70‑chaperoner, inklusive en lokal form kallad BiP, för att förhindra att nysyntetiserade proteiner felviks under stress. Författarna undersökte hur starkt neurotrofa fästings‑ och myggburna orthoflavivirus är beroende av dessa chaperoner för att montera infektiösa partiklar.
Direkta handslag mellan virala proteiner och Hsp70
Genom att använda celler konstruerade för att överproducera specifika virala proteiner, samt celler infekterade med autentiska virus, drog forskarna ner BiP eller Hsp70 och kontrollerade vilka virala partner som följde med. De fann att BiP och Hsp70 konsekvent bildade komplex med höljeproteinet E från flera orthoflavivirus, oavsett om de bar på fästingar eller myggor. Detta tyder på att vikningen av E i det endoplasmatiska nätverket styrs av dessa chaperoner. Bilden var mer selektiv för NS1: BiP och Hsp70 band starkt till NS1 från de fästingburna virusen fästingburen encefalitvirus och Langatvirus, men inte till NS1 från de myggburna West Nile‑ och Usutu‑virusen. Dessa skillnader återspeglar sannolikt variationer i hur NS1 är försedd med sockergrupper och hur det viks, vilket antyder att inte alla närbesläktade virus använder samma värdvägar.
Blockering av chaperoner minskar kraftigt virusutsläpp
Eftersom Hsp70‑proteiner är drogbar testade gruppen två små molekyler som stör olika delar av chaperonmaskineriet. YM‑1 riktar sig mot nukleotidbindningsdomänen och fryser Hsp70‑proteiner i ett inaktivt tillstånd, medan PES‑Cl blockerar substratbindningsfickan som normalt greppar klientproteiner. Vid doser som lämnade de flesta celler vid liv minskade YM‑1 drastiskt mängden infektiöst virus som släpptes ut för alla fyra testade orthoflavivirus och sänkte mängden höljeprotein som påträffades i odlingsvätskan, vilket pekar på ett generellt hinder för partikelbildning eller utsläpp. PES‑Cl hade däremot liten effekt på infektiösa titrar eller nivåer av höljeprotein, trots att det försvagade den fysiska interaktionen mellan Hsp70/BiP och höljeproteinet i bindningsanalyser. Detta tyder på att kortvarig störning av greppfickan inte räcker för att förlama virusmontering, medan att stänga ner chaperonens energidrivna cykel är det.
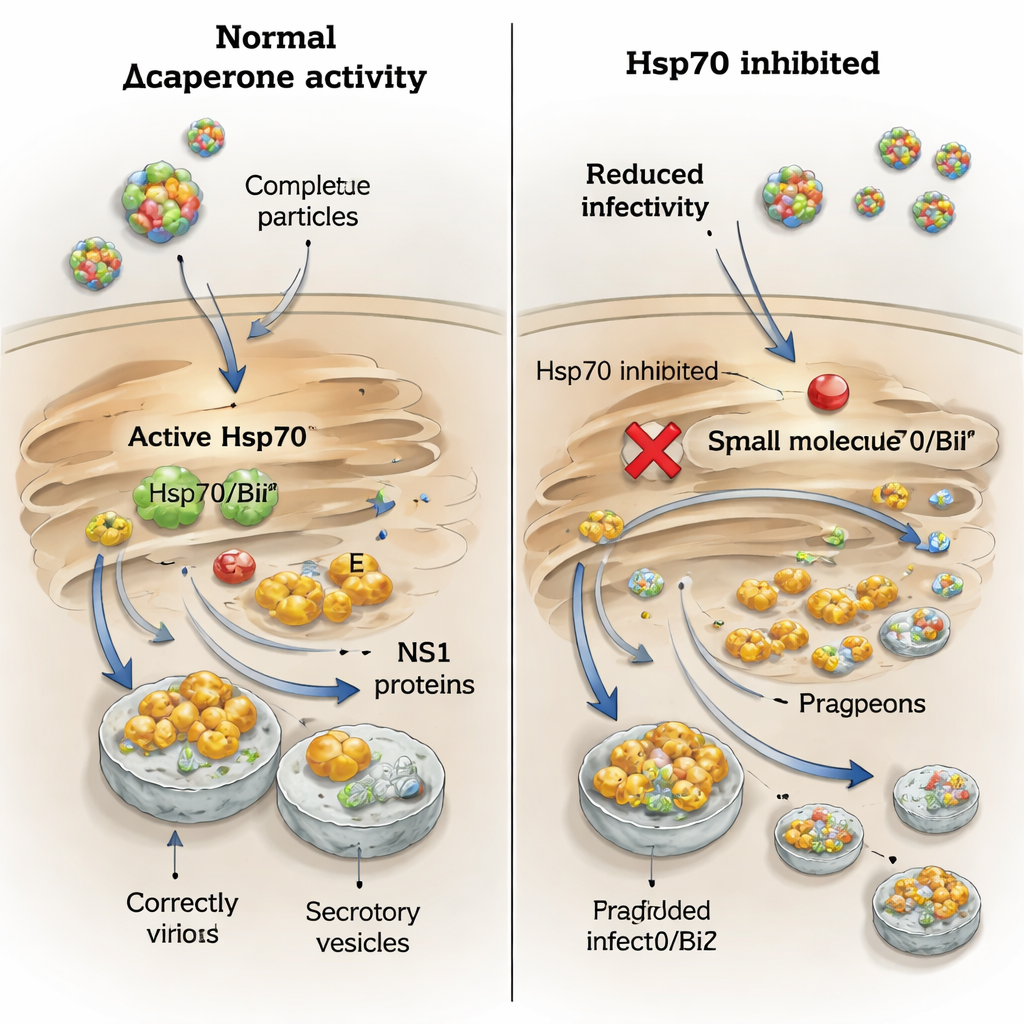
En särskild beroende för fästingburna virus av BiP för NS1
Berättelsen för NS1 var mer nyanserad. När infekterade celler behandlades med PES‑Cl sjönk sekretionen av NS1 från fästingburen encefalit- och Langatvirus kraftigt, medan NS1 från West Nile‑ och Usutu‑virus inte påverkades. Detta speglar tidigare fynd att endast de fästingburna NS1‑proteinerna binder starkt till BiP och Hsp70. För att zooma in på BiP:s roll använde författarna små interfererande RNA för att specifikt sänka BiP‑nivåerna. Detta minskade mängderna av både hölje‑ och NS1‑proteiner inne i cellerna och i den omgivande vätskan för fästingburen encefalit‑ och West Nile‑virus, men mängden infektiöst virus föll bara måttligt. När BiP‑depleterade celler behandlades med läkemedel som blockerar proteinnedbrytning återhämtade sig NS1‑nivåerna inne i cellen men dess sekretion gjorde det inte, vilket visar att BiP behövs inte bara för att skydda NS1 från nedbrytning utan också för att vägleda det längs sekretoriska vägen.
Vad detta innebär för framtida antivirala strategier
För en icke‑specialist är huvudbudskapet att dessa hjärninfekterande virus starkt förlitar sig på cellens egna proteinvikningshjälpare för att bygga sitt yttre hölje och, för vissa arter, för att skicka ut NS1 som ett sekreterat vapen. En bredverkande chaperonhämmare som YM‑1 kan därför kraftigt minska produktionen av infektiösa partiklar från flera närbesläktade virus samtidigt, även om dess kraftfulla effekter sannolikt sträcker sig bortom en enskild chaperon och kan stressa friska celler också. Mer riktade angreppssätt, kanske med fokus på hur BiP och Hsp70 hanterar specifika virala klienter som NS1, kan en dag hjälpa till att utforma behandlingar som är svårare för virus att utveckla resistens mot samtidigt som de skonar det mesta av den normala proteinvikningen i värden.
Citering: Blank, L., Lorenz, C. & Steffen, I. Divergent roles of Hsp70 chaperones in orthoflavivirus protein secretion and virion formation. npj Viruses 4, 8 (2026). https://doi.org/10.1038/s44298-026-00175-8
Nyckelord: orthoflavivirus, Hsp70-chaperon, fästingburen encefalitvirus, West Nile-virus, antivirala läkemeddsmål