Clear Sky Science · sv
Det lösliga G-proteinet hos respiratoriskt syncytialvirus främjar viral spridning via TLR2-medierad NLRP3-priming och pyroptos
Varför detta lungvirus är viktigt för alla
Respiratoriskt syncytialvirus, eller RSV, är mest känt som ett vinterhot mot spädbarn, men det skickar också många äldre och personer med nedsatt immunförsvar till sjukhus. Även med nya vacciner och skyddande antikroppar återinfekterar RSV människor om och om igen och kan orsaka svåra lungsymptom. Denna studie undersöker ett lite känt virusprotein, en löslig form av RSV:s G-protein, och visar hur det kan förbereda lungceller för explosiv inflammation och hjälpa viruset att sprida sig mer effektivt genom luftvägarna.
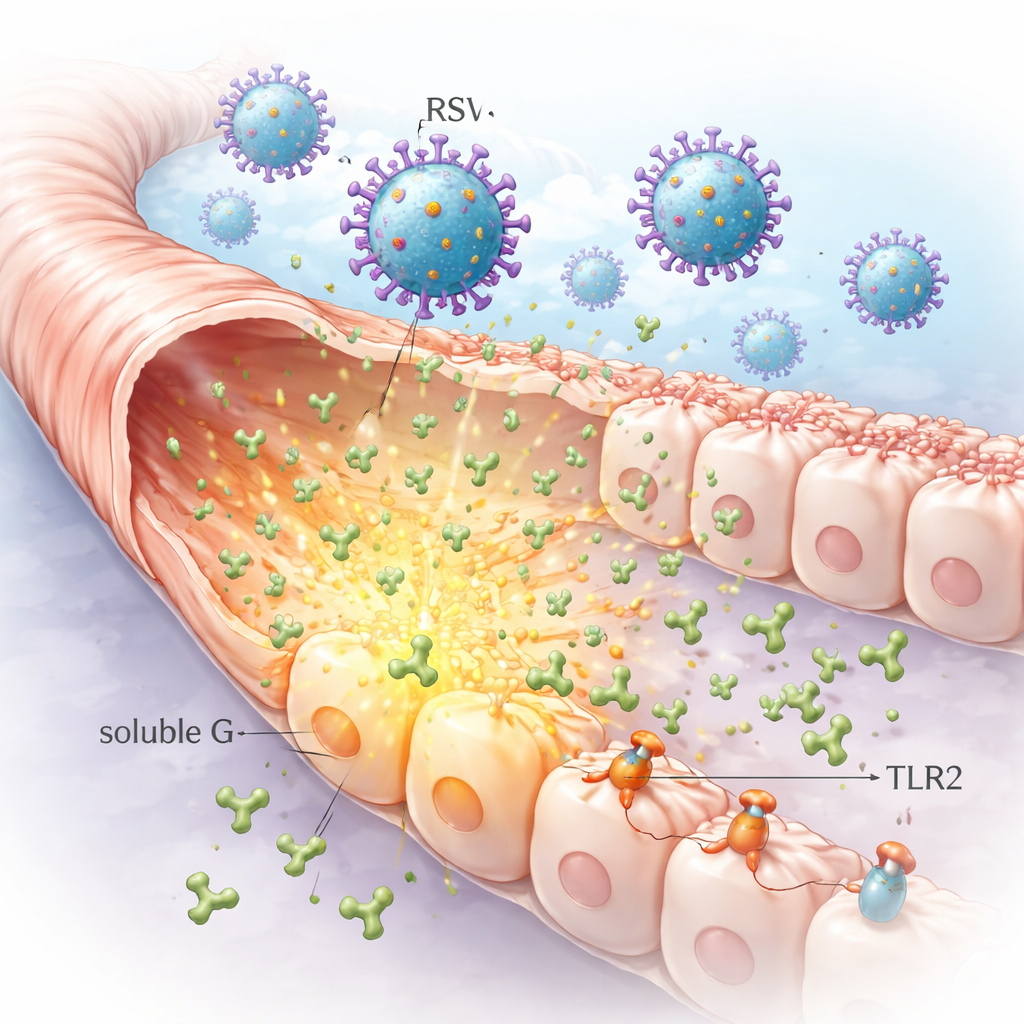
Ett sekreterat virusprotein som rör sig framför infektionen
RSV har ett fästningsprotein kallat G på ytan som hjälper det att fästa vid luftvägsceller. Ovanligt nog frisätter infekterade celler också stora mängder av en fritt flytande version av detta protein, känd som lösligt G. Forskarna visade att lungceller infekterade i laboratoriet kan avge mycket höga nivåer av lösligt G i sin omgivning. Eftersom denna form kan diffundera bort från den ursprungliga infektionsplatsen kan den nå närliggande celler som ännu inte är infekterade och därmed bana väg för bredare förändringar i lungans ytskikt än vad viruset ensam skulle orsaka.
Lösligt G som en tvåfunktionell nyckel på cells yta
Genom att kombinera mikroskopi, biokemiska pull-down-tester och enzymbehandlingar kartlade teamet hur lösligt G fäster vid celler. De fann att det kan binda till sockerkedjor kallade glycosaminoglykaner samt till en känd RSV-receptor som heter CX3CR1. Avgörande nog binder lösligt G också till ett mönsterkännande molekyl på immunceller och luftvägsceller kallat TLR2. Ett litet motiv i G-proteinet, känt som CX3C, visade sig vara viktigt för stark bindning till CX3CR1 och för robust rekrytering av TLR2. Det innebär att lösligt G först kan fångas upp löst på cellytan och sedan engagera mer specifika receptorer som styr hur celler svarar på hot.
Priming av lungceller för en inflammatorisk typ av celldöd
Engagemang av TLR2 av lösligt G visade sig vara långt ifrån ofarligt. I rapporterceller från immunsystemet och i humanlungcellinjer aktiverade lösligt G MyD88–NF-κB-signalvägen nedströms om TLR2, vilket ledde till frisättning av inflammatoriska budbärare såsom IL-6 och IL-8. Samtidigt ökade det produktionen av komponenter i ett molekylärt "larmsystem" kallat NLRP3-inflammasom och enzymer som genererar reaktiva molekyler som kväveoxid och syreradikaler. Dessa förändringar orsakade isolerat sett endast mild skada. Men när de förberedda cellerna senare infekterades med RSV utlöstes full montering av inflammasomet, aktivering av enzymet caspas‑1, bildning av porer i cellmembranet och en hetsig form av celldöd känd som pyroptos. Denna process borrade hål i cellerna, spillde inflammatoriskt innehåll och sammanföll med högre mängder infektiöst virus som släpptes ut i odlingsvätskan.
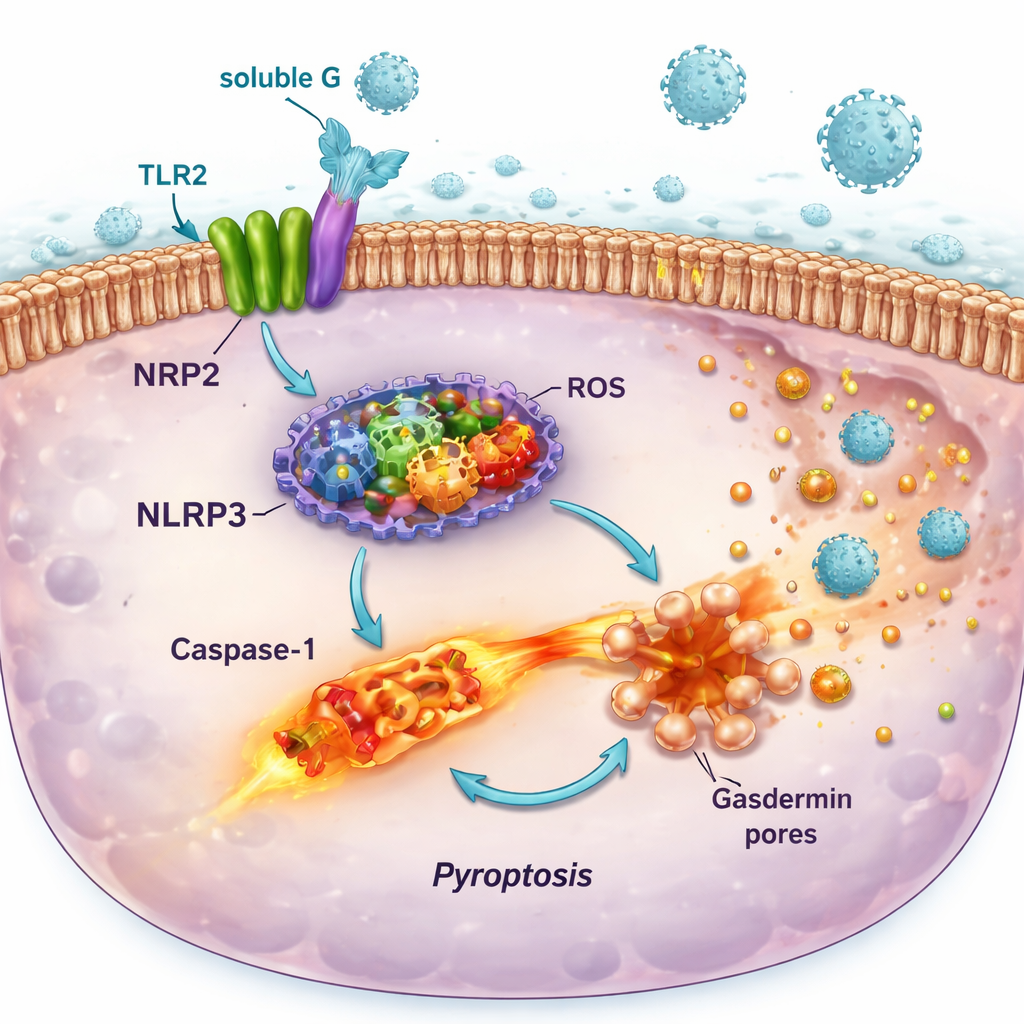
Hur denna kedjereaktion kan förvärra lungsjukdom
Den pro-dödliga effekten av lösligt G var starkast i luftvägsepitelceller — de celler RSV föredrar att infektera — och var beroende av NLRP3-inflammasomet, eftersom en specifik NLRP3-hämmare till stor del återställde cellernas livskraft. I kontrast genomgick vissa immunceller som var rika på TLR2 men fattiga på CX3CR1 inte samma uttalade lytiska död under samma förhållanden. Detta mönster tyder på att RSV använder lösligt G för att selektivt försvaga och förstöra luftvägarnas skyddande ytskikt samtidigt som vissa immunceller bevaras för att fortsätta sända signaler. Resultatet är en lungmiljö med mer inflammation, mer celldebris och fler möjligheter för nya viruspartiklar att undkomma och infektera intilliggande celler.
Vad detta betyder för framtida behandlingar
För en icke-specialist är huvudbudskapet att RSV inte enbart förlitar sig på direkt skada från virusinvasion. Genom att frisätta stora mängder lösligt G-protein kan det "mjukgöra" närliggande celler via TLR2, vilket gör dem mer benägna att dö på ett inflammatoriskt sätt och att släppa ut virus. Detta arbete identifierar flera steg i den kedjan — det lösliga G:et självt, dess CX3C-motiv, TLR2 och NLRP3-inflammasomet — som potentiella läkemedelsmål. I princip skulle terapier som blockerar interaktionen mellan lösligt G och TLR2, eller som dämpar NLRP3-aktivitet, kunna minska både lungskada och virusspridning. Sådana angreppssätt kan i framtiden komplettera befintliga RSV-vacciner och antikroppar och erbjuda bättre skydd för de yngsta och mest sårbara patienterna.
Citering: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
Nyckelord: respiratoriskt syncytialvirus, lösligt G-protein, TLR2-inflammasom, pyroptos, lungeinflammation