Clear Sky Science · sv
STAR (stroma-tumor AI risk) bedömning: samband mellan AI-beräknad tumör‑stroma‑proportion och patientöverlevnad ger tillskjuten prognostiskt värde utöver KELIM vid epitelial äggstockscancer
Varför “grannskapet” runt en tumör spelar roll
När vi tänker på cancer föreställer vi oss ofta en klump av avvikande celler. Men tumörer lever i ett livligt grannskap av stödvävnad, blodkärl och immunceller som kallas stroma. Den här studien ställer en enkel men kraftfull fråga: kan vi använda balansen mellan tumörceller och den omgivande vävnaden, mätt med artificiell intelligens (AI) på rutinmässiga mikroskopiska preparat, för att förutsäga vilka patienter med äggstockscancer som sannolikt får bättre eller sämre utfall — redan före behandlingens början?
Ett nytt sätt att läsa standardbiopsier
Kvinnor med epitelial äggstockscancer får vanligtvis vävnad borttagen vid operation eller biopsi. Dessa prover färgas och undersöks i mikroskop på alla sjukhus. Forskarna fokuserade på en egenskap kallad tumör–stroma‑proportion (TSP): hur stor del av bilden som består av stödjande vävnad jämfört med cancerceller. I tidigare arbete uppskattade patologer denna andel med blotta ögat och fann att tumörer rika på stroma ofta betedde sig mer aggressivt och var mer resistenta mot standardkemoterapi med platina. I den aktuella studien använde teamet ett djupinlärnings‑AI‑system för att automatiskt mäta TSP på digitaliserade preparat, med målet att göra en manuell, delvis subjektiv uppgift till en snabb och reproducerbar avläsning som är tillgänglig redan vid diagnos.
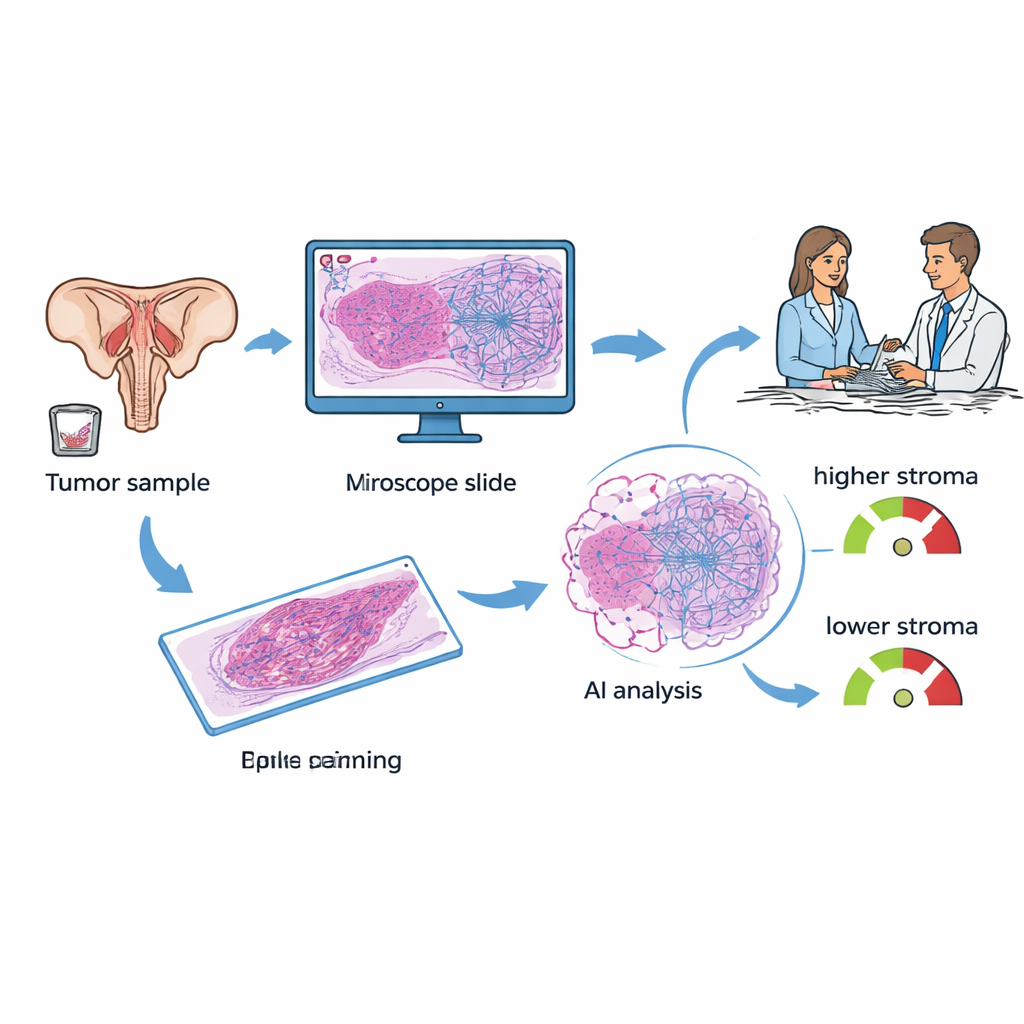
Jämförelse mellan AI‑vävnadsanalys och ett blodbaserat mått
Idag är ett ofta diskuterat verktyg för äggstockscancer KELIM, ett mått baserat på hur snabbt en blodmarkör kallad CA‑125 sjunker under de första 100 dagarna av kemoterapi. KELIM är billigt och användbart, men det kan bara beräknas efter flera veckors behandling, och inte alla patienter har tillräckligt tidiga blodprover för att generera poängen. Utredarna sammanställde data från 89 kvinnor som behandlats vid ett enda cancersjukhus och som hade både vävnadspreparat och minst tre CA‑125‑mätningar. De beräknade KELIM för varje patient, lät en patolog märka ut tumörområden på preparaten och lät sedan AI‑modellen uppskatta TSP, och klassificerade varje fall som ”stroma‑låg” (mindre än 50 % stroma) eller ”stroma‑hög” (50 % eller mer).
AI motsvarar experter och identifierar högre risktumörer
AIns bedömning stämde väl överens med erfarna patologers: i 94 % av fallen överensstämde den automatiska TSP‑klassificeringen med den manuella, en grad av överensstämmelse som anses utmärkt. När teamet granskade patientutfall fann de att kvinnor vars tumörer klassificerades som stroma‑höga av AI hade signifikant sämre total överlevnad än de med stroma‑låga tumörer. Statistiskt sett nästan fördubblade hög TSP risken för död under uppföljningen, och denna effekt kvarstod även efter att KELIM‑poängen beaktats. Däremot var KELIM i denna verkliga patientgrupp kopplat till om tumörer var resistenta mot platinumbaserad behandling men inte tydligt relaterat till hur länge patienterna levde.
Vad detta kan innebära för behandlingsbeslut
Eftersom TSP kan mätas från rutinpreparat tagna vid tidpunkten för diagnos erbjuder AI‑baserad TSP ett sätt att bedöma risk innan kemoterapi påbörjas, potentiellt månader tidigare än KELIM. Ett högt TSP‑resultat kan varna kliniker för att en tumör är mer benägen att vara aggressiv och svårbehandlad, vilket kan leda till tätare uppföljning, tidigare övervägande av kompletterande terapier eller andra kirurgiska strategier. Metoden är också relativt lågkostnad: den bygger på befintliga patologibilder och en programvarumodell snarare än nya laboratorietester. Författarna menar att automatiserad TSP kan användas tillsammans med andra markörer, såsom genetiska tester och CA‑125‑trender, för att förfina prognosen utan att tillföra avsevärd börda för patienter eller patologiavdelningar.
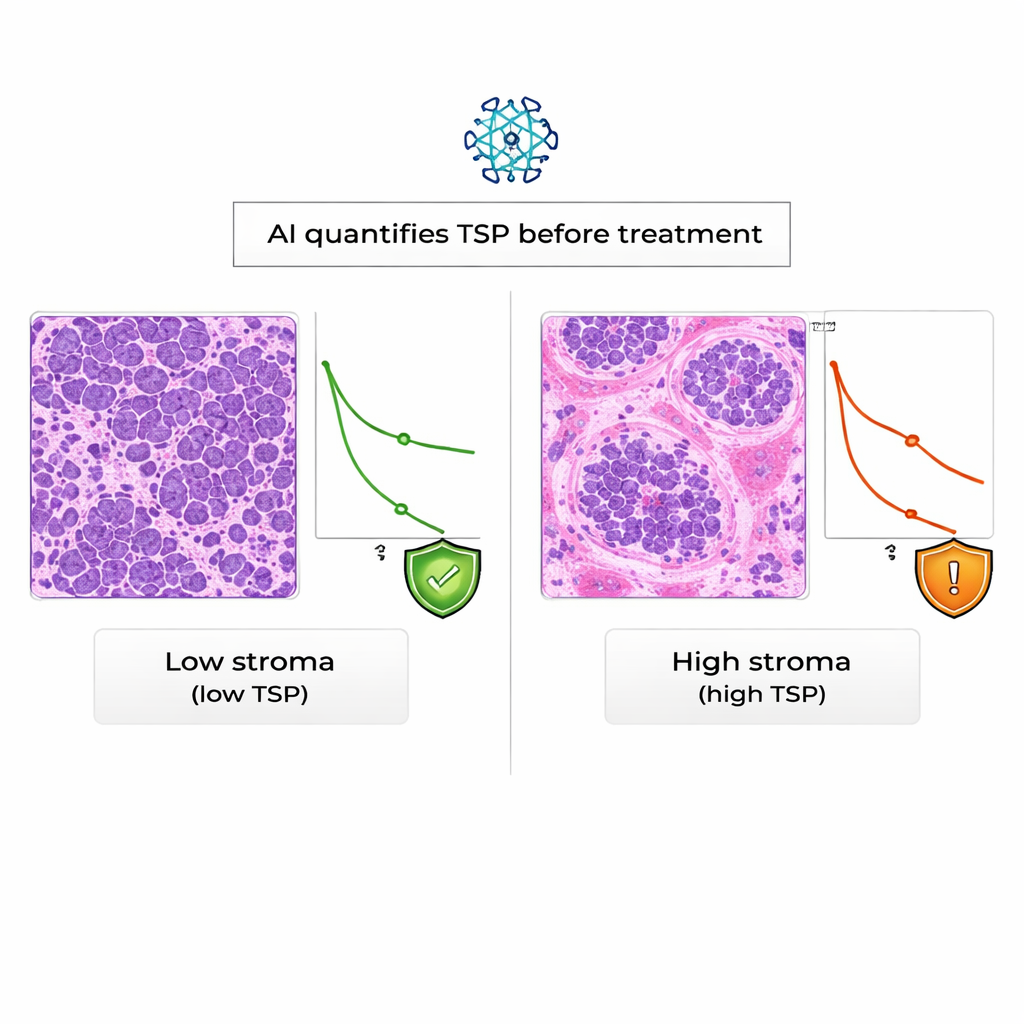
Framåtblick: smartare och tidigare vägledning för patienter
För en lekmannapublik är huvudbudskapet att inte alla äggstockscancer är lika, och att stödvävnaden runt tumören bär viktiga ledtrådar om hur sjukdomen kommer att utvecklas. Denna studie visar att AI kan läsa dessa ledtrådar pålitligt på standardbiopsier och att en stroma‑tung tumör tenderar att vara kopplad till sämre överlevnad, oberoende av befintliga blodbaserade mått. Medan större och mer mångsidiga studier behövs innan detta tillvägagångssätt blir en del av rutinvården, har AI‑beräknad TSP potentialen att fungera som en tidig varningssignal som kan hjälpa läkare att skräddarsy behandlingsplaner och ge patienter tydligare förväntningar från början.
Citering: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
Nyckelord: äggstockscancer, artificiell intelligens, tumörmikromiljö, prognostisk biomarkör, digital patologi