Clear Sky Science · sv
Globalt svar på antibiotikaexponering avslöjar en avgörande roll för nukleotidmetabolism i höggradig β-laktam-tolerans
Varför vissa bakterier nonchalant klarar våra bästa antibiotika
Antibiotika ska utplåna skadliga bakterier, ändå kvarstår många infektioner envist eller återkommer efter behandling. Denna artikel undersöker en ofta förbisedd orsak: vissa bakterier kan gräva ner sig och tillfälligt överleva även mycket höga doser av kraftfulla läkemedel som penicillin. Genom att kartlägga hur dessa mikrober omprogrammerar sin inre kemi för att uthärda attacken pekar forskarna på nya sätt att återställa effekten hos befintliga antibiotika.
En dold överlevnadstrick inne i infektioner
När de utsätts för beta-laktam antibiotika som penicillin dör många farliga gramnegativa bakterier inte enkelt. Istället kan de kasta av sig sin styva cellvägg och förvandlas till spröda, runda kroppar kallade sferoplaster. I denna form slutar de föröka sig men förblir fullt vid liv och metabolt aktiva. När läkemedlet försvunnit bygger de upp väggen igen, återtar sin normala stavform och kan återigen orsaka infektion. Eftersom denna ”tolerans” är ett steg på vägen mot full antibiotikaresistens och behandlingsmisslyckande är det avgörande för framtida medicin att förstå hur sferoplaster överlever.
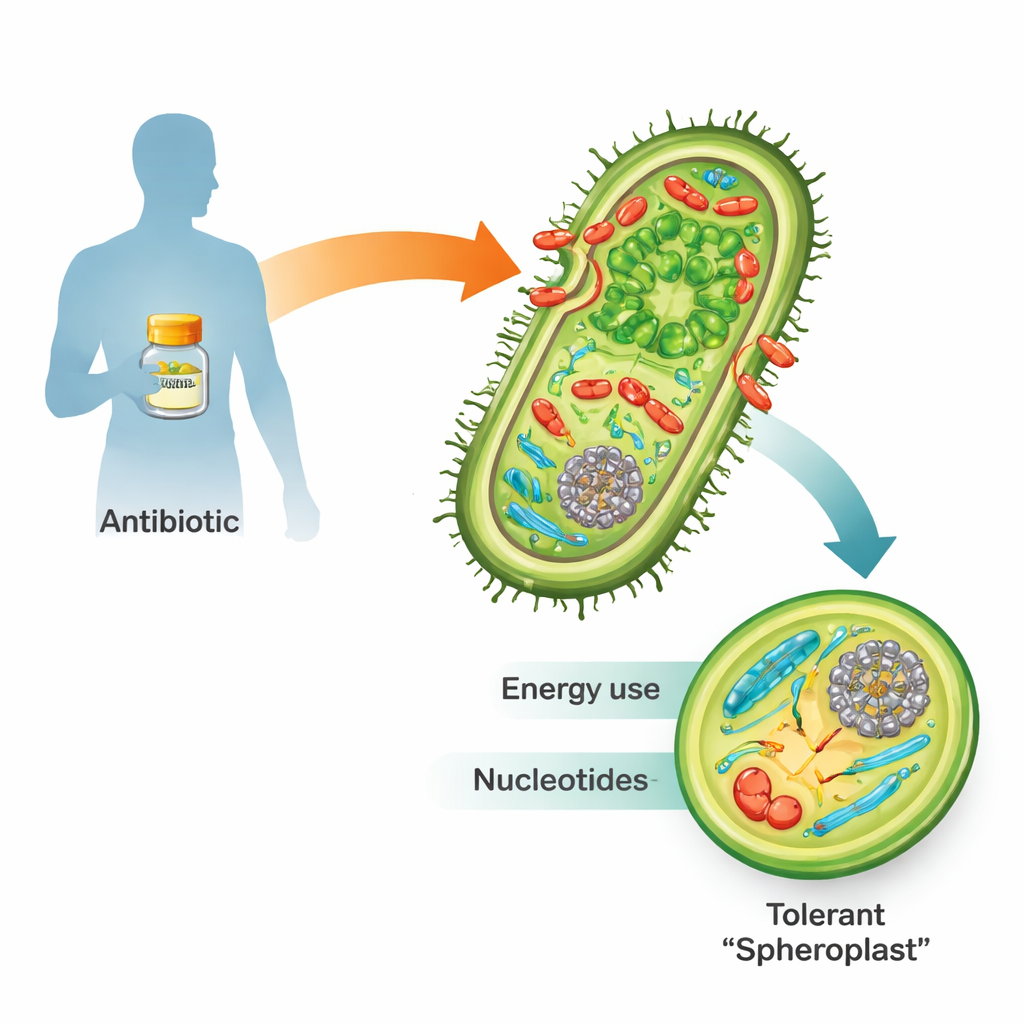
Lyssna på cellens nödsändning
Forskarna använde Vibrio cholerae, bakterien som orsakar kolera, som modell eftersom den är exceptionellt tolerant mot beta-laktamer och lätt att genetiskt manipulera. De badade bakterierna i tio gånger den minimala dödliga dosen penicillin och följde svaret över tid med två kraftfulla verktyg. Transkriptomik spårade vilka gener som slog på eller av, medan metabolomik mätte hundratals småmolekyler som driver och bygger cellen. Tillsammans skapade dessa ”multi-omiska” tekniker en tidsupplöst karta över hur en tolerant cell omstrukturerar sitt inre under en läkemedelsattack.
Metabol omdirigering och en dold svag punkt
Data visade omfattande förändringar i centrala vägar. Gener för uppbyggnad av cellväggen aktiverades starkt, i linje med cellens försök att reparera skador och förbereda återhämtning. Värmechock- och stressresponssystem eldade också upp sig, sannolikt för att hantera felveckade eller oxiderade proteiner som skapats av antibiotikainducerad stress. Samtidigt försköts central kolmetabolism: vissa steg i TCA-cykeln (cellens huvudsakliga energigenerator) ökade, medan nyckelintermediärer i glykolysen som glukos-6-fosfat och fruktos-6-fosfat drabbades av kraftig uttömning. Dessa intermediärer matar normalt både energiproduktion och byggande av cellväggen, vilket antyder att kontinuerlig, slösaktig ”meningslös cykling” av väggmaterial drog ut resurserna.
Nukleotider under press
Den mest slående förändringen rörde nukleotider, byggstenarna i DNA, RNA och många energibärande molekyler. Halterna av många nukleotider och deras prekursorer kollapsade i penicillinbehandlade celler, trots att generna för att syntetisera dem från grunden var starkt aktiverade. Samtidigt dämpades gener som är involverade i att ”återvinna” nukleotider, som om cellen försökte spara på det lilla som återstod. Dessa mönster tyder på att sferoplaster befinner sig i svår nukleotidstress. När forskarna medvetet störde vägar som levererar nukleotidprekursorer — såsom pentosfosfatvägen — eller blockerade nukleotidproduktion med ett annat läkemedel, trimetoprim, dödade kombinationen med beta-laktamer långt fler bakterier än något av läkemedlen ensamt. Denna starka synergi sågs inte bara i Vibrio cholerae utan även i höggradigt toleranta kliniska stammar av Klebsiella pneumoniae och Escherichia coli.
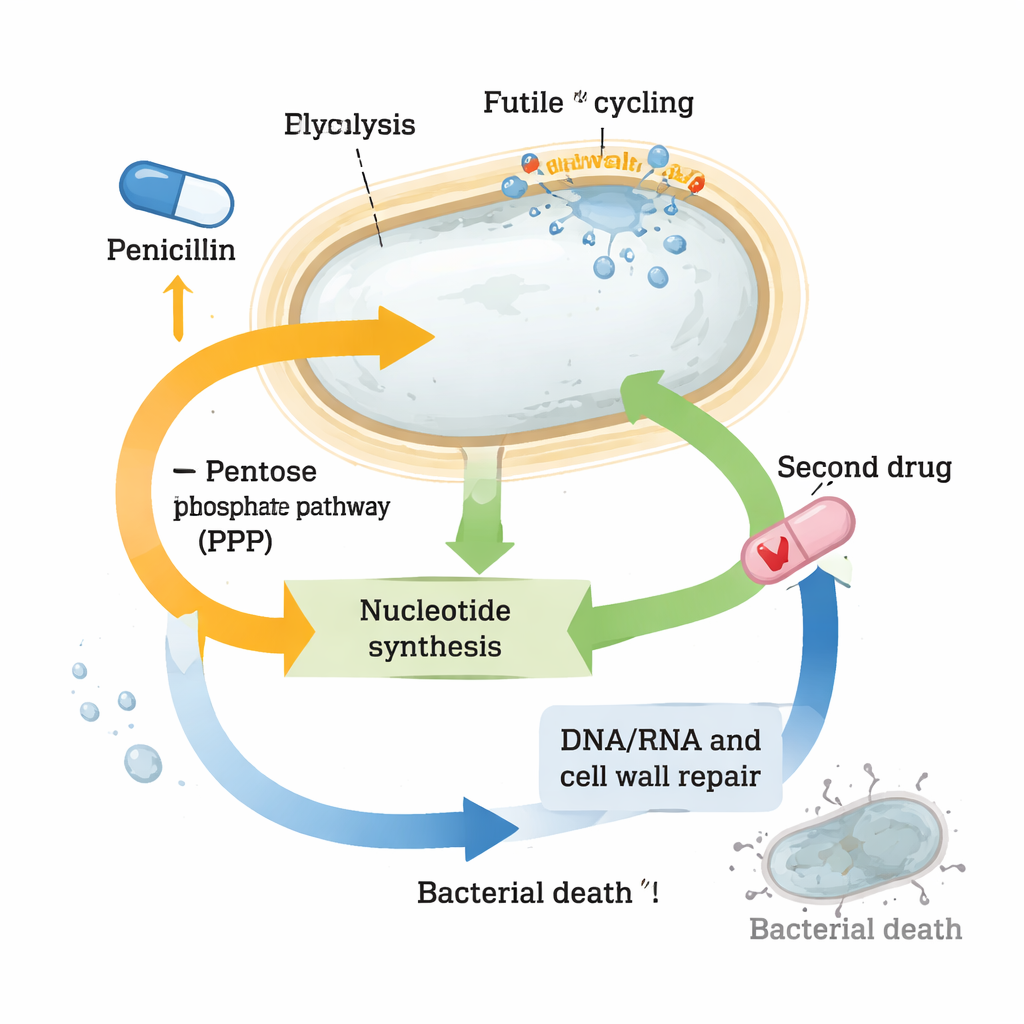
Göra överlevnadskemins svagheter till en terapeutisk fördel
Trots stora omformningar av deras metabolism lyckas toleranta sferoplaster hålla sitt energivaluta, ATP, relativt stabilt och undvika katastrofala skador, vilket hjälper dem att överleva långvarig antibiotikaexponering. Men arbetet visar att de i detta försök pressar sina nukleotidpooler till bristningsgränsen. Denna osäkra balans skapar en sårbarhet: att rubba nukleotidmetabolismen en aning till med ett andra läkemedel kollapsar deras försvar och återställer effektiv dödlighet. För lekmän är slutsatsen att vissa bakterier överlever antibiotika inte för att läkemedlen misslyckas att träffa sina mål, utan för att cellerna snabbt omkopplar sin kemi för att uthärda smällen. Genom att hitta och utnyttja svaga länkar i denna överlevnadslogik — här nukleotidmetabolismen — kan forskare kanske förvandla gamla antibiotika till kraftfulla kombinationsterapier som överlistar även höggradigt toleranta patogener.
Citering: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
Nyckelord: antibiotikatolerans, beta-laktam antibiotika, nukleotidmetabolism, bakteriell persistens, läkemedelskombinationer