Clear Sky Science · sv
Dämpning av epikardiell aktivering och myofibroblastmängd via Fbln2–Nupr1b-axeln stimulerar hjärtregenerering hos zebrafisk
Varför vissa hjärtan kan läka sig själva
När en person drabbas av en hjärtinfarkt täcks den skadade muskeln vanligtvis över av en stel ärrvävnad som aldrig riktigt återbildas. Zebrafiskar, små randiga akvariefiskar, gör något märkbart annorlunda: de återbildar hjärtvävnaden och rensar så småningom bort större delen av ärret. Denna studie ställer en bedrägligt enkel fråga med stora medicinska följder: hur vet ett läkande hjärta när det ska bygga ärrvävnad och när det ska ta bort det så att ny muskel kan växa? Genom att tyda denna balans hos zebrafiskar pekar arbetet mot strategier som en dag skulle kunna hjälpa skadade mänskliga hjärtan att reparera sig istället för att svikta.
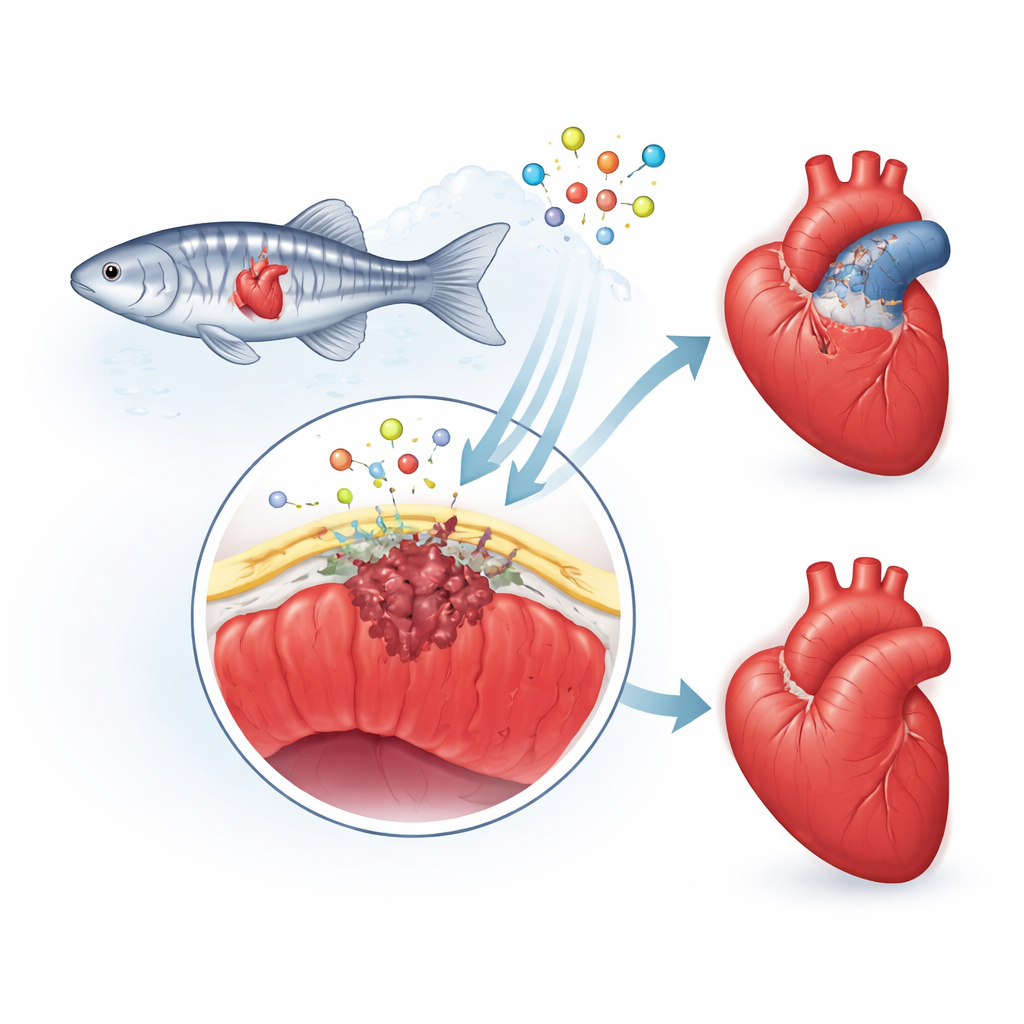
Hjärtats skyddande ytterhud
Forskarna fokuserar på epikardiet, ett tunt "skinn" som täcker hjärtat. Efter skada vaknar detta skikt till liv, cellerna ändrar identitet och en del går in i det skadade området. Där blir de stödjeceller och ärrbildande celler, och de frisätter kemiska signaler som styr tillväxten av nya blodkärl och hjärtmuskel. Hos människor tenderar denna reparationsreaktion att överkompensera och lämna kvar ett tjockt, bestående ärr. Hos zebrafiskar är ärret däremot tillfälligt och bryts gradvis ner allteftersom frisk muskel återkommer. Teamet misstänkte att ett protein kallat fibulin‑2 (Fbln2), som finns i hjärtats omgivande stödstruktur, hjälper till att ställa in hastigheten och intensiteten i denna epikardiella respons.
En molekylär dimmer för ärrbildning
Med genredigering i zebrafisk skapade forskarna två typer av djur med olika nivåer av Fbln2: en stam med reducerad Fbln2 och en annan där proteinet var helt borttaget. De skadade fiskarnas hjärtan med en fryssond, som efterliknar en hjärtinfarkt, och följde läkningsförloppet över veckor till månader. När Fbln2‑nivåerna sänktes minskade tidig celldelning i hjärtmuskel och blodkärlsfoder, men det fibrösa ärr som bildades var mindre och lättare att omforma. Efter tre månader hade dessa hjärtan regenererat väl och innehöll lite kollagen, det huvudsakliga ärrmaterialet. I kontrast visade fiskar som helt saknade Fbln2 en starkare nedreglering av en nyckelväg för tillväxt och ärrbildning, involverande en familj signaler känd som TGFβ, och hade betydligt färre ärrbildande celler precis under epikardiet. Deras tidiga ärr var också mindre—men senare misslyckades dessa hjärtan med att rensa bort kollagen och slutade med stora, bestående ärr och dålig regenerering.
Närmare granskning av epikardiella tillståndsförändringar
För att se hur epikardiella celler betedde sig på single‑cell‑nivå använde teamet single‑cell RNA‑sekvensering kort efter skadan. De identifierade flera "tillstånd" hos epikardiella celler, inklusive tysta celler, nyaktiverade celler, stressade celler som anpassar sig till låg syra, och celler som delade sig aktivt. Hos fisk med normal Fbln2 gick epikardiella celler smidigt från tysta till aktiverade till mogna tillstånd. Hos fisk med reducerad eller frånvarande Fbln2 stannade denna progression av: celler dröjde kvar i tidiga stadier och de mer mogna aktiverade grupperna var underrepresenterade, särskilt hos djuren utan Fbln2. Flera gener som normalt slås på under epikardiell aktivering och som svar på TGFβ‑signalering var nedtonade, vilket pekar på Fbln2 som en ställskruv i denna väg som avgör hur starkt epikardiet engagerar sig i att bilda och omforma ärrvävnad.
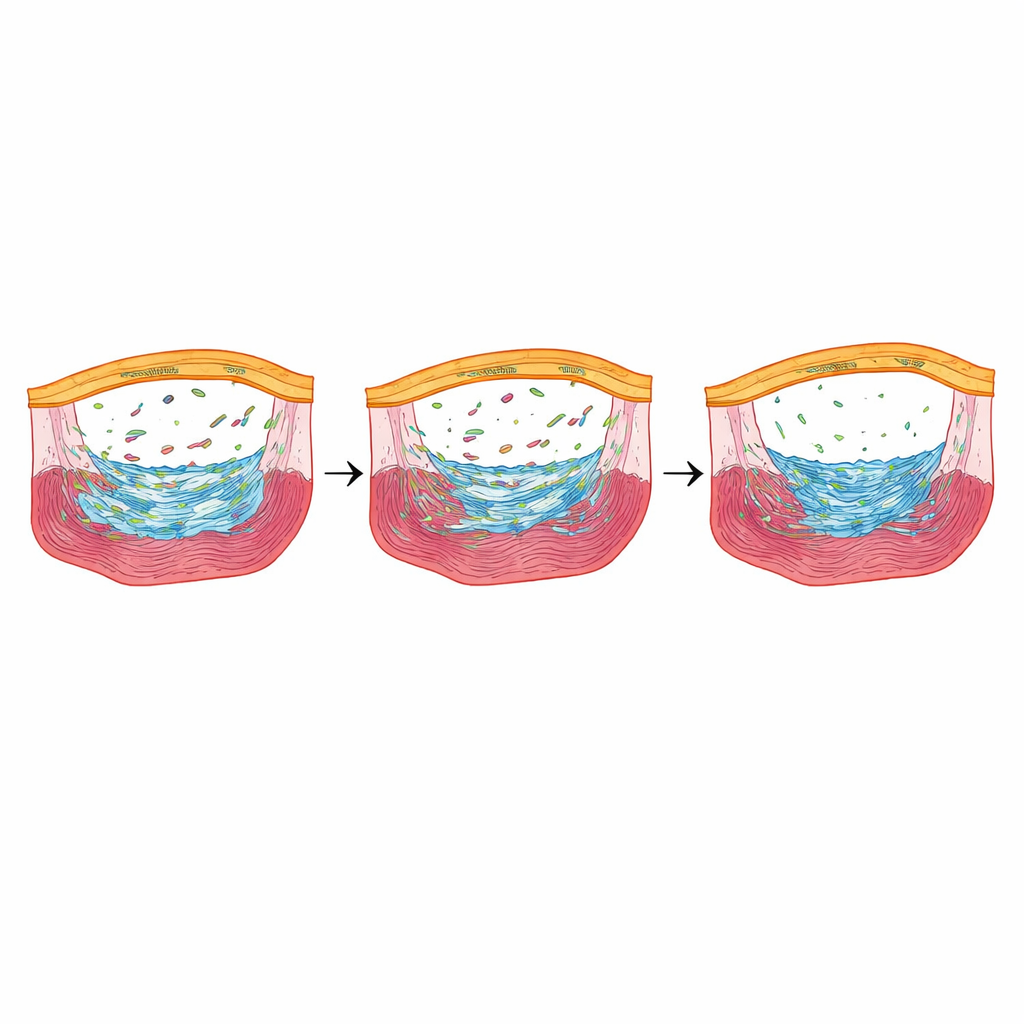
En stressresponder som finslipar reparationen
Bland de gener som skarpt reducerades när Fbln2 sänktes utmärkte sig en: nupr1b, en stressresponsregulator aktiv i epikardiella celler under tidig läkning. När forskarna raderade nupr1b visade zebrafiskarna färre epikardiella ärrbildande celler och minskad hjärtmuskelcelldelning, och de behöll stora kollagendepositioner månader efter skadan—mycket likt fisk som helt saknade Fbln2. Slående nog, när de kortvarigt tvingade på nupr1b igen endast i epikardiella celler hos Fbln2‑reducerade fisk återhämtade sig antalet ärrbildande celler och proliferation av hjärtmuskelceller, och sen ärrbildning ökade. Blockering av TGFβ‑receptorer kemiskt sänkte nupr1b‑nivåerna, vilket placerar nupr1b nedströms i en Fbln2–TGFβ‑signalaxel.
Vad detta betyder för att läka mänskliga hjärtan
Tillsammans visar dessa fynd en "epikardiell Fbln2–Nupr1b‑axel" som hjälper zebrafiskhjärtan att balansera mellan för lite och för mycket fibros. Att dämpa denna axel något lugnar den tidiga ärrbrytningen och uppmuntrar effektiv ärrborttagning, medan att stänga av den helt spårar ur regenereringen och lämnar ett stelt ärr efter sig. För humanmedicin är lärdomen att målet inte är att helt blockera ärrbildning, utan att ställa in den—behålla tillräcklig struktur för att förhindra ruptur samtidigt som ärrvävnad är tillfällig och kan ersättas av frisk muskel. Att förstå och så småningom utnyttja detta kontrollsystem från zebrafiskar skulle kunna informera framtida terapier som får det skadade mänskliga hjärtat att gå mot verklig regenerering istället för kronisk ärrbildning.
Citering: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
Nyckelord: hjärtregenerering, fibros, zebrafisk, epikardium, TGF-beta-signalering