Clear Sky Science · sv
Selektiv blockering av latent TGF-β1-aktivering dämpar vävnadsfibros med god säkerhet
Varför dold ärrbildning spelar roll
Många kroniska sjukdomar skadar våra organ i tysthet genom att lägga ner stel ärrvävnad, en process som kallas fibros. Denna ärrbildning kan långsamt kväva normal funktion i levern, njurarna, lungorna och även runt tumörer, där den dessutom kan dämpa effekten av moderna cancerimmunterapier. Proteinet TGF-β1 står i centrum för denna ärrbildningsprocess, men att stänga av det överallt i kroppen har visat sig vara farligt. Den här studien beskriver en ny antikropp, kallad SOF10, designad för att blockera enbart den skadliga aktiveringen av TGF-β1 samtidigt som dess viktiga funktioner bevaras, och visar lovande effekter i djurmodeller för leversjukdom, njursvikt och cancer.
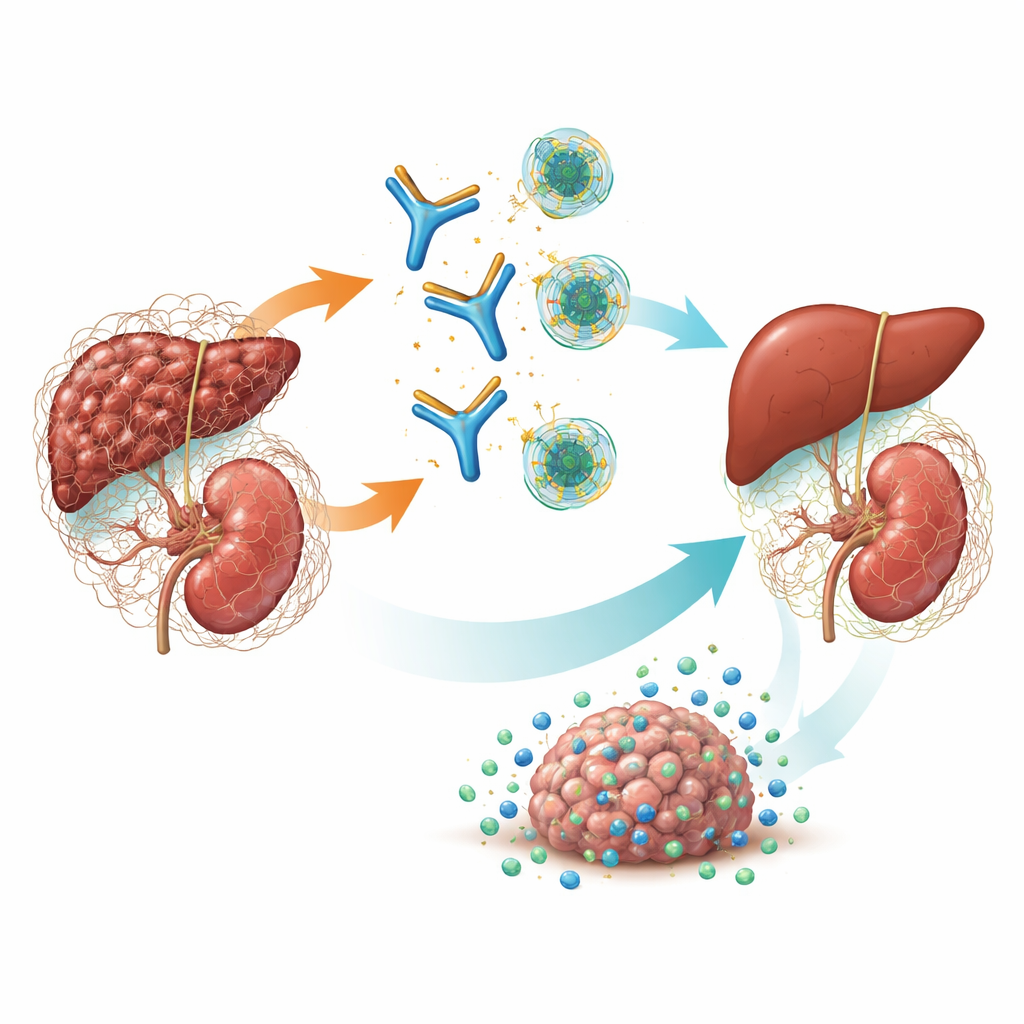
En huvudbrytare för ärrbildning och cancer
TGF-β är ett kraftfullt signalsubstans som hjälper till att styra hur celler växer, läker och interagerar med immunsystemet. Vid kronisk sjukdom driver en form—TGF-β1—fibroblaster att bygga överflödig bindväv, vilket leder till organstelhet och svikt. Den formar också en immunsuppressiv, fibrotisk kapsel runt tumörer som hindrar immunceller och läkemedel från att nå cancercellerna. Tidigare läkemedel försökte stänga av alla tre TGF-β-formerna samtidigt, men denna ”pan-blockad” orsakade allvarliga biverkningar såsom skador på hjärtklaffar, blödningar och hudtumörer. Genetiska studier och tidigare modeller föreslog att TGF-β1 är huvudorsaken vid fibrotisk njursjukdom och många solida tumörer, vilket öppnade möjligheten att noggrant rikta in sig på endast denna isoform skulle kunna vara både effektivt och säkrare.
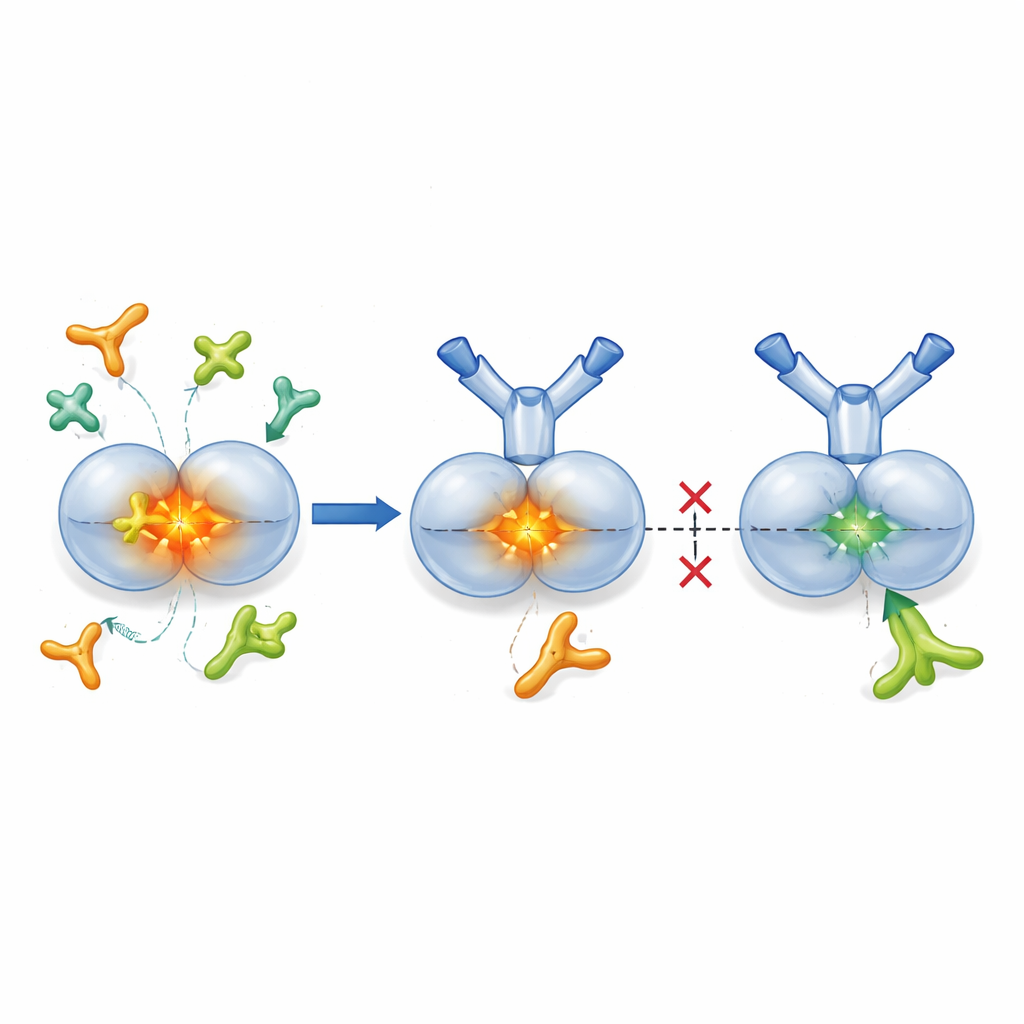
Låsning av TGF-β1 i dess inaktiva form
TGF-β1 produceras normalt i ett ”latent” paket, där den aktiva kärnan är omsluten av ett partnerprotein som håller den avstängd tills den behövs. Enzymer kallade proteaser och vissa cellytans fästande proteiner, så kallade integriner, kan öppna detta paket och frigöra aktiv TGF-β1 till närliggande vävnad. Forskarna konstruerade SOF10, en humaniserad antikropp som binder endast till den latenta formen av TGF-β1, inte till det aktiva hormonet eller andra isoformer. Strukturella studier med röntgenkristallografi visade att SOF10 kilas in i gränssnittet mellan de två halvorna av den latenta komplexet och stabiliserar det som en klämma. I laboratorietester förhindrade detta att proteaser och en integrin (αvβ8) frigjorde aktiv TGF-β1, samtidigt som en annan integrin (αvβ6)—viktig för att upprätthålla immunbalans i friska vävnader—i stort sett lämnades orörd. I praktiken tystar SOF10 selektivt de skadliga aktiveringsvägarna samtidigt som en nyckel för homeostas sparas.
Skydd av lever och njurar från långsam skada
För att se om detta selektiva klämgrepp på TGF-β1 verkligen kunde begränsa ärrbildning testade teamet SOF10 i flera musmodeller. I en snabb dietinducerad modell av fettlever som utvecklas till leverskleros minskade SOF10-behandling leverns uttryck av TGF-β–responsiva gener och kollagenbyggande gener, och den sänkte hydroxyprolin, en kemisk markör för ackumulerad ärrvävnad. I två olika njurmodeller—en kirurgisk obstruktionsmodell som driver interstitiell fibros och en genetisk modell av Alports syndrom som utvecklar både glomerulär ärrbildning och njursvikt—minskade SOF10 den fibrotiska genaktiviteten, reducerade kollageninnehållet och krympte synligt ärrade områden under mikroskopet. I den kroniska Alport-modellen visade blodprover förbättrad njurfunktion, och dessa fördelar stod sig jämförda med en bredare TGF-β–blockerande antikropp, men utan att blockera andra TGF-β-isoformer.
Frigöra immunsystemet inne i tumörer
Eftersom fibrotisk vävnad runt tumörer kan fungera både som en fysisk barriär och ett immunhämmande moment, undersökte forskarna om SOF10 kunde förbättra svaren på checkpoint-hämmarläkemedel. I musmodeller för bröst- och koloncancer som normalt svarar dåligt på anti–PD-L1-terapi bromsade tillägg av SOF10 tumörtillväxten signifikant, medan vare sig SOF10 eller anti–PD-L1 ensamma hade större effekt. Tumörer från kombinationsbehandlade djur innehöll fler mördande CD8-T-celler och mer av de toxiska enzymer de använder för att förstöra cancerceller. Fibroblaster tagna från dessa tumörer visade lägre aktivitet i kollagen- och matrixbyggande vägar men högre aktivitet i interferon- och antigenpresentationsvägar—en förskjutning mot ett mer immunsupportivt stroma. Dessa förändringar speglade nära vad som setts med bred TGF-β-blockad, vilket tyder på att riktning mot latent TGF-β1 ensam kan omprogrammera tumörmiljön på ett liknande sätt.
Säkerhetssignaler i djur
Eftersom tidigare försök att brett blockera TGF-β stött på säkerhetsproblem genomförde teamet 13-veckors toxicitetsstudier i möss och cynomolgus-apor, och gav upprepade höga doser av SOF10. Läkemedlet uppträdde som en typisk antikropp i blodomloppet, och över ett brett dosintervall fanns inga tecken på skador i stora organ, blodbild eller hjärt- och lungfunktion. De högsta testade doserna—upp till 200 mg/kg varannan vecka i möss och 100 mg/kg i apor—utsågs till nivåer utan observerbara skadliga effekter. Denna säkerhetsprofil stöder idén att sparande av TGF-β2, TGF-β3 och αvβ6-medierad aktivering minskar riskerna som sågs med tidigare, mindre selektiva tillvägagångssätt.
Vad detta kan betyda för patienter
Tillsammans tyder fynden på att låsning av TGF-β1 i dess inaktiva skal—hellre än att utplåna all TGF-β-signalering—kan lindra ärrbildning i flera organ, förbättra njurfunktionen och göra envisa tumörer mer sårbara för immunoterapi, allt med uppmuntrande säkerhet i djurtester. Även om mänskliga prövningar behövs för att bekräfta dessa fördelar och övervaka långtidseffekter kan SOF10 och liknande strategier öppna en ny väg för att behandla kroniska fibrotiska sjukdomar och vissa cancerformer, genom att dämpa skadlig ärrbildning samtidigt som vävnadernas läknings- och immunbalanserande roller bevaras.
Citering: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
Nyckelord: fibros, TGF-beta1, monoklonant antikropp, njure- och leversjukdom, cancerimmunoterapi