Clear Sky Science · sv
Genomisk karaktärisering och sub-klustring av Escherichia coli klonkomplex 38 avslöjar värdtillhöriga genetiska markörer
Varför detta spelar roll i vardagen
Antibiotikaresistenta infektioner är inte längre en avlägsen sjukhusfråga—de berör i allt högre grad mat, djur, resor och samhällsliv. Denna studie fokuserar på en särskild grupp Escherichia coli-bakterier, kallad klonkomplex 38 (CC38), som kan orsaka allvarliga blod- och urinvägsinfektioner och ofta står emot våra viktigaste antibiotika. Genom att spåra var dessa bakterier kommer ifrån och hur de rör sig mellan människor, djur och miljö, avslöjar forskarna ledtrådar som kan hjälpa myndigheter att stoppa farliga stammar innan de sprider sig brett.
En närmare titt på en besvärlig bakteriefamilj
Alla E. coli är inte skadliga, men vissa linjer är återfallsförövare i svår sjukdom. CC38 har nyligen framträtt som en av dessa problematiska grupper, endast efterhängande en välkänd högrisklinje (ST131) vid danska blodinfektioner. Teamet undersökte 242 resistenta E. coli CC38 från danska patienter, 83 från livsmedel och lantbruksdjur samt mer än 2 300 närbesläktade genom samlade världen över. De använde helgenomsekvensering—i praktiken att läsa varje bakteries DNA—för att kartlägga hur olika grenar av denna familj hänger ihop, vilka resistensgener de bär och vilka värdar de tenderar att förekomma i.
Följ spåren från sjukhus till gårdar och mat
När forskarna jämförde E. coli CC38 från danska patienter med de från fjäderfä, boskap och livsmedel fann de två huvudsakliga danska grupper. Den ena gruppen bestod mestadels av mänskliga infektioner, medan den andra innehöll bakterier från fjäderfä, andra lantbruksdjur och livsmedelsprodukter. Viktigt är att det inte fanns några nära identifierbara DNA‑matchningar mellan humana och animaliska isolat, vilket tyder på att det inte förekom några tydliga matburna utbrott i Danmark under studieperioden. Dock indikerade statistiska modeller som analyserar accessoriska DNA‑segment att vissa människobundna undergrupper sannolikt har ursprung i fjäderfä, vilket antyder tidigare eller indirekta överföringar från kycklingar till människor.
En global släktträd med två stora grenar
Genom att utvidga till en global datamängd med 2 638 genom byggde teamet ett globalt ”släktträd” för CC38. Två större grenar framträdde. Den ena var starkt knuten till fjäderfä och bar måttliga nivåer av läkemedelsresistens tillsammans med många egenskaper kopplade till allvarlig sjukdom. Den andra dominerades av människobundna undergrupper som skilde sig åt i resistens, sjukdomspotential och föredragna värdar. Några undergrupper var tydligt människoorienterade och starkt resistenta, medan andra visade blandade mönster och återfanns hos människor, fjäderfä, vilda djur, vatten och sällskapsdjur. Detta lapptäcke återspeglar CC38:s förmåga att anpassa sig till olika miljöer och värdarter, vilket komplicerar insatser för att kontrollera den.
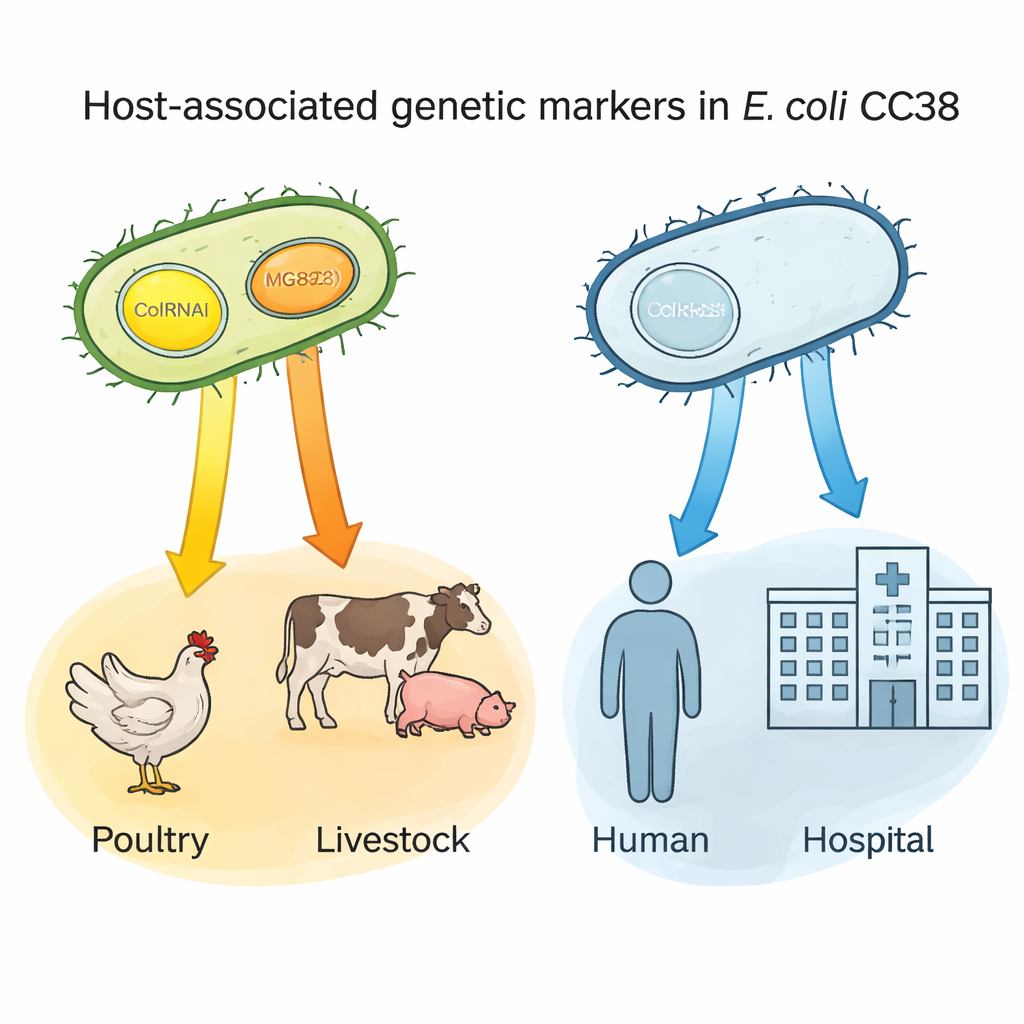
Små DNA‑cirklar som värdarnas ”namnskyltar”
En viktig upptäckt rörde två små DNA‑stycken—plasmider kallade ColRNAI och Col(MG828)—som kan röra sig mellan bakterier. Dessa plasmider var vanliga i CC38 från fjäderfä och andra lantbruksdjur men sällsynta i de människocentrerade undergrupperna. Med statistisk analys visade författarna att bärande av endera plasmiden starkt förutsade ett ursprung i fjäderfä; att bära båda tillsammans var särskilt karaktäristiskt för linjer kopplade till boskap och vissa livsmedelskällor. Eftersom dessa plasmider ofta också bär resistensegenskaper kan de fungera som genetiska ”namnskyltar” som markerar bakterier som sannolikt kommer från animaliska reservoarer och kan hjälpa till att spåra hur resistenta stammar kommer in i livsmedelskedjan och når människor.
Vad detta betyder för att skydda hälsan
För en icke‑specialist är huvudbudskapet att skadliga, läkemedelsresistenta E. coli inte är begränsade till sjukhus eller patienter: de bildar sammankopplade populationer som sträcker sig över människor, fjäderfä, boskap, vilda djur, livsmedel och miljö. Denna studie visar att inom en viktig linje, CC38, är vissa grenar starkt knutna till djur och andra till människor, och att specifika mobila DNA‑element kan hjälpa till att avslöja var en stam sannolikt härstammar från. Att använda dessa genetiska markörer i rutinmässig övervakning skulle kunna ge tidiga varningssignaler när djurbundna resistenta bakterier börjar dyka upp hos människor. I sin tur stöder detta ett ”One Health”-ansats—att betrakta mänsklig, animalisk och miljömässig hälsa som delar av samma system—för att utforma smartare, riktade strategier för att förebygga infektioner och bromsa spridningen av antibiotikaresistens.
Citering: Roer, L., Rasmussen, A., Hansen, F. et al. Genomic characterization and sub-clustering of Escherichia coli clonal complex 38 reveal host associated genetic markers. Commun Med 6, 126 (2026). https://doi.org/10.1038/s43856-026-01402-2
Nyckelord: antimikrobiell resistens, Escherichia coli, zoonotisk överföring, fjäderfä och boskap, genomisk övervakning