Clear Sky Science · sv
Prognos av utfall från rumslig proteinprofilering av trippelnegativa bröstcancer
Varför cancercellernas layout spelar roll
När läkare tittar på en aggressiv bröstcancer i mikroskop ser de ett tätt landskap av tumörceller, immunceller och stödjevävnad. Men fram till nyligen har de flesta tester fokuserat på hur mycket av en viss molekyl som finns, inte var den är belägen. Denna studie visar att den fysiska ordningen av proteiner och celler i trippelnegativa bröstcancer kan förutsäga patienternas utfall och introducerar ett nytt sätt att läsa av dessa rumsliga mönster direkt från högupplösta bilder.
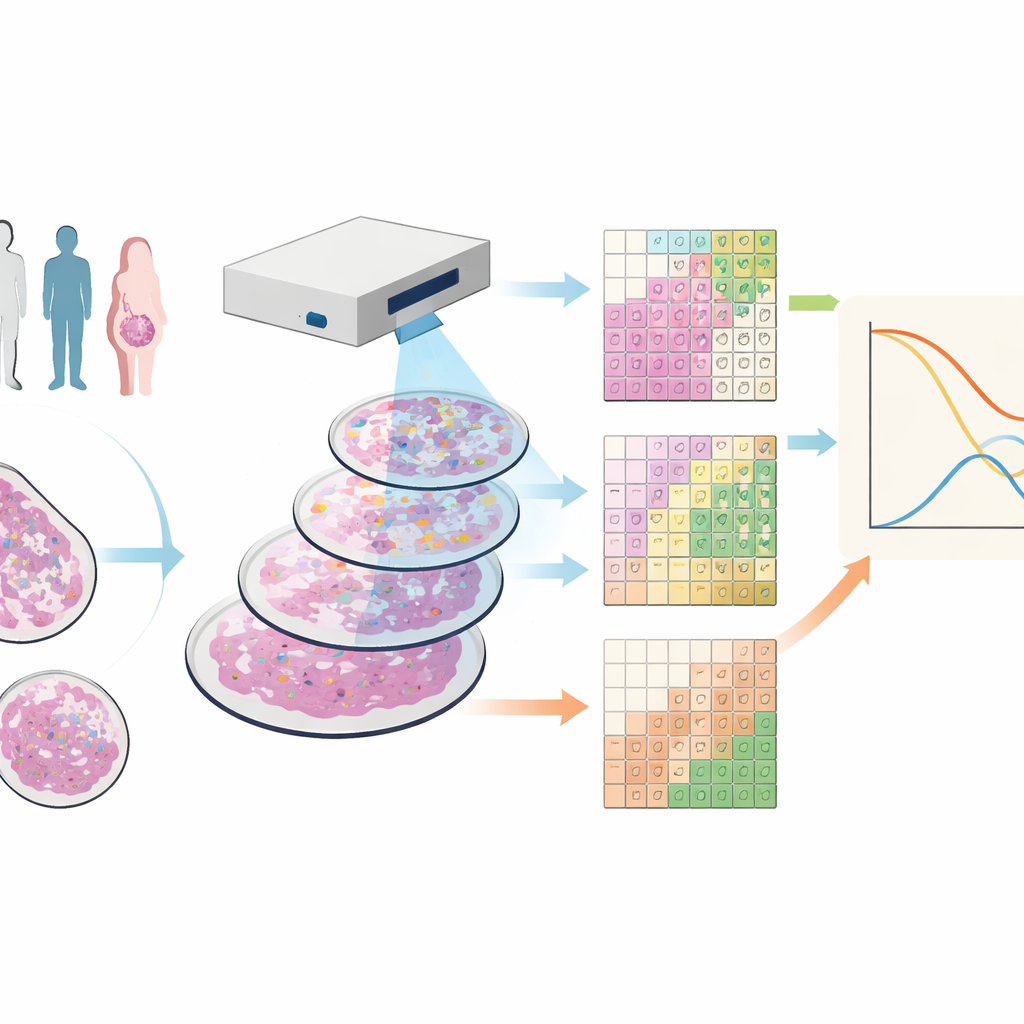
Att se cancervävnad i många färger
Forskarna arbetade med vävnadsprover från 88 personer med trippelnegativ bröstcancer, en form av sjukdomen som saknar vanliga läkemedelsmål och ofta har dålig prognos. De använde en teknik kallad avbildande masscytometri, som färgar varje prov med dussintals metalltaggade antikroppar. Under en specialiserad skanner ger detta bilder där varje punkt i vävnaden har ett detaljerat fingeravtryck av många olika proteiner, vilket avslöjar tumörceller, olika immunceller, blodkärl och strukturella fibrer på en gång.
Att dela bilden i rutor istället för celler
De flesta nuvarande verktyg försöker rita gränser runt varje cell och därefter klassificera dem efter typ, en process som kan vara felbenägen och långsam, särskilt i tunna vävnadsskivor där celler bara delvis fångas upp. Teamet skapade istället SparTile, en metod som hoppar över att rita individuella cellkonturer. SparTile delar varje bild i många små överlappande fyrkanter, eller tiles, och använder matematiska tekniker för att lära sig återkommande mönster av proteinkombinationer inom dessa tiles. Först grupperar den tiles till breda regioner—tumör, stödjevävnad (stroma) eller immunrika zoner—och delar sedan varje region i mer specifika ”mikromiljöer”, var och en med sin egen blandning av proteiner och närliggande celltyper.
Dolda kvarter kopplade till patientutfall
Med dessa mikromiljöer kartlagda mätte forskarna hur mycket av varje mönster som förekom i varje patients prov och jämförde detta med långsiktig överlevnad. Flera påfallande samband framträdde. En tumörcentrerad mikromiljö rik på ett protein kallat MX1 och markörer för myeloida immunceller var kopplad till en avsevärt högre dödsrisk. Ett annat tumörmönster markerat av vimentin—ett tecken på att tumörceller har skiftat mot ett mer rörligt, invasivt tillstånd—korrelerade också starkt med dålig överlevnad. Däremot var områden dominerade av vissa T‑celler kopplade till bättre utfall, medan B‑cellsrika regioner visade svagare effekter, möjligen eftersom de var sällsynta i de små vävnadskärnorna som analyserades.
Avståndet mellan tumör- och immunceller som varningstecken
Bortom förekomsten av särskilda kvarter spelade deras rumsliga relationer också roll. Teamet undersökte hur nära tumörregioner och myeloida immunsregioner låg varandra genom att beräkna en statistisk mått på hur mycket deras proteinsignaler överlappade i rummet. Patienter vars tumörer hade myeloidrika områden insprängda tätt bland tumörceller tenderade att få sämre utfall än de där de två populationerna var mer åtskilda. Detta ”avståndsmått” förblev en stark riskprediktor även efter att vanliga kliniska faktorer beaktats, och dess betydelse höll i sig när metoden testades på två oberoende bröstcancerbildsdatamängder från andra forskargrupper.
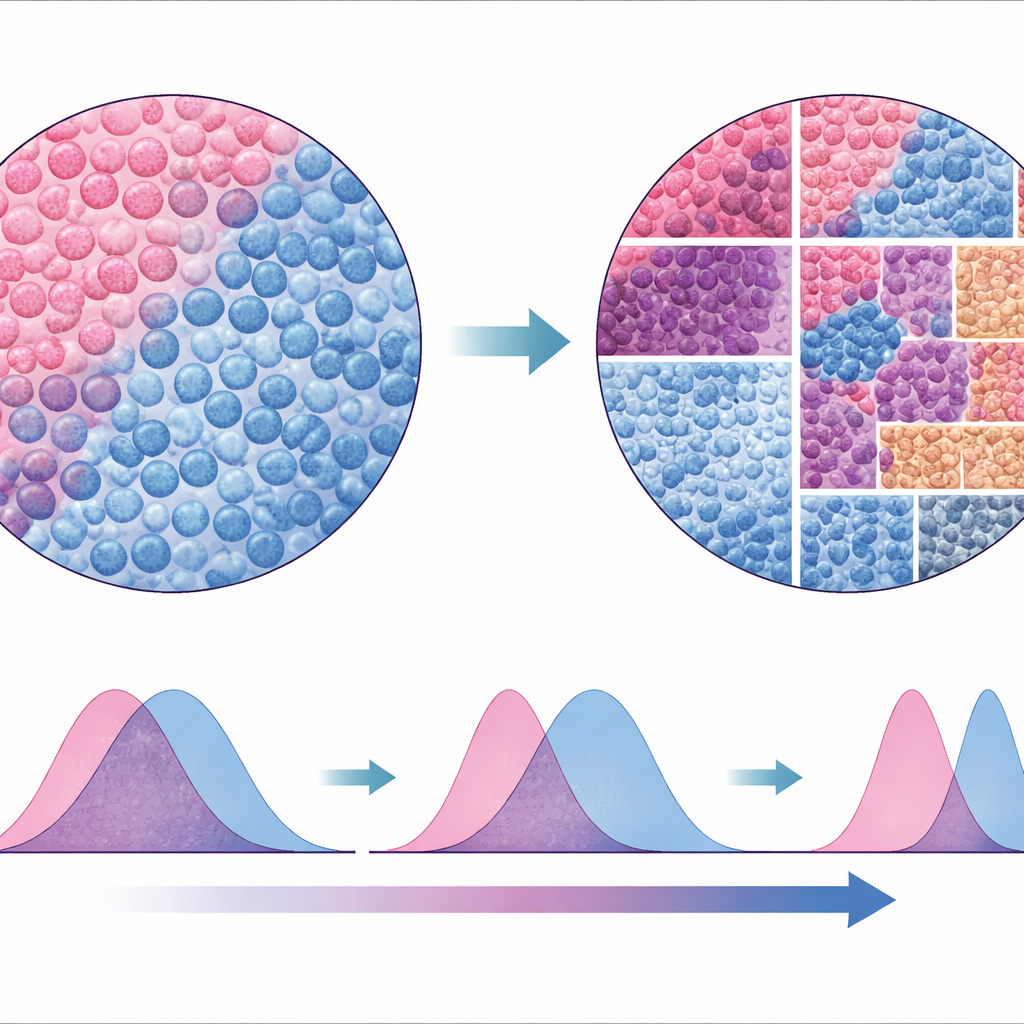
Ett nytt sätt att läsa tumörlandskapet
För att testa hur robust deras tillvägagångssätt var jämförde författarna SparTile med traditionella metoder som bygger på segmentering och klassificering av individuella celler och därefter konstruktion av kvarter kring dem. Medan cellbaserade analyser återfann några av samma mönster var de mindre konsekventa över datamängder och mindre tillförlitliga för att flagga vissa riskfyllda mikromiljöer, såsom de som involverade MX1 och myeloida celler. Eftersom SparTile arbetar direkt på de råa proteinbilderna undviker det många av antagandena och tekniska fallgroparna i cell‑för‑cell‑metoder, men det kan ändå kombineras med dem senare när detaljerade celltyper behövs för att planera experiment eller terapier.
Vad detta innebär för patienter och framtida vård
Detta arbete visar att det inte bara är ingredienserna utan även tumörens layout som spelar roll för att förutsäga hur en patient med trippelnegativ bröstcancer kommer att klara sig. Genom att omvandla komplexa, multiproteinbilder till tolkningsbara rumsliga mönster och enkla avståndsmått erbjuder SparTile ett sätt att identifiera hög‑riskpatienter från små vävnadsprov och att avslöja biologiska arrangemang som kan riktas av framtida behandlingar. Medan mer validering krävs innan metoden kan vägleda rutinvård pekar den mot en framtid där en tumörs ”karta” blir lika viktig som dess molekylära innehållsförteckning.
Citering: Foroughi pour, A., Wu, TC., Noorbakhsh, J. et al. Prediction of outcome from spatial Protein profiling of triple-negative breast cancers. Commun Med 6, 133 (2026). https://doi.org/10.1038/s43856-026-01400-4
Nyckelord: trippelnegativ bröstcancer, tumörmikromiljö, rumslig proteomik, avbildande masscytometri, prognostiska biomarkörer