Clear Sky Science · sv
IdentifiHR förutspår brist i homolog rekombination hos höggradig serös ovarialkarcinom med hjälp av genuttryck
Varför denna forskning är viktig för patienter med äggstockscancer
För personer med höggradig serös äggstockscancer, en av de dödligaste formerna av sjukdomen, kan behandlingsval vara livsavgörande. Ungefär hälften av dessa tumörer har en svaghet i hur de reparerar skadat DNA, vilket gör dem särskilt känsliga för vissa läkemedel som kallas PARP-hämmare. Utmaningen är att avgöra för varje patient om tumören har denna svaghet. Denna studie presenterar IdentifiHR, ett nytt verktyg som läser av mönster i genaktivitet — snarare än enbart DNA-mutationer — för att förutsäga vilka tumörer som har defekt DNA-reparation och därmed kan gynnas mest av dessa riktade behandlingar.
Från DNA-ärr till genaktivitetsmönster
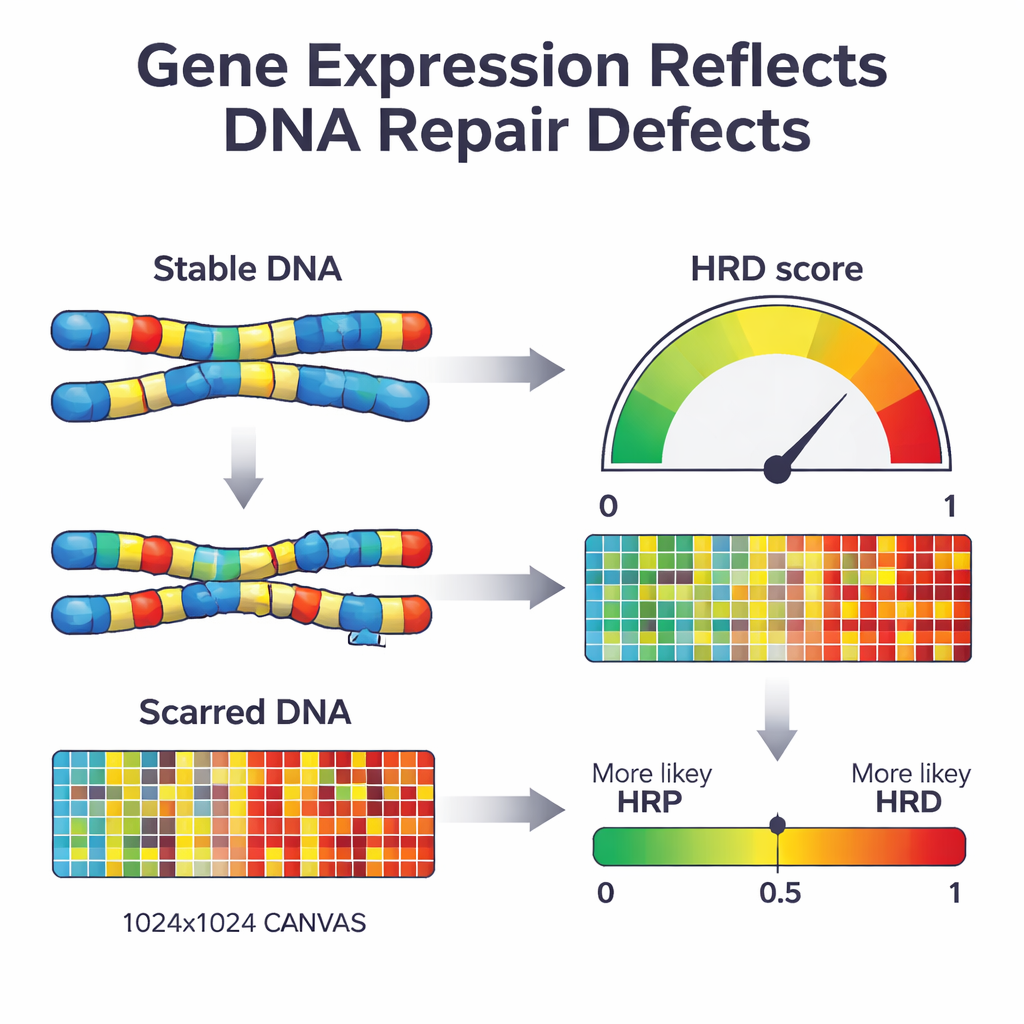
När en cell förlorar en viktig reparationsväg som homolog rekombination börjar den lappa ihop sitt DNA med mer felbenägna metoder. Med tiden lämnar detta ett karakteristiskt mönster av ”ärr” i genomet — förlorade regioner, extra kopior och brutna kromosomsegment. Befintliga kliniska tester söker efter dessa ärr direkt i DNA:t eller efter specifika mutationer i nyckelgener som BRCA1 och BRCA2. Även om dessa tester är kraftfulla kräver de omfattande DNA-sekvensering och fångar inte alltid tumörens aktuella reparationsstatus. Författarna undrade om en annan nivå av biologin — vilka gener som är på- eller avstängda i tumören — skulle kunna fungera som en levande avläsning av denna skada och användas för att klassificera tumörer som reparationsdefekt eller reparationskompetent.
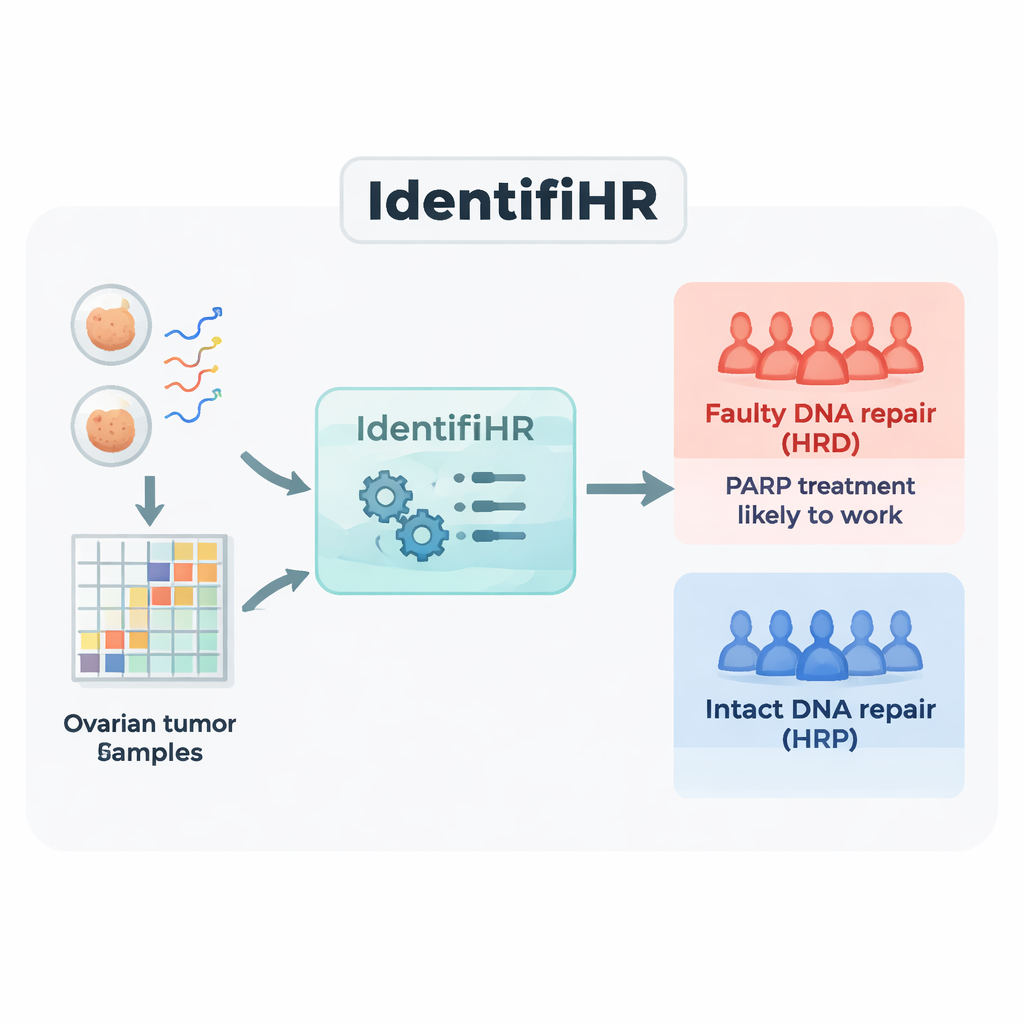
Att bygga en genbaserad prediktor, IdentifiHR
Gruppen började med RNA-sekvenseringsdata från 361 ovarialtumörer i en stor publik resurs, The Cancer Genome Atlas. RNA-sekvensering mäter vilka gener som är aktiva, och i vilken omfattning, i varje prov. De delade upp tumörerna i en träningsgrupp och en testgrupp och märkte varje fall som antingen reparationsdefekt (HRD) eller reparationskompetent (HRP) med hjälp av nuvarande DNA-baserade standard som kombinerar flera mått på genomiska ärr. I träningssetet identifierade de 2 604 gener vars aktivitet konsekvent skilde sig mellan HRD- och HRP-cancer. Många av dessa gener låg i genomområden som redan är kända för att upprepade gånger förloras eller ökas i reparationsdefekta tumörer, vilket visar att signalen i genaktivitet speglade det underliggande DNA-slättet.
Ett 209-geners signatur som följer reparationsstatus
Därefter använde forskarna ett maskininlärningsförfarande känt som straffad logistisk regression för att komprimera listan på 2 604 gener till den mest informativa uppsättningen. Den resulterande modellen, som de kallade IdentifiHR, förlitar sig på aktiviteten hos endast 209 gener för att uppskatta sannolikheten att en tumör är reparationsdefekt. Intressant nog är endast en av dessa gener en klassisk DNA-reparationsgen; de flesta är vanliga gener vars aktivitet förändrats på grund av bredare förändringar i kromosomstrukturen. IdentifiHR ger inte bara ett ja-eller-nej-svar — den producerar en sannolikhetspoäng som följer smidigt med det underliggande DNA-baserade skademåttet, vilket speglar idén att reparationsbrist existerar på ett spektrum snarare än som ett strikt av-/på-tillstånd.
Testning av verktyget i flera patientkohorter
Författarna testade noggrant IdentifiHR i tre oberoende dataset som aldrig använts i träningen. I den utsläppta delmängden av The Cancer Genome Atlas skilde modellen korrekt HRD från HRP-tumörer i ungefär 85 % av fallen. Den presterade lika bra — runt 86 % noggrannhet — i en separat australiensisk studie som inkluderade inte bara primära tumörer utan också prover tagna vid obduktion, från vätska i buken (ascites) och från normala äggledare, den troliga plats där många av dessa cancerformer börjar. I varje normalt prov från äggledaren förutspådde IdentifiHR korrekt intakt DNA-reparation. Verktyget fungerade också på "pseudobulkade" single-cell-data, där tusentals enskilda cancerceller kombinerades datoriserat för att efterlikna ett bulkprov, och uppnådde återigen ungefär 84 % noggrannhet. I dessa tester motsvarade eller överträffade IdentifiHR prestandan hos flera befintliga genbaserade metoder som ursprungligen utvecklats för andra cancerformer eller för att förutsäga relaterade skademått.
Hur detta kan förändra forskning och vård
Eftersom IdentifiHR körs på RNA-data, som ofta är billigare och enklare att samla in än helgenomssekvensering av DNA, erbjuder det ett praktiskt sätt för forskare — och potentiellt, i framtiden, kliniker — att uppskatta DNA-reparationsstatus när endast genuttrycksdata finns tillgängliga. Modellen släpps som ett öppen källkods R-paket, så varje grupp med lämpliga sekvenseringsdata kan använda den. Även om den ännu inte ersätter guldsstandard-DNA-tester, och dess förmåga att fånga mer subtila förändringar såsom återställning av reparation fortfarande behöver studeras, ger IdentifiHR ett kraftfullt nytt perspektiv på vilka ovarialtumörer som mest sannolikt svarar på PARP-hämmare och liknande läkemedel. För patienter förflyttar denna typ av arbete fältet närmare mer precisa, biologidrivna behandlingsbeslut anpassade efter hur deras cancerceller faktiskt beter sig.
Citering: Weir, A.L., Lee, S.C., Li, M. et al. IdentifiHR predicts homologous recombination deficiency in high-grade serous ovarian carcinoma using gene expression. Commun Med 6, 119 (2026). https://doi.org/10.1038/s43856-026-01387-y
Nyckelord: äggstockscancer, DNA-reparation, homolog rekombinationsbrist, genuttryck, maskininlärning