Clear Sky Science · sv
Brister i homolog rekombination vid primär ER‑positiv och HER2‑negativ bröstcancer
Varför detta är viktigt för bröstcancerpatienter
De flesta bröstcancrar tillhör en stor grupp som kallas östrogenreceptor‑positiva och HER2‑negativa. Dessa tumörer behandlas vanligtvis med hormonhämmande läkemedel, ibland i kombination med cytostatika. Ändå återfaller många patienter, och läkare saknar precisa verktyg för att avgöra vem som verkligen behöver intensiv behandling eller kan gynnas av nya målinriktade läkemedel. Denna studie undersöker en särskild sårbarhet i vissa tumörer — kallad defekt i homolog rekombination, eller HRD — som gör att cancerceller är dåliga på att reparera brutet DNA, och som potentiellt öppnar för mer individualiserad behandling.
En dold svaghet i bara vissa tumörer
Homolog rekombination är ett av cellens huvudsystem för att laga farliga DNA‑brott. När detta system sviktar — ofta på grund av fel i välkända gener som BRCA1, BRCA2, PALB2 eller RAD51C — ansamlas mutationer i cellerna och de kan bli särskilt känsliga för vissa läkemedel, inklusive platinumbaserad cytostatika och PARP‑hämmare. HRD är vanligt i en aggressiv form av bröstcancer som kallas trippelnegativ, men dess roll i den vanligare östrogenreceptorpositiva, HER2‑negativa gruppen har varit osäker. För att klargöra detta analyserade forskarna 502 sådana tumörer från den svenska SCAN‑B‑studien med helgenomssekvensering, tillsammans med matchande data om genaktivitet, DNA‑metylering, givna behandlingar och långsiktiga utfall.
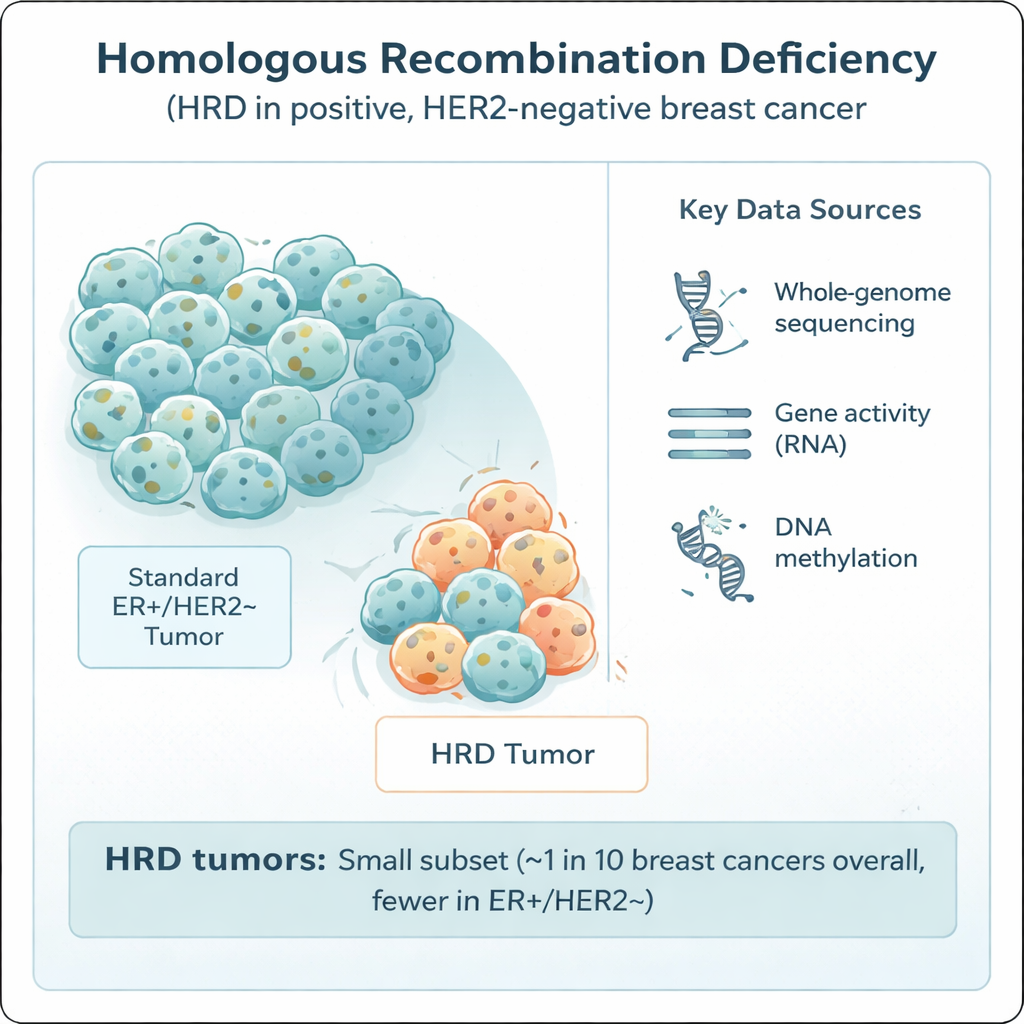
Hur studien genomfördes
Alla tumörer togs bort vid kirurgi, före någon läkemedelsbehandling, vilket ger en tydlig bild av deras ursprungliga biologi. Teamet använde ett sofistikerat mönsterigenkänningsverktyg, HRDetect, för att läsa av de ”mutationssignaturer” som lämnas i cancer‑DNA när homolog rekombination är skadad. Tumörer klassificerades som HRD om de översteg en strikt sannolikhetströskel. Forskarna jämförde också olika sätt att upptäcka HRD — från andra DNA‑baserade poängsystem till ett RNA‑baserat genuttryckstest — för att se hur väl olika metoder överensstämmer. Dessutom undersökte de bredare egenskaper som den totala mutationsbördan, mönster av kromosomala vinster och förluster, immunsystemrelaterad genaktivitet samt kemiska markörer på DNA (metylering) som kan slå av eller på gener.
Hur vanligt är HRD, och vad orsakar det?
Forskarna fann att bara 8,4 % av de östrogenreceptorpositiva, HER2‑negativa tumörerna i deras sekvenserade grupp visade starkt stöd för HRD — långt under de ungefär 60 % som ses i trippelnegativ sjukdom. Genom att kombinera dessa data med nationella registeruppgifter och andra studier uppskattade de att omkring 1 av 20 tumörer i denna kliniska undergrupp, och ungefär 1 av 9 bröstcancerfall totalt i Västeuropéiska/Nordiska populationer, är HRD. I de HRD‑tumörer de kunde ofta peka ut en sannolik orsak: cirka 70 % hade tydlig påverkan på BRCA1, BRCA2, RAD51C eller PALB2, genom ärftliga mutationer, tumörspecifika mutationer eller deletioner, eller epigenetisk tystnad av genpromotorer. Slående nog berodde omkring en tredjedel av HRD‑fallen på promotorhypermetylering — ett extra kemiskt lager som slår av DNA‑reparationsgener utan att ändra deras sekvens. Dock visade ungefär 30 % av HRD‑tumörerna ingen uppenbar enstaka förklaring, vilket tyder på ytterligare, ännu oupptäckta vägar till denna reparationsbrist.
Hur HRD‑tumörer ser ut i mikroskopet och i kliniken
HRD‑tumörer i denna vanliga bröstcancergrupp tenderade att uppvisa kännetecken för mer aggressiv sjukdom: de hade ofta högre celldelningstakt, lägre nivåer av hormonreceptorfärgning och mer komplexa, mutationsrika genom jämfört med HR‑kompetenta tumörer. De förekom i nästan alla större molekylära subtyper, men var sällsynta i den mer långsamt växande Luminal A‑klassen och relativt förhöjda i en mindre basal‑liknande undergrupp. När forskarna tittade på övergripande genaktivitet och DNA‑metyleringsmönster föll HRD‑tumörerna dock inte in i en enda lättigenkännlig profil. Istället var deras uttrycksmönster varierande och eventuella skillnader inom specifika subtyper var blygsamma. Vissa HRD‑tumörer, särskilt i Luminal B‑ och basal‑liknande grupperna, visade högre tecken på immunsvar och ökat uttryck av PD‑L1, vilket antyder att de kan vara mer synliga för immunsystemet och potentiellt mer mottagliga för immunterapi.
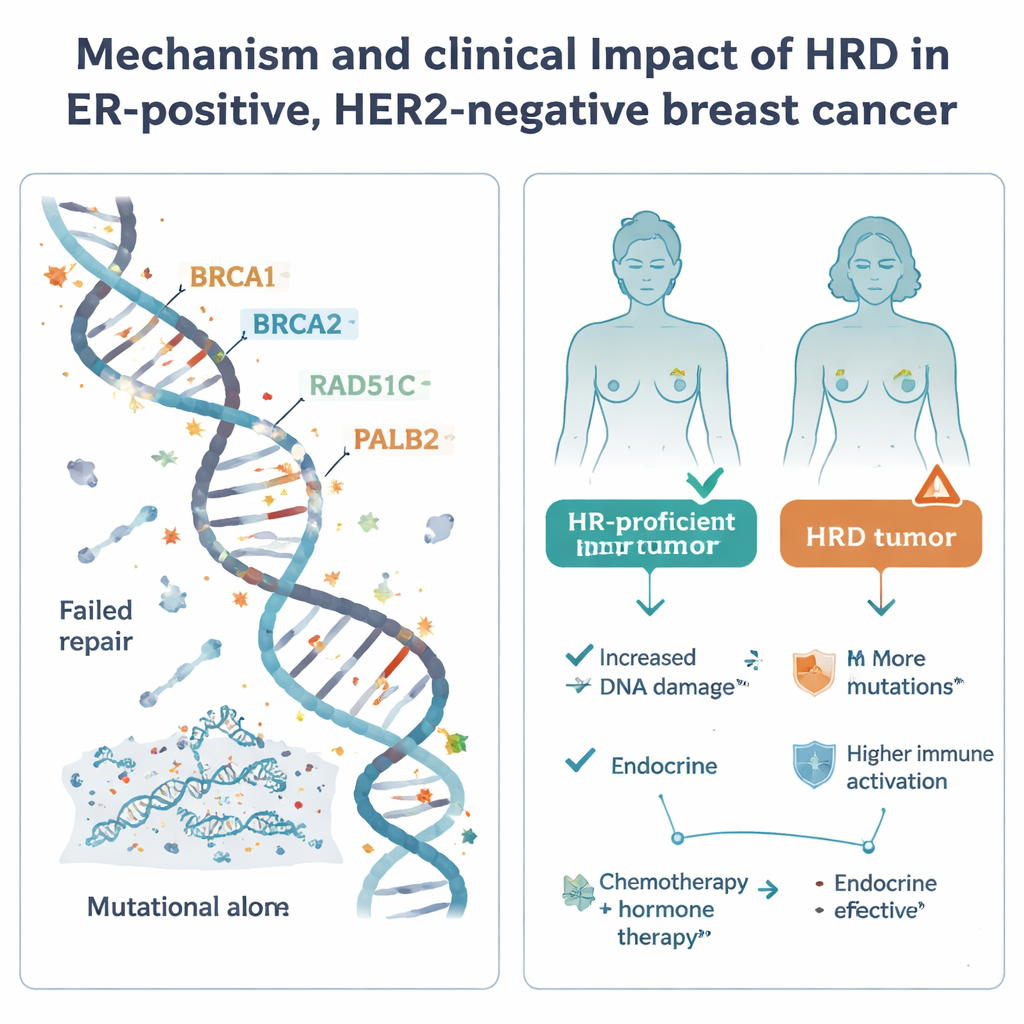
Påverkar HRD patientutfallet?
Studien undersökte sedan hur HRD‑status förhöll sig till verkliga utfall under standardvård. Hos patienter som behandlades med endokrin terapi ensam efter operation visade HRD‑tumörer en tendens till sämre fjärrrecidivfritt överlevnad, även om antalet HRD‑fall var litet och resultatet inte nådde formell statistisk signifikans. Detta mönster, tillsammans med deras aggressiva molekylära drag, tyder på att förlita sig enbart på endokrin behandling kan vara riskfyllt för patienter med HRD‑tumörer. Däremot, bland patienter som fick både cytostatika och hormonbehandling, var HRD‑status inte tydligt kopplad till bättre eller sämre utfall; alla grupper hade i stort sett liknande återfallsfrekvenser, och cytostatika kan dämpa en del av den ökade risken i HRD‑tumörer.
Vad detta betyder för framtida behandlingsval
För en allmän läsare är huvudbudskapet att bara en minoritet av östrogenreceptorpositiva, HER2‑negativa bröstcancrar bär denna särskilda DNA‑reparationssvaghet, men när den finns tenderar den att markera en mer aggressiv sjukdom som kanske inte kontrolleras väl av enbart hormonbehandling. Arbetet stödjer idén att helgenomssekvensering kan flagga HRD på ett tillförlitligt sätt och klarlägga dess bakomliggande orsaker, utöver att bara testa för ärftliga BRCA1‑ eller BRCA2‑mutationer. Även om studien ännu inte bevisar att förändrad behandling baserat på HRD‑status förbättrar överlevnaden, ger den tidiga bevis för att patienter med HRD‑tumörer kan gynnas av cytostatika och i framtida studier av PARP‑hämmare eller immunterapier. Sammanfattningsvis skulle HRD‑testning kunna bli en del av en mer förfinad verktygslåda för att skräddarsy behandlingsintensitet — och nya målinriktade alternativ — efter biologin i varje patients bröstcancer.
Citering: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
Nyckelord: bröstcancer, DNA‑reparation, BRCA‑gener, genomsekvensering, målinriktad behandling